Фосфорная кислота – одно из важных химических соединений, которое обладает широким спектром применения в различных отраслях промышленности. Особый интерес вызывает ее взаимодействие с металлами, которое ведет к образованию фосфатов – веществ, наиболее активно используемых в производстве удобрений и других химических соединений. В данной статье рассмотрим особенности реакций фосфорной кислоты с различными металлами и их применение.
Взаимодействие фосфорной кислоты с металлами происходит путем замещения одного или нескольких атомов водорода в кислоте атомами металла. Это обусловлено высокой кислотностью фосфорной кислоты и ее способностью образовывать стабильные соединения с металлами. Реакции с металлами протекают с выделением водорода и образованием солей фосфорной кислоты – фосфатов.
Особенностью взаимодействия фосфорной кислоты с металлами является возможность использования различных концентраций и температур, что позволяет получать разные соединения с желаемыми свойствами. Каждая комбинация металла и фосфатной кислоты может иметь свои уникальные физические и химические свойства, что делает их применение широким и разнообразным.
Реакции взаимодействия фосфорной кислоты с металлами
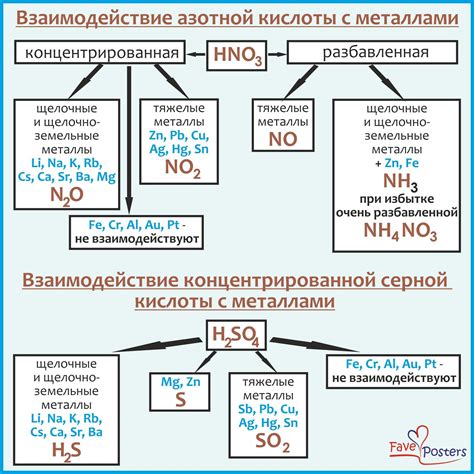
Фосфорная кислота обладает высокой химической активностью и способна взаимодействовать с многими металлами. Реакции ее взаимодействия с металлами проявляются в различных формах и могут быть как спонтанными, так и провоцируемыми.
В результате реакции фосфорной кислоты с некоторыми металлами образуются соответствующие фосфаты металлов. Фосфаты металлов обладают различными свойствами и находят широкое применение в различных областях, включая производство удобрений, стекла, керамики и многих других материалов.
Важно отметить, что реакции взаимодействия фосфорной кислоты с металлами могут протекать как в водных растворах, так и в плавающих металлах. В водных растворах реакция может сопровождаться выделением водорода и образованием кислых солей, а в случае плавающих металлов может происходить поплавление металла и образование сплавов с фосфором.
Реакции взаимодействия фосфорной кислоты с металлами обладают высоким практическим значением и широко используются в различных отраслях промышленности. Они не только позволяют получать ценные продукты, но и являются основой для разработки новых технологий и материалов, которые могут быть использованы в различных сферах деятельности человека.
Фосфорная кислота: свойства и применение

Фосфорная кислота – это химическое соединение, состоящее из трех атомов водорода, одного атома фосфора и четырех атомов кислорода. Она обладает высокой степенью кислотности, и ее химическая формула обычно обозначается H3PO4.
Основным свойством фосфорной кислоты является ее растворимость в воде. При добавлении фосфорной кислоты в воду происходит выделение тепла, что связано с эндотермической реакцией гидратации. Это явление широко используется в химической промышленности для получения концентрированных растворов фосфорной кислоты.
Фосфорная кислота имеет широкое применение в различных отраслях промышленности. Она является основным сырьем для производства многочисленных продуктов, таких как удобрения, пищевые добавки, фосфаты для производства стекла и шамотные огнеупоры. Благодаря своей кислотности, фосфорная кислота также используется в металлургии для удаления окислов и загрязнений с поверхности металлов.
Химические реакции фосфорной кислоты с металлами
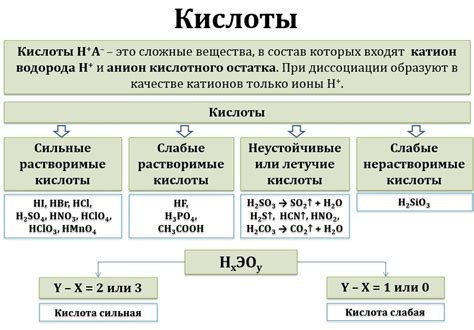
Фосфорная кислота (H3PO4) - это одна из самых распространенных бинарных кислот, которая широко применяется в различных отраслях промышленности. Взаимодействие фосфорной кислоты с металлами протекает с образованием соответствующих солей - фосфатов, а также выделением водорода.
Соли фосфорной кислоты имеют важное значение в сельском хозяйстве и производстве удобрений. В результате реакции фосфорной кислоты с металлами образуются различные фосфаты: монофосфаты (MH2PO4), дифосфаты (MHPO4) и трифосфаты (MPO4). Эти соли используются для улучшения качества и плодородия почв, а также в производстве минеральных удобрений.
Некоторые металлы образуют с фосфорной кислотой комлексы. Например, с кальцием (Ca) и алюминием (Al) фосфорная кислота образует кальцийфосфат (CaHPO4) и алюмофосфат (AlPO4) соответственно. Эти вещества имеют широкое применение в производстве лекарственных препаратов, пищевых добавок и других промышленных продуктов.
Взаимодействие фосфорной кислоты с активными металлами, такими как натрий (Na) и калий (K), протекает с образованием фосфатов и выделением водорода. Реакция можно представить следующим образом:
2H3PO4 + 6Na → 2Na3PO4 + 3H2
В целом, реакции фосфорной кислоты с металлами имеют большое практическое значение и находят свое применение в различных отраслях промышленности и сельском хозяйстве.
Режимы фосфатирования металлов

Фосфатирование металлов – это процесс нанесения на металлическую поверхность защитного слоя фосфатов. Режимы фосфатирования металлов могут быть различными и зависят от типа металла, его состояния, цели обработки и требований к предельным значениям. Режимы фосфатирования обычно включают несколько этапов, таких как очистка и предварительная обработка поверхности, нанесение фосфатного покрытия и последующая обработка.
Один из основных режимов фосфатирования металлов – это холодное фосфатирование. Оно подразумевает обработку металла в холодном состоянии, без применения высоких температур. Холодное фосфатирование обычно выполняется путем погружения металла в раствор фосфатной кислоты или прохождения металла через фосфатирующий раствор. Этот метод позволяет получить тонкое и равномерное фосфатное покрытие, обладающее хорошей адгезией.
Еще одним из распространенных режимов фосфатирования металлов является термическое фосфатирование. В этом случае металл нагревается до определенной температуры, что приводит к реакции фосфорной кислоты с поверхностью металла. Термическое фосфатирование обеспечивает более прочное и долговечное фосфатное покрытие, которое может использоваться для защиты металла от коррозии и повышения его адгезии к окрашиваемым покрытиям.
Выбор режима фосфатирования металлов зависит от требований по качеству покрытия, долговечности и особенностей конкретного металла. Кроме того, режим фосфатирования может быть комбинированным, когда используются различные методы обработки для достижения оптимальных результатов. Важно правильно выбирать режим фосфатирования и выполнять все этапы процесса с соблюдением требований и рекомендаций, чтобы получить качественное и долговечное фосфатное покрытие на металлической поверхности.
Особенности взаимодействия фосфорной кислоты с различными металлами
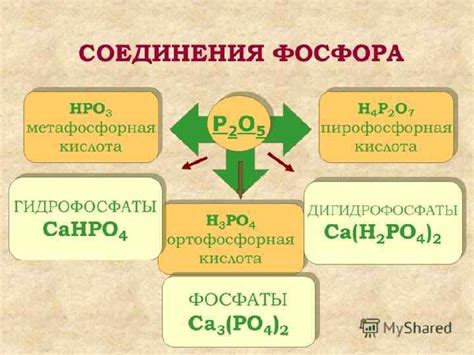
Фосфорная кислота, или ортофосфорная кислота (H3PO4), проявляет свои химические свойства при взаимодействии с различными металлами. На основе этих свойств, ее можно использовать в различных технологических процессах и синтезах.
Взаимодействие фосфорной кислоты с металлами приводит к образованию фосфатов, которые являются солью данной кислоты. Фосфаты могут быть как растворимыми, так и нерастворимыми в воде, в зависимости от металла, с которым происходит реакция. Например, при взаимодействии с щелочными металлами (например, натрием, калием) образуются растворимые фосфаты, которые хорошо растворяются в воде.
Взаимодействие фосфорной кислоты с некоторыми металлами, такими как железо, алюминий или цинк, может приводить к образованию пассивной защитной пленки на металлической поверхности. Это обусловлено образованием инертного соединения, которое защищает металл от коррозии или других воздействий.
Также, фосфорная кислота может использоваться для удаления ржавчины или других загрязнений со металлических поверхностей. Она способна растворять окисленные слои и образовывать растворимые фосфаты, которые затем можно легко удалить.
Влияние концентрации фосфорной кислоты на процесс реакции

Фосфорная кислота – химическое вещество, обладающее кислотными свойствами и широко применяемое в различных отраслях промышленности. Данная кислота способна реагировать с различными металлами, образуя соединения и сопутствующие реакционные продукты.
Интересно отметить, что влияние концентрации фосфорной кислоты на процесс реакции между кислотой и металлами является важным фактором. При низкой концентрации кислоты может происходить не полная реакция, что приводит к образованию нежелательных побочных продуктов. Более высокая концентрация кислоты, в свою очередь, может способствовать усилению химической реакции и повышению эффективности процесса.
Чтобы определить оптимальную концентрацию фосфорной кислоты для проведения реакции с конкретным металлом, можно провести серию экспериментов, варьируя концентрацию кислоты и наблюдая изменение скорости процесса и образование продуктов реакции. Таким образом, удастся определить наилучшие условия для взаимодействия данных веществ, что позволит получить желаемый результат с минимальными потерями и нежелательными побочными эффектами.
Применение фосфорных соединений в металлургической и электротехнической отрасли

Фосфорные соединения широко применяются в металлургической и электротехнической отрасли благодаря своим уникальным свойствам. Одним из основных применений фосфора в металлургии является его использование в качестве добавки при производстве стали. При добавлении фосфора происходит улучшение механических свойств стали, ее стойкость к коррозии и способность к обработке. Также фосфорные соединения используются для удаления нежелательных примесей из металлических сплавов, что позволяет получить материалы с более высокой прочностью и химической стабильностью.
В электротехнической отрасли фосфорные соединения широко применяются для производства электрических проводов и кабелей. Фосфорные комплексы обладают высокой огнестойкостью и низкой дымообразующей способностью, что делает их идеальным материалом для создания пожаробезопасных электрокабелей. Кроме того, фосфорные соединения используются в производстве паяльных и сварочных материалов, так как они способны обладать низкой температурой плавления и высокой прочностью соединения.
Фосфорные соединения также применяются в электролитическом производстве металлов. Они участвуют в процессе электролиза и обеспечивают эффективное осаждение и очистку металлических ионообразующих растворов. В процессе гальванического покрытия фосфатные соединения используются для создания защитных покрытий, которые обеспечивают повышенную стойкость к коррозии и старению металлических поверхностей.
В заключение, фосфорные соединения играют важную роль в металлургической и электротехнической отрасли, обеспечивая повышение качества металлических материалов, создание пожаробезопасных электрических систем и обеспечение надежного покрытия на металлических поверхностях. Их уникальные свойства и высокая химическая активность делают их незаменимыми компонентами при производстве различных изделий и материалов в этих отраслях.
Вопрос-ответ

Какая роль фосфорной кислоты взаимодействии с металлами?
Фосфорная кислота может реагировать с металлами, образуя соли. Она может служить в качестве основания или кислоты, в зависимости от условий реакции.
Каким образом фосфорная кислота взаимодействует с алюминием?
Фосфорная кислота и алюминий реагируют друг с другом, образуя алюминийфосфат и выделяя водород. Эта реакция является экзотермической и ведется быстро, особенно при нагреве.
На что следует обратить внимание при взаимодействии фосфорной кислоты с металлами?
При взаимодействии фосфорной кислоты с металлами следует быть осторожным, так как реакция может сопровождаться выделением водорода и образованием токсичных газов. Также важно учитывать, что реакции могут проходить с выделением большого количества тепла.
Какие металлы могут реагировать с фосфорной кислотой?
Фосфорная кислота может реагировать с различными металлами, такими как алюминий, железо, цинк, натрий и др. Однако, скорость и интенсивность реакции могут зависеть от свойств конкретного металла и условий взаимодействия.
Какова химическая реакция между фосфорной кислотой и железом?
При взаимодействии фосфорной кислоты и железа образуется соединение - фосфат железа(III). Эту реакцию можно представить следующим уравнением: 2 H3PO4 + 3 Fe -> 2 FePO4 + 3 H2.




