Реакция этилового спирта с металлом является одним из классических примеров органической химии. Этот химический процесс имеет особенности, которые определяют его применение в различных областях науки и промышленности.
Одной из особенностей реакции этилового спирта с металлами является возможность образования гидридов, т.е. соединений, состоящих из металлического атома и водорода. При этом происходит замещение одного или нескольких атомов водорода в молекуле спирта. Этот процесс может быть использован для получения чистого водорода, который в последующем может быть использован в различных химических реакциях или как источник энергии.
Кроме того, реакция этилового спирта с металлом может приводить к образованию различных органических соединений. Один из самых известных примеров такой реакции - образование этилацетатa. Эта смесь используется в парфюмерии и косметической промышленности, а также в производстве растворителей. Также реакция спирта с металлом может приводить к образованию органических кислот, которые могут быть использованы в производстве пластмасс, лекарств и других продуктов.
Химические свойства этилового спирта
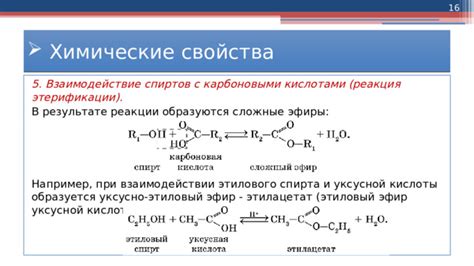
Этиловый спирт, или этиловый спирт, также известный как алкоголь этиловый, является одной из наиболее распространенных и широко используемых органических соединений. Он имеет химическую формулу C2H5OH и обладает рядом уникальных свойств, которые делают его полезным в различных областях жизни.
Одним из основных химических свойств этилового спирта является его способность реагировать с металлами. При взаимодействии с металлом происходит окислительно-восстановительная реакция, в результате которой образуются соответствующие соли и выделяется водород.
Процесс реакции этилового спирта с металлом зависит от активности металла. Наиболее реактивные металлы, такие как натрий и калий, быстро реагируют с этиловым спиртом, выделяя большое количество водорода и образуя алкоксиды металлов.
Более инертные металлы, такие как алюминий и цинк, реагируют медленнее с этиловым спиртом, образуя оксиды и алкоксиды металлов. В реакции с этиловым спиртом эти металлы не выделяют значительного количества водорода.
Реакция этилового спирта с металлами может быть полезна в различных применениях. Например, она может использоваться для очистки и полировки металлических поверхностей. Этиловый спирт обладает высокой растворимостью и может легко удалять загрязнения и окислительные пленки с поверхности металла.
Кроме того, реакция этилового спирта с металлами может использоваться в качестве метода синтеза органических соединений. Например, в органическом синтезе этиловый спирт может служить источником этилового заместителя при замещении хлорида активным металлом.
Активность металлов в реакции

Реакция этилового спирта с металлом - это химическая реакция, при которой этиловый спирт вступает во взаимодействие с металлическим элементом. Активность металлов в этой реакции определяется их электрохимической реактивностью.
Наиболее активные металлы, такие как калий, натрий и литий, сильно реагируют с этиловым спиртом, вызывая выделение водорода и образование соответствующих металлических спиртатов. Их реактивность объясняется низкой ионизационной энергией и высоким окислительным потенциалом.
Менее активные металлы, такие как магний, цинк и алюминий, также могут реагировать с этиловым спиртом, но не так интенсивно. В этом случае образуется металлический спиртат и выделяется водород. Реакция сильнее проявляется в присутствии кислорода или воды, что может вызвать возгорание.
Менее реактивные металлы, такие как железо и медь, обычно не реагируют с этиловым спиртом при обычных условиях. Это объясняется их более высокой электрохимической стабильностью и меньшей способностью отдавать электроны.
Таким образом, активность металлов в реакции с этиловым спиртом определяет степень и скорость реакции, а также возможность образования опасных продуктов реакции. Поэтому необходимо быть осторожным при проведении реакции и соблюдать все необходимые меры предосторожности.
Токсичность продуктов реакции
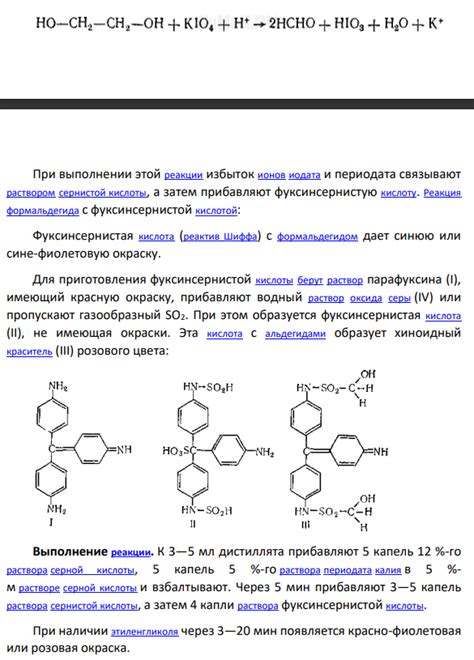
Реакция этилового спирта с металлом может привести к образованию определенных продуктов, содержащих токсичные вещества. Эти продукты могут быть опасными для здоровья человека при вдыхании, контакте с кожей или попадании в организм.
Один из основных продуктов реакции этилового спирта с металлом - этанолат металла (этиловый спиртат). Этот соединение может вызывать раздражение кожи, слизистых оболочек и дыхательных путей при вдыхании его паров.
Также в результате реакции этилового спирта с металлом могут образовываться другие токсичные соединения, такие, как карбонилы металлов. Некоторые из них могут вызывать отравление при контакте с кожей или попадании внутрь организма.
Поэтому важно соблюдать меры безопасности при работе с этиловым спиртом и металлами. Необходимо обеспечить хорошую вентиляцию помещения, использовать защитные перчатки и средства индивидуальной защиты, чтобы избежать непосредственного контакта с токсичными продуктами реакции. Также рекомендуется проводить работы под контролем и в соответствии с правилами безопасности.
Применение реакции с этиловым спиртом

1. Получение эфиров. Одним из основных применений реакции этилового спирта с металлом является получение эфиров. При взаимодействии этилового спирта с кислотами или кислородсодержащими соединениями в присутствии катализаторов на металлической основе, происходит образование эфиров. Это реакция называется эфированием и широко используется в органическом синтезе.
2. Производство растворителей. Реакция этилового спирта с металлом может быть использована для получения различных растворителей. Например, в результате взаимодействия этилового спирта с натрием или калием образуется этиловый спиртат, который является одним из основных компонентов растворителя для лакокрасочных материалов. Также этиловый спирт может служить основой для получения других растворителей, таких как этиловый эфир или этиленгликоль.
3. Выделение солей. Реакция этилового спирта с металлом может применяться для выделения солей из растворов. При взаимодействии этилового спирта с металлическими солями происходит образование этиловых соединений с элементом металла. Эти соединения обладают хорошей растворимостью в этиловом спирте, что позволяет выделить соли в виде осадка и использовать их в дальнейших химических реакциях.
4. Получение эфиров красителей и ароматических веществ. Эфиры, полученные в результате реакции этилового спирта с металлом, могут служить основой для синтеза различных органических соединений. Например, этиловый спирт может быть использован для получения эфиров красителей и ароматических веществ, которые находят широкое применение в пищевой, парфюмерной и косметической промышленности.
5. Анализ вредных веществ. Реакция этилового спирта с металлом может использоваться для анализа вредных веществ в промышленных и природных образцах. При взаимодействии этилового спирта с металлами, такими как натрий или калий, происходит образование спиртатов, которые обладают специфическими физико-химическими свойствами. Эти свойства можно использовать для выявления наличия и концентрации определенных веществ в образцах.
Вопрос-ответ

Как происходит реакция этилового спирта с металлом?
Реакция этилового спирта с металлом протекает через образование гидрида металла. Эта реакция является реакцией окисления, в результате которой образуется соответствующий гидроксид и выделяется водород.
Какие металлы могут реагировать с этиловым спиртом?
Некоторые активные металлы, такие как натрий, калий и литий, могут реагировать с этиловым спиртом. Эти металлы образуют гидриды, которые можно использовать в различных химических реакциях и синтезах.
Каковы применения реакции этилового спирта с металлом?
Применение реакции этилового спирта с металлом заключается в получении гидридов металлов. Гидриды металлов являются важными реагентами в химической промышленности и используются в различных синтезах и органических реакциях.
