Реакция азотной кислоты с металлами при нагревании представляет собой важный объект исследования в области химии и может иметь различные особенности в зависимости от металла и условий реакции. Азотная кислота (HNO3) является сильным окислителем и обладает способностью разлагаться с выделением кислорода и образованием окислов азота. Она может реагировать с металлами при нагревании, образуя различные реакционные продукты.
При нагревании азотной кислоты с некоторыми металлами, например, железом (Fe), наблюдается реакция горения металла в окислительной среде. Железо окисляется до высших окислительных состояний, образуя оксиды железа. В результате реакции образуются различные соли и оксид азота, которые можно обнаружить и изучить с помощью химических анализов.
Интересной особенностью реакции азотной кислоты с металлами при нагревании является образование не только солей, но и нитратов металлов. Нитраты – соли азотной кислоты – могут быть использованы в различных промышленных и химических процессах. Их свойства зависят от металла, с которым они образуются, и могут быть использованы в качестве удобрений, пищевых добавок и других промышленных продуктов.
В заключениие:
Таким образом, реакция азотной кислоты с металлами при нагревании представляет собой сложный процесс, который может приводить к образованию различных реакционных продуктов. Изучение этих реакций позволяет не только понять особенности взаимодействия между азотной кислотой и металлами, но и найти новые способы использования полученных продуктов в промышленности.
Влияние нагревания на реакцию азотной кислоты с металлами

Реакция азотной кислоты с металлами при нагревании является одной из важных химических реакций, которая происходит в результате взаимодействия азотной кислоты с различными металлическими элементами. Нагревание играет ключевую роль в этом процессе, поскольку ускоряет ход реакции и обеспечивает образование новых реакционных продуктов.
Влияние нагревания на реакцию зависит от свойств и химической активности конкретного металла. Некоторые металлы, например, медь и серебро, реагируют с азотной кислотой довольно медленно при комнатной температуре. Однако, при нагревании сильно ускоряется процесс реакции и образуются соответствующие нитраты этих металлов.
Другие металлы, такие как железо или алюминий, более активно реагируют с азотной кислотой уже при комнатной температуре. При нагревании происходит интенсификация данной реакции, что приводит к образованию нитратов данных металлов.
В общем случае, нагревание металлов с азотной кислотой приводит к образованию соответствующих нитратов, которые можно использовать в различных отраслях промышленности, таких как химическая или сельскохозяйственная. Температура нагревания оказывает существенное влияние на скорость реакции и образование конечных продуктов, что подтверждает важность контроля этого параметра при проведении подобных реакций.
Реакция азотной кислоты с металлами: что происходит?

Реакция азотной кислоты с металлами является одной из важных реакций, которая приводит к образованию нитратов и оксидов металлов. При нагревании азотной кислоты с металлом происходит окислительно-восстановительная реакция, в результате которой образуются соответствующие соли и газообразные продукты.
В зависимости от свойств металлов, происходящая реакция может проходить с разной интенсивностью. Легкие металлы, такие как магний и алюминий, реагируют с азотной кислотой очень активно, выделяя большое количество газа и образуя нитраты. Тяжелые металлы, например, железо или свинец, могут реагировать с азотной кислотой медленнее и образовывать оксиды и нитраты.
Процесс реакции азотной кислоты с металлами является экзотермическим, то есть сопровождается выделением тепла. Это объясняет нагревание смеси при проведении данной реакции. Кроме того, в процессе реакции могут образовываться ядовитые газы, такие как оксид азота, которые следует обрабатывать в специальных условиях или удалить с помощью газоочистки.
Особенности взаимодействия азотной кислоты с металлами при нагревании
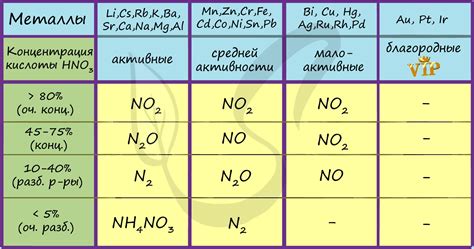
Азотная кислота (HNO3) является сильной окислительной кислотой, и ее взаимодействие с металлами при нагревании имеет свои особенности.
При взаимодействии азотной кислоты с металлами происходит окисление металла за счет кислорода, присутствующего в кислоте. Реакция сопровождается выделением газообразных продуктов, образованием соединений металла с кислородом и образованием нитратов.
Одной из особенностей реакции является быстрая реакция с металлами активными, такими как железо, цинк и алюминий. При нагревании этих металлов с азотной кислотой образуется большое количество газа, который сопровождается знакомыми нам пузырьками.
Следует отметить, что металлы, которые покрыты защитной оксидной пленкой, проявляют меньшую реакционную активность при взаимодействии с азотной кислотой. Это связано с тем, что оксидная пленка препятствует проникновению кислоты к металлической поверхности. Однако, при нагревании, оксидная пленка может разрушаться, и реакция будет протекать более интенсивно.
В результате реакции азотной кислоты с металлами образуются нитраты. Нитраты имеют сольную природу, и их свойства и применение определяютс
Реакционные продукты обработки металлов азотной кислотой при нагревании

Реакция металлов с азотной кислотой при нагревании является одной из важных реакций в химии. При этой реакции образуются различные продукты в зависимости от свойств и типа металла.
Сначала необходимо отметить, что азотная кислота (HNO3) является окислителем, что означает, что она способна отбирать электроны у металлов. При нагревании, металлы реагируют с азотной кислотой, выделяя диоксид азота (NO2) и образуя соответствующие соли металлов.
Например, реакция азотной кислоты с железом приводит к образованию нитрата железа (Fe(NO3)3) и выделению диоксида азота:
- 4Fe + 10HNO3 → 4Fe(NO3)3 + 5H2O + 2NO2
Аналогично, реакция с азотной кислотой может привести к образованию нитратов других металлов, таких как цинк, медь или свинец, в зависимости от используемого металла. При этом также выделяется диоксид азота.
Таким образом, реакция азотной кислоты с металлами при нагревании приводит к образованию нитратов и диоксида азота. Эта реакция имеет широкое применение в различных областях, включая производство удобрений, химические реакции и лабораторные эксперименты.
Вопрос-ответ

Какая реакция происходит между азотной кислотой и металлами при нагревании?
При нагревании азотной кислоты с металлами происходит реакция окисления, при которой металлы окисляются до соответствующих оксидов, а азотная кислота восстанавливается до азотного оксида или газообразного азота.
Какие особенности есть в реакции азотной кислоты с металлами?
Особенностью реакции азотной кислоты с металлами является то, что она происходит при низких температурах и в условиях недостатка кислорода. Это связано с тем, что азотная кислота, в отличие от других окислителей, сама является окислителем и может восстанавливаться до азотных оксидов.
Какие реакционные продукты могут образоваться при взаимодействии азотной кислоты с металлами при нагревании?
При взаимодействии азотной кислоты с металлами могут образовываться различные реакционные продукты. Например, с некоторыми металлами (например, медью) могут образовываться азотные оксиды, а при взаимодействии с другими металлами (например, железом) могут образовываться аммиак и азотистые соединения.
Почему азотная кислота проявляет окислительные свойства при реакции с металлами?
Азотная кислота проявляет окислительные свойства при реакции с металлами из-за наличия в ее составе атомов азота с высокой степенью окисления. При взаимодействии с металлом азотная кислота окисляет металл, передавая ему свои электроны и сама восстанавливаясь до азотных оксидов.
Какие металлы реагируют с азотной кислотой при нагревании?
Реакция азотной кислоты с металлами при нагревании происходит с различными металлами, включая железо, медь, цинк и некоторые другие. Однако, не все металлы реагируют с азотной кислотой, так как их активность может быть недостаточной для вступления в реакцию.
