Взаимодействие металлов с кислотами является одной из важных химических реакций. Многие металлы реагируют с азотной кислотой, образуя соединения, которые широко используются в промышленности и научных исследованиях.
Однако влияние водорода на течение реакции азотной кислоты с металлами является весьма интересным и значимым для понимания основных аспектов данного процесса. Водород, который образуется в результате реакции, может оказывать как положительное, так и отрицательное воздействие на характер и эффективность взаимодействия металла с кислотой.
С одной стороны, водород может ускорять течение реакции, образуя комплексы с металлом и кислотой. Комплексы водорода с металлами могут обладать высокой активностью и способствовать разрушительным реакциям. С другой стороны, водород может замедлять процесс реакции и снижать ее активность. Образуемая металлом пленка водорода может препятствовать дальнейшему растворению металла в кислоте.
Влияние водорода на процесс взаимодействия азотной кислоты с металлами
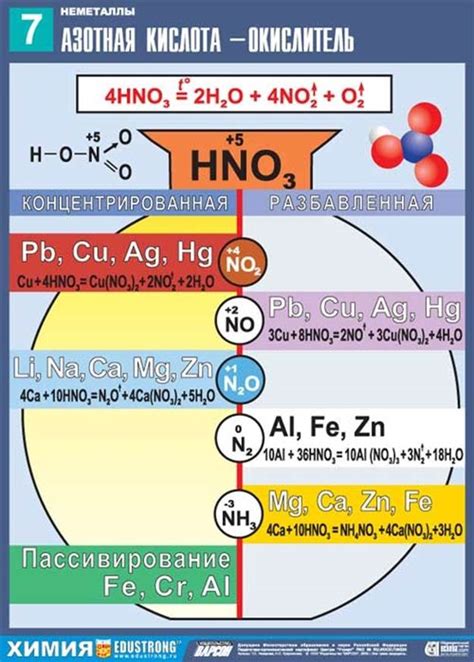
Азотная кислота (HNO3) обладает сильной окисляющей способностью и может реагировать с различными металлами. Важное влияние на характер и скорость реакции азотной кислоты с металлами оказывает присутствие водорода.
Водород, который образуется в результате взаимодействия азотной кислоты с металлами, участвует в химических реакциях и может изменить ход процесса. Например, водород может образовывать воду, что способствует ускорению реакции. Также водород может обладать редокс-активностью, то есть участвовать в окислительно-восстановительных реакциях.
Взаимодействие азотной кислоты с различными металлами может привести к образованию нитратов и аммониевых соединений. Образование нитратов особенно интенсивно происходит в присутствии водорода. Так, например, азотная кислота может реагировать с железом, образуя нитрат железа(III) и аммиак:
- 3HNO3 + 2Fe → 2Fe(NO3)3 + 3H2O + 2NH3
Этот процесс можно использовать для получения необходимых нитратов и аммиака в промышленных масштабах.
Интересно, что влияние водорода на реакцию азотной кислоты с металлами может быть различным в зависимости от условий. Гидрогенация азотной кислоты, то есть процесс её превращения в аммиак, может происходить при повышенной температуре и давлении в присутствии каталитического вещества, такого как платина или никель. Этот процесс является важным в производстве аммиака, который в дальнейшем используется для производства удобрений и других химических соединений.
Таким образом, влияние водорода на процесс взаимодействия азотной кислоты с металлами может быть разнообразным и зависит от множества факторов, включая условия реакции и свойства используемых веществ.
Физические свойства азотной кислоты и ее роль в химических реакциях

Азотная кислота (HNO3) - безцветная жидкость с характерным резким запахом. Она является сильным окислителем и кислотой, растворяется в воде и этиловом спирте, образуя концентрированные растворы.
Азотная кислота хорошо растворяет металлы, такие как железо, медь, цинк и алюминий. При этом происходит химическая реакция, в результате которой образуется результат химического процесса. Возможен образование нитратов или аммиакатов металлов в растворе.
Уксусная кислота также влияет на реакцию азотной кислоты с металлами. Образуется газовый пузырь из аммиака, который можно обнаружить по характерному запаху.
При реакции с металлами азотная кислота также сопровождается выделением газа - водорода. Для реакции с поблочной линейкой металлов сформирован ряд реакционной активности. У марганца водород освобождается просто при разбавлении кислоты водой. Железо и алюминий взаимодействуют с ней при нагревании продуктов и нет освобождения газа в процессе непосредственного взаимодействия с кислотой.
- Азотная кислота широко используется в производстве удобрений и взрывчатых веществ;
- Она также применяется в лабораторной практике в качестве кислотного катализатора;
- Азотная кислота используется в промышленности для получения нитробензола, нитроглицерина, азотной кислоты и других химических соединений;
- Она также применяется в химической аналитике для определения концентрации металлических и неорганических соединений.
Азотная кислота является важным химическим соединением, играющим значительную роль в различных производствах и химических процессах. Ее физические свойства и реакционная способность с металлами позволяют ей успешно выполнять свою функцию в химической промышленности и научных исследованиях.
Взаимодействие азотной кислоты с металлами: особенности и механизмы
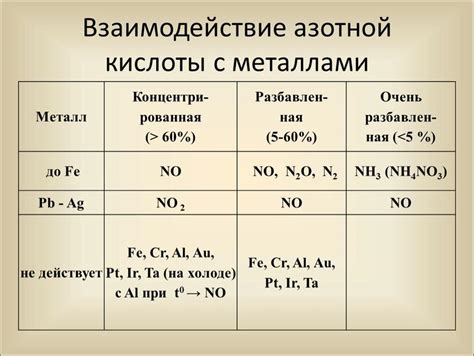
Азотная кислота – это химическое соединение, состоящее из азота, кислорода и воды. Взаимодействие данного соединения с металлами является одним из важных процессов в химии и может протекать по различным механизмам в зависимости от условий и среды.
Одним из основных механизмов взаимодействия азотной кислоты с металлами является окислительно-восстановительная реакция. В данной реакции азотная кислота служит окислителем, передавая свои кислородные атомы металлу. В результате происходит окисление металла и образование соответствующего оксида.
Еще одним механизмом взаимодействия азотной кислоты с металлами является образование нитратов. При этом азотная кислота реагирует с металлом, образуя нитратную соль. Эта реакция обычно протекает при высоких температурах и может сопровождаться выделением газов.
Особенностью взаимодействия азотной кислоты с металлами является ее высокая реакционность и агрессивность. Азотная кислота может вызвать коррозию металлов и разрушение их структуры. Поэтому при работе с азотной кислотой необходимо соблюдать особые меры предосторожности и использовать соответствующую защитную экипировку.
Потенциальные применения водорода в реакциях с азотной кислотой и металлами
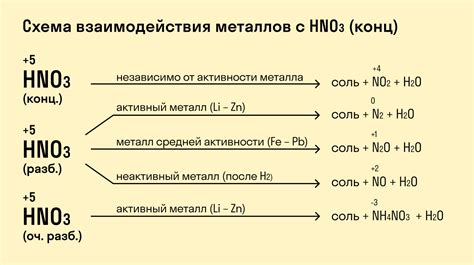
Взаимодействие водорода с азотной кислотой и металлами является важным направлением исследований в области химии и материаловедения. Эти реакции имеют потенциальное применение в различных областях науки и технологий.
Одним из потенциальных применений водорода в реакциях с азотной кислотой и металлами является производство аммиака. Аммиак широко используется в производстве удобрений, а также в качестве промышленного растворителя. Использование водорода в реакции с азотной кислотой и металлами может предложить новые, более эффективные пути синтеза аммиака.
Еще одним потенциальным применением водорода является водородная активация азотной кислоты и металлов. Водород может служить активатором для реакций, связанных с азотной кислотой и металлами, что может привести к образованию новых полезных соединений. Такие реакции могут быть использованы в синтезе новых материалов с улучшенными свойствами.
Кроме того, водород способен взаимодействовать с азотной кислотой и металлами при высоких температурах, что может быть использовано в процессах высокотемпературного катализа. Водородные реакции могут способствовать активации азотной кислоты и металлов, что открывает новые возможности для эффективного применения катализаторов в процессах обработки газов, производства энергии и других промышленных процессах.
Основные вызывающие интерес вопросы и перспективы дальнейших исследований

Интерес к вопросу о влиянии водорода на реакцию азотной кислоты с металлами вызывается рядом неизученных аспектов этого процесса. Одним из ключевых вопросов является определение механизма взаимодействия водорода с азотной кислотой и металлами.
Важно исследование влияния различных условий на скорость и характер реакции. Например, можно исследовать влияние концентрации азотной кислоты и металла, температуры, давления и других параметров на степень окисления металла и выделение водорода.
Продолжение исследований позволит уточнить кинетические и термодинамические параметры реакции и определить ее эффективность. Это может иметь практическое применение в различных областях, включая производство водорода, разработку новых материалов или каталитических процессов.
Также интерес представляет возможность управления реакцией азотной кислоты с металлами путем изменения условий или добавления катализаторов. Это открывает перспективы разработки новых методов синтеза и обработки материалов, а также применения данных процессов в экологически чистых технологиях.
Для достижения этих целей необходимо проводить систематические исследования с использованием разных методов анализа и контроля реакции. Кроме того, важно учесть особенности электрохимического взаимодействия между водородом, азотной кислотой и металлом, поскольку эти процессы могут иметь значительное влияние на характер реакции.
Вопрос-ответ

Как водород влияет на реакцию азотной кислоты с металлами?
Водород может влиять на реакцию азотной кислоты с металлами различными способами. Он может служить реагентом, образуя при взаимодействии с кислотой аммиак, который обладает щелочными свойствами и может осаждать ионы металлов. Также водород может вступать в реакцию с образовавшимися ионами металла и образовывать газы. Водород может также присутствовать в среде как растворитель и влиять на скорость и направление реакции.
Какие металлы реагируют с азотной кислотой в присутствии водорода?
В присутствии водорода с азотной кислотой могут реагировать различные металлы, такие как железо, цинк, медь и др. Реакция может протекать с образованием аммиака и нитритов металлов. При этом водород может образовывать пузырьки, которые видны на поверхности металла.
Каков механизм реакции азотной кислоты с металлами в присутствии водорода?
Механизм реакции азотной кислоты с металлами в присутствии водорода может быть сложным и зависит от условий проведения реакции. Одним из возможных механизмов является реакция взаимодействия металла с кислотой, при которой образуется соль, а водород выделяется в виде газа. В другом случае металл может реагировать с аммиаком, образованным при реакции кислоты с водородом, и образовывать амминийные соединения.
Какова практическая значимость реакции азотной кислоты с металлами в присутствии водорода?
Реакция азотной кислоты с металлами в присутствии водорода имеет практическую значимость в различных областях науки и техники. Например, она может использоваться для получения азотистых соединений, которые в дальнейшем могут применяться в производстве удобрений или в качестве реагентов в органическом синтезе. Также реакция может быть использована для очистки металлических поверхностей от окислов и покрытий, а также для электрохимического нанесения металлических покрытий на различные материалы.
