Щелочные металлы, такие как литий (Li), натрий (Na), калий (K) и другие, являются химически активными элементами, способными образовывать различные соединения. Одним из интересных исследовательских направлений в области химии щелочных металлов является изучение их взаимодействия с фосфором.
Фосфор - химический элемент с символом P и атомным номером 15. Он является необходимым компонентом живых организмов и широко применяется в промышленности. Взаимодействие щелочных металлов с фосфором может привести к образованию различных фосфидов - соединений, состоящих из щелочного металла и фосфора.
Реакции между щелочными металлами и фосфором могут происходить при различных условиях. Например, возможно образование фосфидов при нагревании щелочного металла с фосфором до высоких температур. Эти реакции могут происходить с выделением энергии и образованием ярких пламенных реакций. Кроме того, взаимодействие может происходить и в жидкой фазе, при погружении щелочного металла в раствор фосфора или его соединений.
Взаимодействие щелочных металлов с фосфором

Щелочные металлы, такие как литий, натрий, калий и др., проявляют активное взаимодействие с фосфором, химический элемент из группы Галогенов. Это взаимодействие можно описать реакцией, в результате которой образуются соединения щелочных металлов и фосфора.
Реакция взаимодействия щелочных металлов с фосфором протекает с выделением значительного количества тепла и обычно сопровождается плавкостью металла. Кроме того, при этой реакции может происходить выделение газа фосфина (PH3), который обладает неприятным запахом и может быть токсичным. Поэтому взаимодействие щелочных металлов с фосфором требует особого внимания и осторожности.
В результате взаимодействия, образуются соединения щелочных металлов и фосфора, такие как гидрофосфаты или фосфиды. Фосфиды щелочных металлов обладают высокими температурами плавления и являются проводниками электричества. Одно из применений фосфидов щелочных металлов - в производстве полупроводников и светоизлучающих диодов.
Дополнительно, щелочные металлы реагируют с фосфором при взаимодействии с водой, образуя оксокислородные и водородофосфатные соединения. В таких реакциях образующийся водородофосфат можно использовать в качестве удобрения, так как он содержит фосфор - один из необходимых элементов для роста растений.
Щелочные металлы и их химические свойства
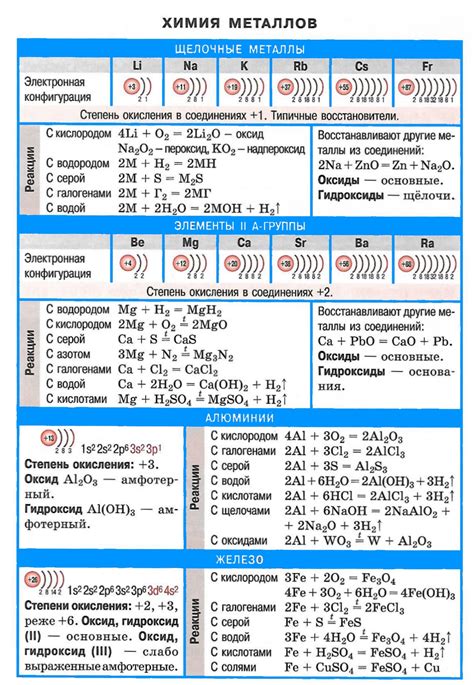
Щелочные металлы – это первая группа элементов в периодической таблице. Они включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Щелочные металлы обладают рядом характерных химических свойств.
- Одной из основных характеристик щелочных металлов является их низкая электроотрицательность. Это означает, что они склонны отдавать свои электроны и образовывать положительно заряженные ионы (катионы).
- Щелочные металлы очень реакционны и легко реагируют с другими веществами, включая кислород, воду и различные неорганические соединения.
- Одна из наиболее известных реакций щелочных металлов – реакция с водой. При контакте с водой они образуют гидроксиды щелочных металлов и высвобождаются водород.
- Щелочные металлы также реагируют с кислородом, образуя оксиды щелочных металлов. Эти реакции могут сопровождаться выделением тепла и света.
Из-за своей реактивности, щелочные металлы обычно хранят в инертной среде, такой как гексан или парафиновое масло. Они также широко используются в различных промышленных процессах и в производстве различных продуктов, включая мыла, стекло, лекарства и батарейки.
Фосфор и его способность к реакциям
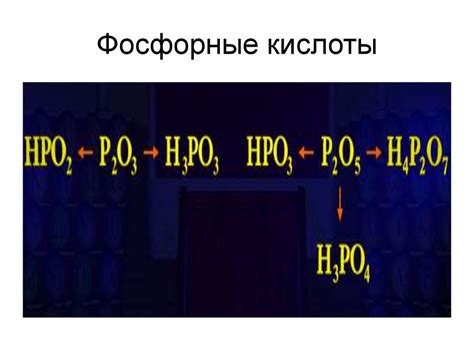
Фосфор – химический элемент, который проявляет высокую активность и способность к реакциям с различными веществами.
Вода и фосфор образуют фосфиды, которые плавают на поверхности воды и образуют газообразные вещества при контакте с кислородом. Фосфиды, такие как PH3 (фосфин) и P4O10 (фосфорный ангидрид), обладают различными свойствами и находят применение в различных областях.
Фосфор также реагирует с кислородом, образуя оксиды. Фосфор оксиды (P2O5, P4O7) обладают кислотными свойствами и применяются в производстве удобрений, стекла и жидкого фосфора.
Взаимодействие фосфора с щелочными металлами (например, натрием или калием) приводит к образованию фосфидов, которые могут быть использованы в различных химических реакциях. Некоторые фосфиды, такие как Na3P или KP2, обладают способностью к сохранению водорода и находят применение в производстве водородных топливных элементов.
Фосфор также может образовывать сплавы с металлами, такими как алюминий, магний или цинк. Это сплавы обладают различными физическими и химическими свойствами и могут использоваться в производстве сплавов и легированных материалов.
Таким образом, фосфор обладает высокой способностью к взаимодействию с другими веществами, что делает его важным элементом в химической промышленности и других областях науки и технологий.
Химические реакции при взаимодействии щелочных металлов с фосфором
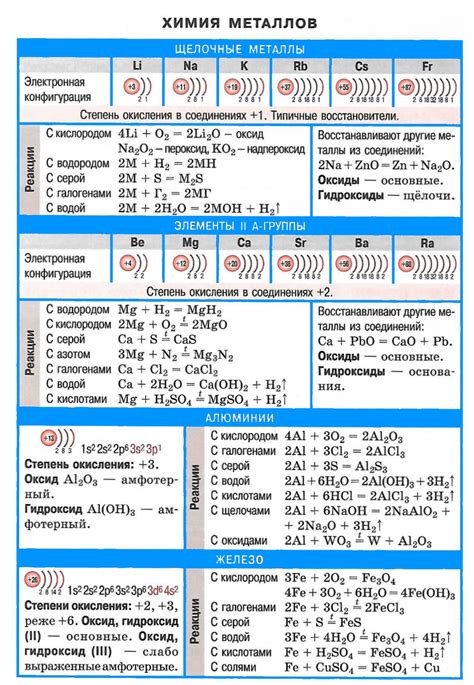
Взаимодействие щелочных металлов с фосфором является одной из важных реакций в неорганической химии. Она происходит при контакте металлов группы 1 с элементом группы 15 периодической таблицы.
При взаимодействии их происходит образование фосфидов. Фосфиды щелочных металлов обладают высокой активностью и могут применяться в различных областях, включая пиротехнику и катализаторы.
Например, при соединении натрия и фосфора образуется натриевый фосфид (Na3P), а при взаимодействии калия и фосфора образуется калиевый фосфид (KP).
Химическая реакция процесса взаимодействия щелочных металлов с фосфором может быть описана следующим образом: металл вступает в реакцию с фосфором, образуя фосфид, и освобождается огромное количество энергии в виде тепла и света.
Таким образом, взаимодействие щелочных металлов с фосфором является экзотермической реакцией, при которой происходит выделение энергии. Эта реакция имеет широкое практическое применение и играет важную роль в различных отраслях промышленности и науки.
Применение реакций щелочных металлов с фосфором в промышленности

Реакции щелочных металлов с фосфором имеют широкое применение в различных отраслях промышленности. Одной из важных областей, где применяются эти реакции, является производство удобрений.
Фосфор является основным компонентом многих удобрений и используется для улучшения питательных свойств почвы. Реакция щелочных металлов с фосфором позволяет получать фосфорные соединения, которые затем используются для производства удобрений.
Кроме того, реакции щелочных металлов с фосфором используются в химической промышленности для получения фосфора и фосфорных соединений. Фосфор является важным сырьем для производства различных продуктов, таких как фосфорные кислоты, сольфат калия и др. Эти продукты широко применяются в производстве удобрений, химической промышленности, металлургии и других отраслях промышленности.
Стоит отметить, что реакции щелочных металлов с фосфором также находят применение в производстве огнеупорных материалов. Использование таких реакций позволяет получать фосфиды щелочных металлов, которые характеризуются высокой стойкостью к высоким температурам. Огнеупорные материалы, получаемые из фосфидов щелочных металлов, используются в различных отраслях промышленности, включая металлургию, строительство, промышленное оборудование и др.
Употребление соединений щелочных металлов и фосфора в быту

Соединения щелочных металлов и фосфора имеют широкое применение в быту и промышленности. Они используются как компоненты в производстве моющих средств, дезинфицирующих средств и средств для очистки поверхностей. Фосфорные соединения эффективно удаляют загрязнения и жировые отложения, обеспечивая безупречную чистоту.
Один из наиболее распространенных примеров использования соединений щелочных металлов и фосфора в быту – это мыльные порошки и жидкости для стирки. Фосфаты натрия и калия, являющиеся соединениями щелочных металлов и фосфора, обеспечивают высокую эффективность удаления пятен и загрязнений с тканей. Они также предотвращают оседание минеральных отложений на ткани и улучшают качество стирки.
Кроме того, соединения щелочных металлов и фосфора широко применяются в производстве удобрений. Фосфатные удобрения содержат фосфор, который является необходимым элементом растений для нормального роста и развития. Фосфорные удобрения на основе щелочных металлов позволяют повысить урожайность и качество сельскохозяйственных культур.
В быту также активно используются соединения щелочных металлов и фосфора в составе домашних фитнес-тренажеров. Фосфатные стекла, содержащие натрий или калий, применяются для создания прозрачных дисплеев и датчиков веса. Эти соединения обладают высокой прочностью и устойчивостью к механическим повреждениям, что обеспечивает долговечность и надежность тренажеров.
Кратко резюмируя, соединения щелочных металлов и фосфора широко применяются в быту и промышленности. Их использование в моющих средствах, удобрениях и домашних тренажерах обеспечивает эффективность и качество результатов. Эти соединения играют важную роль в повседневной жизни, способствуя поддержанию чистоты, росту урожайности и созданию надежного оборудования.
Вопрос-ответ

Что такое щелочные металлы?
Щелочные металлы - это элементы, расположенные в первой группе периодической системы. Их химические свойства в значительной степени определяются наличием одной валентной электронной оболочки.
Какие есть особенности взаимодействия щелочных металлов с фосфором?
Особенности взаимодействия щелочных металлов с фосфором заключаются в образовании соединений, таких как фосфиды. Фосфиды щелочных металлов обладают высокой активностью и часто применяются в различных реакциях органического и неорганического синтеза.
Какие реакции могут происходить между щелочными металлами и фосфором?
Между щелочными металлами и фосфором могут происходить различные реакции, включая образование фосфидов на основе щелочных металлов, как, например, натрия и калия. Также возможна реакция гидрирования, при которой фосфор может добавляться к молекуле воды, образуя гидрофосфид соответствующего щелочного металла.
Какие свойства имеют фосфиды щелочных металлов?
Фосфиды щелочных металлов обладают высокой активностью и могут быть использованы в качестве катализаторов различных химических реакций. Они также обладают низкой температурой плавления, хорошей термической стабильностью и высокой реакционной способностью.
Какие практические применения имеют соединения фосфора с щелочными металлами?
Соединения фосфора с щелочными металлами имеют широкое практическое применение. Например, фосфиды щелочных металлов могут использоваться в качестве катализаторов в химической промышленности. Они также используются в производстве батарей, взрывчатых веществ, легировании металлов и других областях.
