Серная кислота является одним из наиболее распространенных и важных химических соединений. Она обладает высокой кислотностью и активностью, что позволяет ей реагировать с многими различными веществами, в том числе и с металлами.
Металлы представляют собой крупные группу химических элементов, среди которых могут быть как очень реакционные, так и менее активные. Реакция серной кислоты с металлами является важным примером химической реакции, которая позволяет нам изучить взаимодействие кислоты и металлов под воздействием различных условий.
Реакция между серной кислотой и металлами приводит к образованию соответствующих солей и выделению водорода. Это одна из реакций, в которой происходит окисление металла и восстановление серной кислоты. В зависимости от активности металла, реакция может протекать более или менее интенсивно.
Различная активность металлов влияет на скорость протекания реакции, а также на характер выделения водорода. Металлы высокой активности, такие как натрий или калий, реагируют с серной кислотой очень активно и быстро, сопровождаясь интенсивным выделением газа. Металлы низкой активности, такие как железо или цинк, реагируют с серной кислотой медленно, образуя менее интенсивно выделяющийся водород.
Активность металлов в химических реакциях серной кислоты
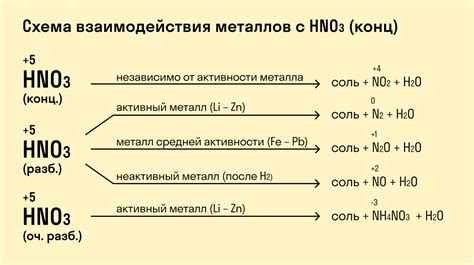
Химическая активность металлов определяется их способностью взаимодействовать с другими веществами, в том числе с кислотами. Серная кислота, или H2SO4, является одной из наиболее широко используемых кислот в химических процессах, и взаимодействие с ней может происходить с разной степенью интенсивности, в зависимости от активности металла.
В химии металлы делятся на активные и пассивные. Активные металлы, такие как натрий, калий, магний и алюминий, реагируют с серной кислотой достаточно интенсивно. При этом образуется сернистый газ (SO2) и соответствующие соли металлов. Это связано с высокой реакционной способностью активных металлов и их способностью образовывать соединения с высокой степенью окисления.
Пассивные металлы, к которым относятся, например, железо, медь и свинец, реагируют с серной кислотой гораздо медленнее и в более ограниченном объеме. Реакция может проходить только с разбавленной или нагретой серной кислотой. При этом образуются соли металлов и выделяется водород. Это связано с низкой реакционной способностью пассивных металлов и их способностью образовывать соединения с более низкой степенью окисления.
Таким образом, активность металлов в химических реакциях с серной кислотой определяется их реакционной способностью и способностью образовывать соединения разной степени окисления. Это свойство металлов может быть использовано для различных химических процессов, таких как синтез органических и неорганических соединений, очистка воды и другие промышленные процессы, где необходимо контролировать химические реакции соответствующих металлов с серной кислотой.
Реакция серной кислоты с активными металлами
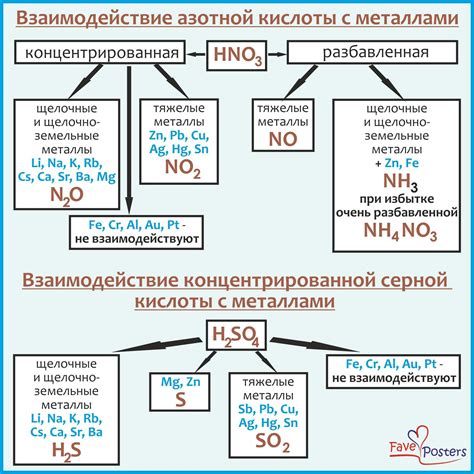
Серная кислота, или H2SO4, является одной из самых распространенных химических соединений. Она обладает сильными окислительными свойствами и может реагировать с различными веществами, включая активные металлы.
Активными металлами считаются металлы, которые легко отдают электроны и образуют ионы положительного заряда. К таким металлам относятся натрий, калий, магний и алюминий. При контакте с серной кислотой они реагируют, образуя соли и выделяя водородный газ.
Реакция между серной кислотой и активными металлами протекает с выделением тепла. Это происходит из-за экзотермической характеристики реакции, которая выражается в выделении энергии в виде тепла при образовании новых химических связей. Данная реакция может протекать с различной скоростью в зависимости от активности металла.
- Например, реакция серной кислоты с натрием (Na) происходит быстро и с выделением большого количества газа.
- Реакция с калием (K) также происходит очень быстро и с похожими характеристиками.
- Однако, реакция серной кислоты с магнием (Mg) протекает медленнее и с выделением меньшего количества газа.
- А реакция с алюминием (Al), в отличие от предыдущих, происходит очень медленно, требуя нагревания.
Таким образом, реакция серной кислоты с активными металлами может иметь различную скорость и характеристики в зависимости от металла, что объясняется их разной активностью и способностью отдавать электроны.
Реакция серной кислоты с полуактивными металлами
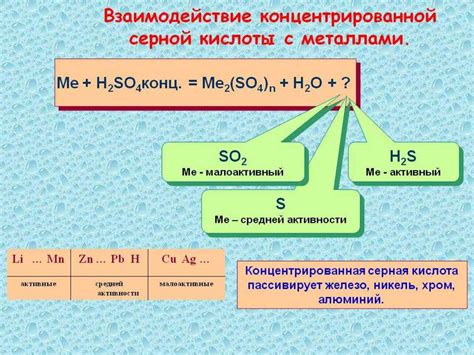
Серная кислота, известная также как сульфатная кислота, имеет широкое применение в различных отраслях химической промышленности. Одним из способов взаимодействия серной кислоты с различными веществами является реакция с металлами разной активности.
Полуактивные металлы, такие как железо, медь, цинк, никель и другие, могут реагировать с серной кислотой, образуя соединения и выделяяся водород. Однако реакция с полуактивными металлами происходит медленнее, чем с активными металлами, такими как натрий или калий.
Реакция серной кислоты с полуактивными металлами происходит по следующему механизму: сначала происходит реакция металла с серной кислотой, при которой образуется соответствующая соль и выделяется водород. Далее серная кислота может действовать как окислитель или восстановитель, в зависимости от условий.
Реакция между серной кислотой и полуактивными металлами может иметь различный характер в зависимости от концентрации кислоты, температуры и других факторов. Например, при высокой концентрации серной кислоты и высокой температуре может происходить разложение соединений и образование новых продуктов реакции.
Таким образом, реакция серной кислоты с полуактивными металлами является важным химическим процессом и находит применение в различных областях промышленности, таких как производство удобрений, очистка воды и других.
Реакция серной кислоты с малоактивными металлами
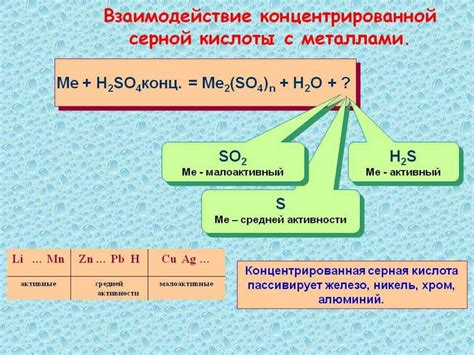
Серная кислота (H2SO4) является одним из наиболее распространенных и важных химических соединений. Она обладает сильно кислыми свойствами и активно реагирует с различными веществами, включая металлы.
Малоактивные металлы, такие как железо (Fe), цинк (Zn), алюминий (Al) и свинец (Pb), реагируют с серной кислотой, образуя соответствующие соли и выделяя водородный газ (H2). Это происходит из-за относительно низкой активности этих металлов, что позволяет им быть окисленными серной кислотой.
Реакция между серной кислотой и малоактивными металлами может быть описана следующим образом:
- Металл растворяется в серной кислоте, образуя соответствующую соль.
- В процессе реакции выделяется водородный газ.
- Образовавшихся продуктов реакции можно идентифицировать с помощью соответствующих химических тестов и методов анализа.
Реакция малоактивных металлов с серной кислотой является безопасной и широко используется в химической промышленности и лабораторных условиях для получения различных продуктов.
Вопрос-ответ

Как происходит химическая реакция серной кислоты с металлами?
Химическая реакция серной кислоты с металлами происходит с образованием соли серной кислоты и выделением водорода.
Каков результат взаимодействия серной кислоты с металлами разной активности?
Результат взаимодействия серной кислоты с металлами разной активности зависит от активности металла. Активные металлы, например, натрий или калий, реагируют со средним выделением водорода. Менее активные металлы, такие как железо или свинец, могут реагировать только при нагревании. Неактивные металлы, такие как медь или серебро, не реагируют с серной кислотой.
Каково применение реакции серной кислоты с металлами в промышленности?
Реакция серной кислоты с металлами имеет широкое применение в промышленности. Например, она используется для получения водорода, который затем может быть использован в различных химических процессах и производстве аммиака, водородной пероксида и других веществ. Кроме того, реакция серной кислоты с металлами может быть использована для очистки поверхностей металлов от окислов и других загрязнений.
