Металлы считаются одним из наиболее распространенных типов химических элементов, которые активно взаимодействуют с различными веществами. Они реагируют с кислотами, особенно сильными такими, как концентрированная серная кислота. Такие реакции могут протекать с образованием газов, солей или специфических остатков, и они имеют свои особенности и результаты.
Во время реакций металлов с концентрированной серной кислотой обычно происходит выделение газа. В зависимости от металла это может быть водород или диоксид серы. Например, алюминий реагирует с серной кислотой, и в результате получается соль алюминия и сероводородный газ:
2Al + 3H2SO4 = Al2(SO4)3 + 3H2S
Еще одним результатом этих реакций являются соли, получаемые в результате образования новых химических связей. Металлический ион обычно образует ионную связь с кислотным остатком, образуя ионные соединения. Например, при реакции цинка с серной кислотой образуется соль:
Zn + H2SO4 = ZnSO4 + H2
Эти реакции также имеют свои особенности в зависимости от концентрации кислоты и типа металла. Некоторые металлы, такие как железо или никель, могут образовывать ослаждающуюся пленку при взаимодействии с концентрированной серной кислотой. Это может остановить реакцию и защитить металл от дальнейшего воздействия кислоты.
Влияние концентрации серной кислоты на реакцию с металлами
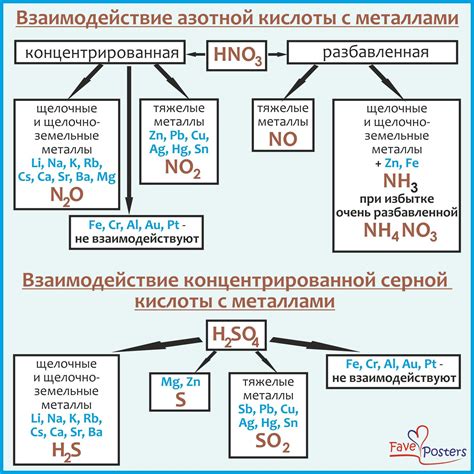
Концентрация серной кислоты является одним из важных факторов, влияющих на характер и скорость реакции с металлами. Главным образом, концентрация серной кислоты определяет агрессивность ее воздействия на металлические поверхности.
При повышении концентрации серной кислоты происходит усиление химической активности вещества и увеличение энергии активации реакции. Это приводит к более интенсивному растворению металла и ускорению реакции. Таким образом, при более высокой концентрации серной кислоты реакция с металлами протекает быстрее и более эффективно.
Однако при очень высоких концентрациях серной кислоты может образовываться пассивная пленка на поверхности металла, которая затрудняет дальнейшее происходящее взаимодействие. В этом случае реакция может замедлиться или даже прекратиться. Также повышенная концентрация серной кислоты может привести к коррозии металла или другим нежелательным побочным эффектам.
В целом, оптимальная концентрация серной кислоты для проведения реакции с металлами зависит от конкретных условий и требований эксперимента или процесса. Поэтому важно выбирать нужный уровень концентрации серной кислоты, чтобы достичь желаемого результата в исследованиях или промышленном производстве.
Различия в скорости реакции металлов с разной концентрацией серной кислоты

Реакции металлов с концентрированной серной кислотой проходят достаточно быстро и генерируют большое количество тепла. Однако, скорость реакции может быть варьирующейся в зависимости от концентрации серной кислоты.
Высокая концентрация серной кислоты обеспечивает достаточно большое количество ионов H+, что повышает активность и реакционную способность кислоты. Это приводит к более быстрой реакции металлов и более интенсивному выделению водорода.
С другой стороны, при низкой концентрации серной кислоты, количество ионов H+ снижается. Это ограничивает активность кислоты и замедляет реакцию металла с кислотой. Металл может быть полностью или частично "обматывен" оксидной пленкой, что затрудняет дальнейшее взаимодействие металла с кислотой и замедляет процесс испускания водорода.
Таким образом, концентрация серной кислоты является определяющим фактором для скорости реакции металлов. Высокая концентрация ускоряет реакцию, а низкая - замедляет ее. Это позволяет контролировать скорость реакции и эффективность действия серной кислоты на металлические поверхности.
Изменение свойств металлов после реакции с концентрированной серной кислотой
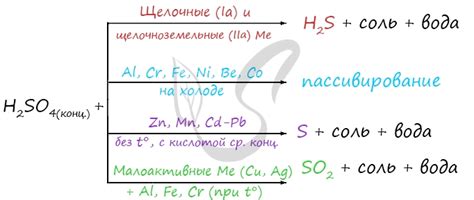
Реакция металлов с концентрированной серной кислотой является очень активной и вызывает значительные изменения свойств металлов. После взаимодействия с кислотой, металлы могут изменить свою цветовую окраску, текстуру и образование новых соединений.
Многие металлы, такие как железо, медь, цинк и олово способны реагировать с концентрированной серной кислотой. При контакте с кислотой, металлы могут испытать коррозию и образование газовых продуктов. Например, железо может образовывать серную соль и выделяться водородный газ.
Результаты реакции металлов с концентрированной серной кислотой зависят от свойств и химической активности каждого металла. Некоторые металлы, такие как золото и платина, не реагируют с кислотой и остаются нереактивными. В то же время, алюминий, магний и цинк могут быстро раствориться в кислоте, образуя соответствующие соли и выделяя водородный газ.
Реакция металлов с концентрированной серной кислотой может быть использована для различных химических исследований и применяется в промышленности для получения соединений металлов и производства газов. Это также позволяет определить химическую активность металлов и оценить их реакционную способность.
Образование сульфатов металлов и их свойства
В результате реакции металлов с концентрированной серной кислотой образуются сульфаты металлов. Сульфаты представляют собой соли серной кислоты, в которых серная кислота замещена металлом.
Сульфаты металлов обладают рядом свойств, которые делают их важными соединениями. Во-первых, сульфаты обычно образуют кристаллические соединения с хорошей растворимостью в воде. Это способствует их распространению и возможности использования в различных областях.
Во-вторых, сульфаты металлов обладают высокой устойчивостью к теплу и окислительным средам. Они не разлагаются при нормальных условиях и обычно не реагируют с другими веществами. Это делает их долговечными и стабильными в различных приложениях и процессах.
В-третьих, сульфаты металлов могут иметь различные степени окисления и, следовательно, различные физические и химические свойства. Некоторые сульфаты металлов используются в качестве катализаторов, а некоторые могут обладать электролитическими свойствами.
Сульфаты металлов также могут использоваться в производстве удобрений и в других промышленных процессах. Они широко используются в различных отраслях, включая сельское хозяйство, строительство, производство химических веществ и энергетику.
Изменение цвета металлов после реакции с серной кислотой

Реакция металлов с концентрированной серной кислотой - это процесс, при котором металлы окисляются и образуются соответствующие соли. Одним из ярких признаков этой реакции является изменение цвета металлов.
Окрашивание металлов во время реакции с серной кислотой может быть результатом образования оксидов или сульфатов металлов. Например, железо при контакте с серной кислотой может образовать железный(II) сульфат, который имеет зеленую окраску.
Реакция цинка с серной кислотой, в свою очередь, приводит к образованию цинкового сульфата, который обладает белой окраской. Кроме того, наблюдается выброс сероводорода, что сопровождается его характерным запахом.
Изменение цвета металлов после реакции с серной кислотой может быть использовано для их идентификации. Например, благодаря свойству образования зеленого оксида железа при реакции с серной кислотой, возможно определить наличие железа в исследуемом образце.
Таким образом, изменение цвета металлов после реакции с концентрированной серной кислотой может служить важным индикатором данных химических процессов и способом определения наличия конкретного металла в пробе.
Влияние температуры на реакцию металлов с концентрированной серной кислотой
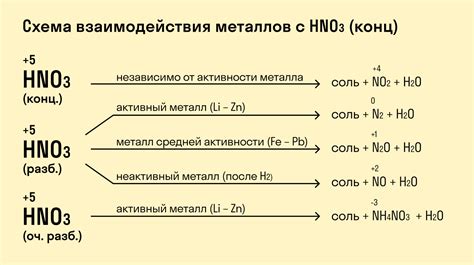
Реакция металлов с концентрированной серной кислотой происходит с выделением водорода и образованием сульфатов металлов. Однако, в зависимости от температуры, процесс может протекать с различной скоростью и давать различные результаты.
Увеличение температуры при взаимодействии металлов с концентрированной серной кислотой может ускорить реакцию и повысить выход продуктов. Это связано с тем, что при повышении температуры увеличивается энергия движения молекул, что способствует их более активным столкновениям и увеличению скорости реакции.
Однако высокая температура может также приводить к нежелательным побочным реакциям, например, окислению или восстановлению серной кислоты. Также возможно образование сульфатов с различной степенью окисления металлов.
Следует отметить, что для каждого металла оптимальная температура реакции может быть разной. Например, некоторые металлы могут быть более реакционными при низких температурах, в то время как другие металлы могут более эффективно реагировать при повышенных температурах.
Температура является важным параметром, который следует учитывать при исследовании реакций металлов с концентрированной серной кислотой и может влиять на скорость реакции и характер образующихся продуктов.
Изменение скорости реакции металлов при различной температуре серной кислоты

Реакция металлов с концентрированной серной кислотой является одним из наиболее распространенных методов получения серovodoroda (H2S) и соответствующих солей металлов с серой. Однако, важным аспектом этой реакции является ее скорость, которая может быть изменена в зависимости от температуры серной кислоты.
При повышении температуры концентрированной серной кислоты, скорость реакции с металлами увеличивается. Это объясняется тем, что при повышенной температуре молекулы кислоты обладают большей энергией и движутся более быстро, что способствует частичным ударам и столкновениям с поверхностью металла.
Однако, при очень высоких температурах концентрированной серной кислоты наблюдаются обратные результаты. Высокая температура может привести к образованию сложных соединений, которые могут замедлить реакцию или даже полностью прекратить ее протекание.
Для оптимальной скорости реакции металлов с концентрированной серной кислотой рекомендуется поддерживать определенную температуру, которая может быть определена экспериментально или расчетными методами. Также следует учитывать, что каждый металл может иметь свою оптимальную температуру для данной реакции, поэтому проведение предварительных испытаний с разными температурами является необходимым.
Изменение скорости реакции металлов с концентрированной серной кислотой при различной температуре играет важную роль в промышленных процессах и лабораторных исследованиях, так как позволяет контролировать и оптимизировать процесс образования сероводорода и соединений металлов с серой.
Вопрос-ответ

Какие металлы реагируют с концентрированной серной кислотой?
С концентрированной серной кислотой реагируют активные металлы, такие как натрий (Na), калий (K), магний (Mg) и алюминий (Al).
Что происходит при реакции металлов с концентрированной серной кислотой?
При реакции металлов с концентрированной серной кислотой образуется соответствующая соль металла и сероводород (H2).
Какие особенности можно выделить при реакции металлов с концентрированной серной кислотой?
Одной из особенностей такой реакции является образование газа сероводорода (H2), который может проявиться в виде шипения или отдачи газа. Также, реакция сопровождается выделением тепла.
Какой результат можно получить при реакции металлов с концентрированной серной кислотой?
Результат реакции металлов с концентрированной серной кислотой - образование соли металла и выделение газа сероводорода (H2).
