Оксиды металлов – это химические соединения, состоящие из металлического и кислородного атомов. Они обладают различными свойствами и активно взаимодействуют с окружающей средой. Одной из наиболее важных реакций оксидов металлов является их взаимодействие с углеродом.
Реакции оксидов металлов с углеродом проходят при высоких температурах и обычно сопровождаются выделением тепла и образованием новых соединений. Полученные в результате реакции оксидоуглероды металлов – это важные продукты, которые широко используются в различных отраслях промышленности.
Одним из примеров реакции оксидов металлов с углеродом является восстановительная пиролизная реакция, при которой происходит превращение оксидов металлов в соответствующие металлы и выделение диоксида углерода. Эта реакция найти применение в металлургической промышленности, а также в процессах получения металлических порошков и композитных материалов.
Важно отметить, что реакции оксидов металлов с углеродом могут происходить при различных условиях и иметь различный характер. Например, восстановление оксидов металлов углеродом достаточно сложный процесс, который требует контроля температуры, давления и концентрации реагентов. Правильное подбор условий позволяет оптимизировать химическую реакцию и повысить выход целевого продукта.
Взаимодействие оксидов металлов с углеродом: механизм и условия
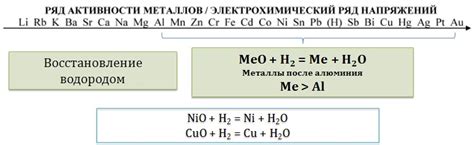
Оксиды металлов могут образовывать различные соединения с углеродом, что обусловлено их химическими свойствами и способностью образовывать ковалентные связи. Механизм взаимодействия оксидов металлов с углеродом зависит от конкретного оксида и условий процесса.
Один из механизмов взаимодействия оксидов металлов с углеродом - реакция восстановления, при которой металл из оксида переходит в ионное состояние, а углероду передается электрон. Этот механизм наблюдается, например, при взаимодействии оксида железа с углеродом, в результате чего образуется железо и диоксид углерода.
Другим механизмом взаимодействия является образование комплексных соединений между оксидами металлов и углеродом. Например, оксид молибдена может образовывать соединения с графеном - одним из разновидностей углерода. Полученные комплексы могут иметь интересные свойства, такие как прозрачность и проводимость.
Условия взаимодействия оксидов металлов с углеродом также играют важную роль. Например, для реакции восстановления важна температура, давление и наличие катализаторов. Также влияет степень окисления металла и структура углерода.
Взаимодействие оксидов металлов с углеродом имеет широкое применение в различных областях, начиная от производства материалов до энергетики. Например, это может быть использовано для синтеза новых материалов с улучшенными свойствами или для создания эффективных катализаторов.
Формирование различных типов соединений при реакции оксидов металлов с углеродом
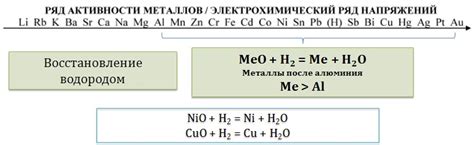
Реакции оксидов металлов с углеродом являются важным аспектом химических процессов, которые могут привести к образованию различных типов соединений. Одним из результатов таких реакций является образование карбоната металла.
Карбонаты металлов – это соединения, в которых катион металла связан с анионом карбоната. Они часто представляют собой твердые вещества с определенными физическими и химическими свойствами. Карбонаты металлов широко используются в различных отраслях промышленности и науки.
При реакции оксидов металлов с углеродом также может образоваться карбид металла. Карбиды – это соединения, в которых металл связан с углеродом. Они обладают специфическими физическими и химическими свойствами.
Формирование карбонатов и карбидов металлов при реакции оксидов с углеродом обусловлено химической реакцией между активным металлом и газообразным углеродом. Оксид металла служит катализатором этой реакции, облегчая процесс образования новых соединений.
Помимо карбонатов и карбидов, реакция оксидов металлов с углеродом может привести к образованию других типов соединений, таких как аллотропы углерода. Например, при реакции окиси железа с углеродом может образоваться графит или алмаз, в зависимости от условий реакции.
Таким образом, реакции оксидов металлов с углеродом являются сложными и многосторонними процессами, которые могут приводить к образованию различных типов соединений, имеющих важное практическое применение.
Применение реакций оксидов металлов с углеродом в промышленности

Реакции оксидов металлов с углеродом имеют широкое применение в промышленности и используются в различных процессах производства. Благодаря этим реакциям можно получить ценные продукты и материалы.
Одним из основных применений реакций оксидов металлов с углеродом является получение металлов. Например, реакция оксида железа с углеродом приводит к образованию чистого железа, которое широко используется в металлургии и строительной отрасли.
Также эти реакции применяются в процессе получения карбидов. Реакция оксида кальция с углеродом позволяет получить карбид кальция, который широко используется в производстве ацетилена, аммиачной селитры, а также в синтезе органических соединений.
Реакции оксидов металлов с углеродом также используются для получения кокса, который является важным сырьем для производства чугуна и стали. Реакция оксида кремния с углеродом приводит к образованию карбида кремния, который является основным компонентом электрокорунда и используется в производстве отливок и абразивов.
Кроме того, реакции оксидов металлов с углеродом могут применяться для удаления загрязнений. Например, реакция оксида серы с углеродом позволяет удалить серу из нефти, а реакция оксида азота с углеродом используется для удаления окислов азота из выбросов.
Таким образом, применение реакций оксидов металлов с углеродом в промышленности позволяет получить различные ценные продукты и материалы, а также проводить очистку от загрязнений. Эти реакции играют важную роль в различных отраслях производства и способствуют развитию промышленности.
Влияние окислительно-восстановительных свойств оксидов металлов на реакции с углеродом

Оксиды металлов являются важными химическими соединениями, которые активно взаимодействуют с углеродом. При этом, их окислительно-восстановительные свойства играют существенную роль в ходе реакций. Углерод может находиться в различных формах, например, в виде графита, алмаза или углеродных соединений.
Оксиды металлов, такие как оксид железа Fe2O3, оксид меди CuO или оксид цинка ZnO, могут быть использованы в качестве катализаторов в различных процессах, связанных с углеродом. Они могут принимать активное участие в окислительно-восстановительных реакциях, способствуя образованию новых соединений.
Например, оксид железа Fe2O3 может служить катализатором в реакции окисления углерода. В этой реакции, металлический железо окисляется до Fe2O3, а углерод редуцируется до диоксида углерода CO2. Таким образом, оксид железа играет роль окислителя в данной реакции.
Взаимодействие оксидов металлов с углеродом может иметь место и в обратном направлении. Например, оксид цинка ZnO может восстанавливаться углеродом с образованием металлического цинка и оксида углерода. Эта реакция может протекать при достаточно высоких температурах и может быть использована для получения металлов из оксидов.
Таким образом, окислительно-восстановительные свойства оксидов металлов играют важную роль в реакциях с углеродом. Они определяют направление и скорость реакции, а также могут быть использованы для получения новых соединений и металлов.
Реакции оксидов металлов с углеродом в природе: роль в геологических процессах
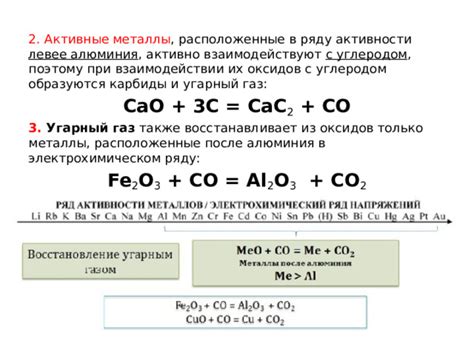
Реакции оксидов металлов с углеродом играют важную роль в геологических процессах и являются неотъемлемой частью естественного круговорота веществ в природе. Эти реакции происходят в различных окружающих условиях и влияют на формирование и изменение горных пород, минералов и природных ресурсов.
Оксиды металлов, такие как оксид железа (Fe2O3) и оксид алюминия (Al2O3), взаимодействуют с углеродом в присутствии высоких температур при геологических процессах, таких как магматическое образование и горение углеводородов. Результатом таких реакций являются процессы образования различных минералов, таких как железная руда и алюмосиликатные минералы.
Реакции оксидов металлов с углеродом также влияют на структуру и свойства горных пород. Например, взаимодействие оксидов металлов с угольными отложениями может привести к образованию сланцев и антрацита, которые имеют высокую углеродную содержательность и используются в промышленности в качестве топлива и сырья.
Более того, реакции оксидов металлов с углеродом способствуют процессам переработки природных ресурсов, таким как железная руда. При снижении оксида железа с помощью углерода получают чистый металл железо, который затем используется в производстве металлургической и строительной промышленности.
Таким образом, реакции оксидов металлов с углеродом являются важными геологическими процессами, которые влияют на формирование и преобразование горных пород и природных ресурсов. Понимание этих реакций помогает не только расширить наши знания о геологических процессах, но и найти практическое применение в различных отраслях промышленности и экологии.
Вопрос-ответ

Какие оксиды металлов могут реагировать с углеродом?
Реагировать с углеродом могут различные оксиды металлов, такие как оксид железа (Fe3O4), оксид алюминия (Al2O3), оксид меди (CuO) и другие. В зависимости от типа оксида и условий реакции, образующиеся соединения и их свойства могут существенно различаться.
Какие свойства образующихся соединений при реакции оксидов металлов с углеродом?
При реакции оксидов металлов с углеродом образуются соединения такие как металлические карбиды. Например, при взаимодействии оксида железа с углеродом образуется карбид железа (Fe3C), который обладает высокой твердостью и прочностью. Карбиды могут использоваться в металлургии для получения легированных сталей с улучшенными механическими свойствами.
