Оксиды металлов являются неорганическими соединениями, содержащими кислород в одной из своих степеней окисления. Их химические свойства и реакционная способность могут существенно отличаться в зависимости от степени окисления металла и его электрохимической активности. Одной из наиболее распространенных реакций оксидов металлов является их взаимодействие с серной кислотой.
Серная кислота (H2SO4) является одним из наиболее широко используемых химических веществ, применяемых в промышленности, лабораторных исследованиях и других областях. Ее реакция с оксидами металлов может приводить к образованию солей металлов и выделению воды. Данная реакция имеет важное практическое значение и находит применение в различных сферах, включая производство удобрений, горнодобывающую промышленность, производство кислот и др.
Процесс взаимодействия оксидов металлов с серной кислотой подчиняется основным законам химии и может происходить с различной интенсивностью в зависимости от электрохимических свойств металлов и условий проведения реакции. Кроме того, в реакции могут участвовать не только оксиды металлов, но и другие соединения, например, соли металлов или гидроксиды.
В данной статье рассмотрены особенности реакций оксидов металлов с серной кислотой, а также применение этих реакций в различных отраслях науки и техники. Особое внимание уделено анализу кинетических аспектов данных процессов, а также факторам, влияющим на их скорость и направление. Изучение данных реакций позволяет расширить наши знания о свойствах оксидов металлов, а также применять их в различных технологических процессах с целью получения определенных продуктов и материалов.
Оксиды металлов: основные характеристики
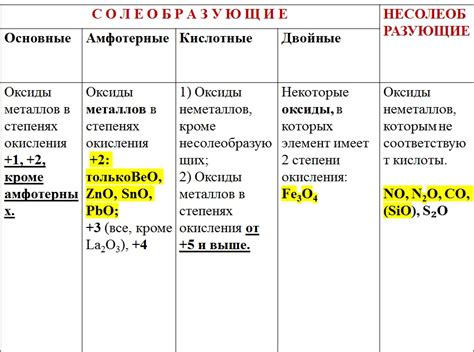
Оксиды металлов являются соединениями металлов с кислородом. Они обладают широким спектром физических и химических свойств, что делает их важными для различных областей науки и промышленности.
Физические свойства оксидов металлов зависят от конкретного металла и его окисления. Некоторые оксиды металлов обладают жидким состоянием при комнатной температуре, например оксид железа (II). Другие оксиды являются твердыми веществами с различными степенями твердости и плотности.
Химические свойства оксидов металлов могут быть различными и зависят от структуры соединения. Они могут проявлять кислотные или щелочные свойства, соответственно образуя соли или основания при реакции с кислотами или щелочами. Некоторые оксиды могут проявлять амфотерные свойства, способность проявлять как кислотные, так и щелочные свойства.
Применение оксидов металлов может быть разнообразным и расширяться от промышленного использования до медицины и электроники. Некоторые оксиды металлов применяются в качестве катализаторов в различных процессах, например оксид железа используется при производстве аммиака. Оксиды металлов также используются для создания красителей, электронных компонентов и в других отраслях промышленности.
Важно отметить, что свойства и применение оксидов металлов могут быть различными и зависят от конкретного соединения. Изучение данных соединений и их реакций с различными веществами является важной задачей для многих научных и промышленных областей, что позволяет расширять наши знания и применение оксидов металлов в различных сферах жизни.
Оксиды металлов - важные соединения

Оксиды металлов являются одними из наиболее распространенных и важных соединений в химии. Они представляют собой химические соединения, состоящие из металлических и кислородных атомов. В природе оксиды металлов встречаются в виде руд или минералов.
Большинство оксидов металлов обладает высокой химической стабильностью и инертностью, что делает их полезными в различных промышленных и научных областях.
Основные свойства оксидов металлов определяются их структурой и химическим составом. Некоторые оксиды металлов являются ионными соединениями, в которых металлический и кислородный атомы образуют ионы различных зарядов. Другие оксиды металлов могут быть ковалентными соединениями, в которых металлический и кислородный атомы образуют ковалентные связи.
Оксиды металлов обладают разными физическими и химическими свойствами, которые позволяют использовать их в различных областях. Например, некоторые оксиды металлов используются в качестве катализаторов в химической промышленности, другие - в производстве стекла и электроники. Оксиды металлов также широко применяются в качестве пигментов для окрашивания красок и керамики.
Оксиды металлов в химических реакциях

Оксиды металлов – это соединения, в состав которых входит металл и кислород. Они обладают различными химическими свойствами и широко используются в различных процессах. Реакции оксидов металлов с другими веществами имеют большую важность как в промышленности, так и в научных исследованиях.
Оксиды металлов с серной кислотой – одна из наиболее распространенных и важных химических реакций. При контакте оксида с серной кислотой происходит образование соли и воды. Эта реакция часто используется для получения различных соединений металлов, а также для очистки газов от примесей.
В зависимости от свойств металла, реакция оксида металла с серной кислотой может проходить с различной интенсивностью. Некоторые металлы действуют как катализаторы, ускоряя реакцию, другие металлы сами оказывают влияние на ход реакции. Например, медный оксид активирует серную кислоту, что ускоряет диссоциацию ее молекул и увеличивает скорость реакции.
Важным аспектом реакций оксидов металлов с серной кислотой является их применение в промышленности. С помощью реакции оксида с серной кислотой можно получать различные соединения металлов, которые затем используются в производстве различных материалов и изделий. Например, оксид кремния с серной кислотой позволяет получать кремниевую кислоту, которая широко применяется в электронной промышленности.
Взаимодействие оксидов металлов с серной кислотой
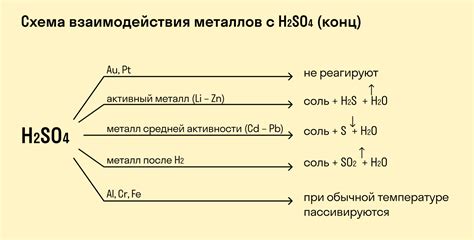
Взаимодействие оксидов металлов с серной кислотой представляет собой химическую реакцию, при которой образуется соответствующая соль металла и вода. Эта реакция является одной из наиболее распространенных и важных в химии.
Оксиды металлов – это химические соединения, состоящие из металла и кислорода. Они обычно имеют сильно щелочной характер и способны быстро реагировать с кислотами. Серная кислота (H2SO4) является одной из самых сильных кислот и широко используется в промышленности и в лабораториях.
При взаимодействии оксидов металлов с серной кислотой происходит следующая реакция: металлический оксид реагирует с серной кислотой, образуя соответствующую соль и воду. Например, реакция между оксидом кальция (CaO) и серной кислотой может быть записана следующим образом: CaO + H2SO4 → CaSO4 + H2O.
Взаимодействие оксидов металлов с серной кислотой широко используется в промышленности для получения солей металлов, которые имеют важное применение в различных отраслях. Например, сульфаты металлов используются в производстве удобрений, фармацевтике, стекольной промышленности и других сферах. Также взаимодействие оксидов металлов с серной кислотой часто используется в лабораторной практике для получения и изучения соответствующих соединений.
Реакционные свойства оксидов металлов и серной кислоты
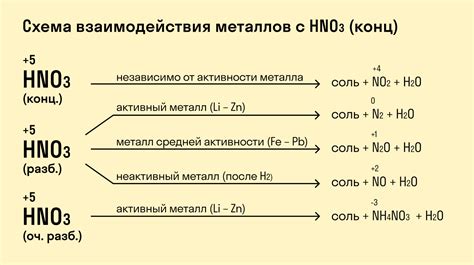
Оксиды металлов обладают уникальными реакционными свойствами при взаимодействии с серной кислотой. Эта реакция является классическим примером образования соли и воды.
При добавлении оксида металла в серную кислоту происходит сильное разложение кислоты и образование сложной структуры соли, содержащей металл и серу. Возникающие при этом осадки могут быть различными по своему цвету и физическим свойствам, что зависит от типа металла и его оксида.
Один из практических примеров использования реакции оксидов металлов с серной кислотой – это получение сульфатов металлов. Сульфаты металлов играют важную роль в различных отраслях промышленности, таких как химическое производство, сельское хозяйство и медицина.
Кроме того, реакции оксидов металлов с серной кислотой способны проявлять окислительные свойства. Например, в реакции с серной кислотой оксид меди CuO переходит в CuSO4, а серная кислота, теряя электроны, превращается в сернистую кислоту H2SO3.
Таким образом, реакции оксидов металлов и серной кислоты являются важным объектом изучения химии и имеют широкий спектр применений в различных сферах науки и промышленности.
Факторы, влияющие на скорость реакции

Скорость реакции оксидов металлов с серной кислотой зависит от нескольких факторов. Один из главных факторов - концентрация реагентов. Чем выше концентрация оксида и серной кислоты, тем быстрее протекает реакция. Это связано с тем, что большая концентрация реагентов приводит к более частым столкновениям между молекулами и ионами, что увеличивает вероятность образования новых веществ.
Температура также оказывает значительное влияние на скорость реакции. При повышении температуры молекулы и ионы становятся более подвижными и активными, что способствует увеличению скорости реакции. Это объясняется увеличением средней кинетической энергии молекул и ионов, что позволяет им преодолевать энергетический барьер и взаимодействовать быстрее.
Каталитические вещества также могут влиять на скорость реакции оксидов металлов с серной кислотой. Каталитические вещества ускоряют реакцию, но при этом не участвуют в ней самостоятельно. Они изменяют механизм реакции или активируют определенные стадии, что позволяет снизить энергетический барьер и ускорить процесс образования новых веществ.
Размер частиц реагентов также играет роль в скорости реакции. Более мелкие частицы обладают большей поверхностной площадью, что способствует более интенсивному взаимодействию между реагентами. Это увеличивает вероятность столкновений и повышает скорость образования новых веществ.
Применение реакции оксидов металлов с серной кислотой
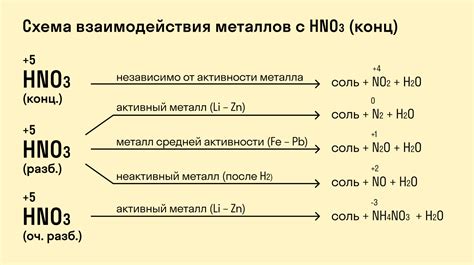
Реакция оксидов металлов с серной кислотой широко применяется в различных областях науки и промышленности.
Одним из основных применений этой реакции является получение сульфатов металлов. Сульфаты металлов широко используются в химической промышленности, в производстве удобрений, в качестве катализаторов реакций и в других отраслях. Реакция оксидов металлов с серной кислотой позволяет получить сульфаты различных металлов, включая алюминий, железо, медь, цинк и другие.
Также реакция оксидов металлов с серной кислотой используется в аналитической химии для определения содержания металлов в образцах. Путем реакции оксида металла с серной кислотой можно провести качественное и количественное определение металла, основываясь на изменении цвета или образовании осадка.
Еще одним применением реакции оксидов металлов с серной кислотой является исследование взаимодействия металлов с кислородом. Реакция оксида металла с серной кислотой позволяет изучить процессы окисления и восстановления металлов, а также степень их активности.
Таким образом, реакция оксидов металлов с серной кислотой имеет широкое применение в различных областях науки и промышленности, играя важную роль в получении сульфатов металлов, аналитической химии и изучении реакций окисления и восстановления металлов.
Конклюзия

В результате проведенного исследования становится очевидным, что оксиды металлов реагируют с серной кислотой, образуя соли и воду. Эта реакция является классическим примером нейтрализации и часто используется в химической промышленности.
Особенности реакции зависят от свойств конкретного оксида металла и его степени окисления. Некоторые оксиды металлов растворяются в серной кислоте без образования дополнительных продуктов, в то время как другие могут образовывать сложные соединения с серной кислотой.
Применение реакции оксидов металлов с серной кислотой широко разнообразно. Например, она может быть использована для получения солей, которые могут применяться в качестве удобрений или добавок в пищевую промышленность. Также эта реакция может быть использована для очистки воды от примесей металлов или для получения важных химических соединений.
Таким образом, реакции оксидов металлов с серной кислотой имеют широкое применение в различных областях науки и промышленности. Изучение и понимание особенностей этих реакций помогает улучшить процессы синтеза веществ и расширить спектр их применения.
Вопрос-ответ

Какие оксиды металлов могут реагировать с серной кислотой?
Серная кислота может реагировать с оксидами многих металлов, включая медь, железо, свинец, цинк и другие. Некоторые металлы образуют сильные растворы, а другие - слабые.
Каков механизм реакции между оксидами металлов и серной кислотой?
Механизм реакции зависит от типа оксида металла. Для металлов, которые образуют сильные растворы, реакция проходит следующим образом: оксид металла реагирует с водой на поверхности, образуя гидроксид металла, который затем распадается на ионы металла и ионы гидроксида. Ионы гидроксида реагируют с ионами серной кислоты, образуя соль и воду. Для металлов, которые образуют слабые растворы, реакция происходит через образование ионов металла и ионов серной кислоты, которые затем реагируют, образуя соль и воду.
