Изучение качественных реакций на металлы играет важную роль в химии. Качественные реакции позволяют определить наличие или отсутствие определенного металла в веществе. При проведении таких реакций используются специальные реагенты, которые образуют с металлами особые соединения.
Существует несколько методов для проведения качественных реакций на металлы. Один из самых распространенных методов - это метод замещения. В этом методе металл замещается в реагенте, образуя новое соединение. Также используется метод осаждения, при котором металл образует осадок в растворе после взаимодействия с определенным реагентом.
Результаты качественных реакций на металлы могут предоставить полезную информацию о составе вещества. Например, они могут указать наличие или отсутствие определенного металла в пробе. Также результаты реакций могут помочь определить степень чистоты металла или его примеси.
Качественные реакции на металлы широко используются в различных областях химии, включая аналитическую, неорганическую и органическую химию. Эти реакции помогают исследователям получать важные данные и делать выводы о свойствах металлов, их реакционной способности и взаимодействии с другими веществами.
Реакции на металлы в химии
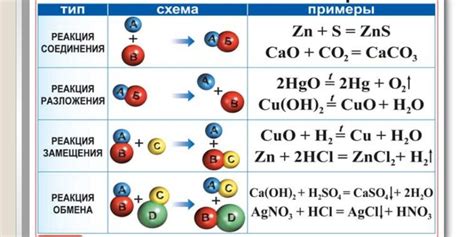
Реакции на металлы в химии являются одним из основных объектов изучения. Металлы, в силу своих химических и физических свойств, способны проявлять различные реакции при взаимодействии с другими веществами.
Одной из самых известных реакций на металлы является их окисление. Металлы могут окисляться воздухом при образовании оксидов, например, железо окисляется воздухом и образует ржавчину. Эта реакция является необратимой и происходит под влиянием кислорода.
Металлы также могут реагировать с кислотами, образуя соли и выделяя водород. Например, реакция цинка с соляной кислотой приводит к образованию соли цинка и выделению водорода. Эта реакция происходит под влиянием активности металла и кислоты.
Кроме того, металлы могут реагировать с основаниями, образуя соли и выделяя воду. Например, реакция алюминия с гидроксидом натрия приводит к образованию соли алюминия и выделению воды. Эта реакция происходит под влиянием активности металла и основания.
Некоторые металлы также могут реагировать с веществами, которые содержат кислород, образуя оксиды. Например, реакция магния с кислородом приводит к образованию оксида магния. Эта реакция является термически нейтральной и происходит при высоких температурах.
Все эти реакции на металлы в химии являются важными для изучения химических свойств металлов и их применения в различных областях науки и техники.
Классификация реакций на металлы

1. Реакция с кислотами: Металлы могут реагировать с кислотами, образуя соли и выделяя водород. Такие реакции происходят между активными металлами (например, натрием или калием) и различными кислотами. Результатом таких реакций может быть образование пузырьков газа и изменение цвета смеси.
2. Реакция с водой: Некоторые металлы способны взаимодействовать с водой, образуя гидроксиды и выделяя водород. Это явление называется реакцией с водой или гидролизом. Реакция может быть очень интенсивной, с выделением большого количества водорода и возгоранием металла, как в случае с натрием. В других случаях реакция протекает медленно и наблюдается образование слабой щелочи.
3. Реакция с кислородом: Металлы могут образовывать оксиды в результате взаимодействия с кислородом. Это реакция окисления, при которой металл теряет электроны. Окисление металла может протекать очень активно, например, при горении магния, или быть медленным, как при образовании корки на поверхности железа.
4. Реакция с карбонатами: Некоторые металлы могут реагировать с карбонатами, образуя соли, углекислый газ и воду. Такие реакции происходят с активными металлами, например, натрием или калием, и карбонатами, такими как карбонат кальция или натрия. Результатом реакции может быть образование пены и выделение газа.
5. Реакция с солями: Металлы могут взаимодействовать с солями, образуя более активные металлы или соли. Например, реакция меди с серной кислотой приводит к образованию сульфата меди и выделению диоксида серы. Результатом таких реакций может быть изменение цвета раствора и образование осадка.
Методы исследования реакций на металлы
1. Реакция с кислородом: Одним из основных методов исследования реакций на металлы является изучение их взаимодействия с кислородом. При взаимодействии многих металлов с кислородом происходит окисление металла, что приводит к образованию оксидов металлов. Такие реакции позволяют оценить активность металла и его способность образовывать соединения.
2. Реакция с кислотой: Другой метод исследования реакций на металлы – это изучение их взаимодействия с кислотами. При контакте с кислотой многие металлы могут реагировать с выделением водорода и образованием солей. Такие реакции помогают определить активность металла и его способность образовывать ионы металла в растворе.
3. Реакция с водой: Следующий метод исследования реакций на металлы – это их взаимодействие с водой. Некоторые металлы могут вступать в реакцию с водой, при этом образуется гидроксид металла и выделяется водород. Обратно, некоторые металлы не реагируют с водой, что позволяет оценить их активность и амфотерность.
4. Реакция с солями: Еще один метод исследования реакций на металлы – это их взаимодействие с солями. Многие металлы могут образовывать сложные соединения с солями, что позволяет определить их активность и способность образовывать комплексные соединения. Также, реакции с солями могут использоваться для определения металла в неизвестных образцах.
5. Реакция с щелочью: Еще один способ исследования реакций на металлы – это изучение их взаимодействия с щелочью. Некоторые металлы могут реагировать с щелочью, образуя гидроксид металла и выделяя водород. Такие реакции позволяют оценить активность металла и его способность взаимодействовать с основаниями.
Экспериментальные результаты реакций на металлы
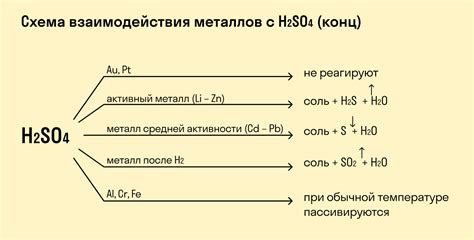
Взаимодействие металлов с кислотами:
Проведенные эксперименты показали, что активные металлы, такие как натрий, калий и магний, реагируют с кислотами с образованием солей и выделением водорода. Например, при взаимодействии натрия с соляной кислотой образуется хлорид натрия и выделяется водородный газ. Реакция протекает с высокой интенсивностью и сопровождается характерным треском.
Реакция металлов с щелочами:
Металлы основной группы (например, алюминий, цинк и магний) взаимодействуют с растворами щелочей, таких как гидроксид натрия или гидроксид калия. В результате образуются гидроксиды металлов и выделяется водородный газ. Например, реакция алюминия с гидроксидом натрия приводит к образованию гидроксида алюминия и выделению водорода.
Реакция металлов с оксидами:
Многие металлы реагируют с оксидами, образуя соли. Например, цинк реагирует с оксидом меди(II) с образованием хлорида цинка и меди. Реакция происходит при нагревании и имеет характерный цветовой эффект – медь образует красную корку на поверхности цинка. Экспериментальные исследования показали, что реакция металлов с оксидами зависит от их активности и электрохимического потенциала.
Реакция металлов с кислородом:
Многие металлы реагируют с кислородом при нагревании или взаимодействии с водой, образуя оксиды металлов. Например, железо при взаимодействии с кислородом образует оксид железа, а магний – оксид магния. Результаты экспериментов подтверждают, что реакция металлов с кислородом является химической окислительно-восстановительной реакцией.
Выводы:
Экспериментальные результаты реакций на металлы позволяют сделать выводы о способности металлов вступать в химические реакции с различными веществами. Реактивность металлов зависит от их активности и электрохимического потенциала. Различные факторы, такие как кислотность среды и наличие кислорода, влияют на характер реакции и образуемых продуктов.
Влияние физических условий на реакцию металла
Температура является одним из важных физических условий, которые оказывают влияние на реакцию металлов. Повышение температуры может способствовать ускорению химической реакции металла с другим веществом. Это связано с увеличением скорости движения молекул, что облегчает столкновение и взаимодействие металла с реагентом. Однако при слишком высоких температурах некоторые металлы могут начать испаряться или распадаться, что может привести к изменению химической реакции.
Давление также может оказывать влияние на реакцию металла. Увеличение давления может способствовать увеличению контакта между металлом и реагентом, что увеличивает вероятность химической реакции. Однако слишком высокое давление может также вызвать деформацию и разрушение металла, что может привести к изменению его химических свойств и реакционной способности.
Освещение также может оказывать влияние на реакцию металла. Некоторые металлы могут быть чувствительны к свету и изменять свою реакционную способность под его воздействием. Например, некоторые металлы могут испускать электроны под воздействием света (фотоэлектрический эффект), что может изменить их реакционную способность. Однако это свойство не присуще всем металлам и зависит от их электронной структуры и химических свойств.
Растворитель также может влиять на реакцию металла. Некоторые металлы могут растворяться в определенных растворителях и образовывать соединения с другими веществами. Присутствие растворителя может способствовать процессам химического взаимодействия и изменить химический характер реакции металла. Однако некоторые металлы могут быть инертны к растворителям и не подвержены реакциям в данной среде.
Особенности химических реакций металлов

Химические реакции металлов отличаются своими особенностями, включающими в себя химические свойства и реакционную способность металлов. Металлы обладают высокой электропроводностью и теплопроводностью, а также способностью образовывать положительные ионы, проявлять металлический блеск и иметь характерное пластичное свойство.
Взаимодействие металлов с другими веществами может происходить в различных формах. Например, реакция металла с кислотой может привести к выделению газа и образованию соли, что является типичной реакцией активных металлов. У некоторых металлов может наблюдаться реакция с кислородом, при которой образуется оксид металла.
Реакция металла с водой также способна проявляться по-разному. Некоторые металлы, такие как натрий и калий, реагируют с водой активно, образуя оксид металла и выделяя водород. Другие металлы, такие как медь и железо, не обладают такой высокой реакционной способностью и не реагируют с водой при комнатной температуре.
Важно отметить, что реакции металлов также могут происходить с неорганическими соединениями, например, солью или кислотой. В таком случае могут образовываться осадки, обладающие специфическими свойствами и являющиеся результатом химической реакции.
Применение реакций на металлы в промышленности

Реакции на металлы являются важной частью многих процессов промышленности. Металлы широко применяются в различных отраслях, начиная от строительства и заканчивая электронной промышленностью. Реакции на металлы позволяют получать новые материалы и сплавы с уникальными свойствами, что открывает широкие возможности для создания новых продуктов и технологий.
Одним из основных способов применения реакций на металлы в промышленности является создание различных сплавов. Сплавы – это материалы, состоящие из двух или более металлов. При соединении металлов путем реакции образуется сплав, который обладает новыми свойствами, такими как повышенная прочность, устойчивость к коррозии, термическая стабильность и др. Сплавы на основе железа, такие как стали и чугуны, широко используются в строительстве, машиностроении, автомобильной и авиационной промышленности.
Еще одной областью применения реакций на металлы является производство различных химических соединений. Металлы используются в качестве катализаторов для проведения различных химических реакций. Благодаря своим особым свойствам, металлы могут активировать молекулы и ускорять протекание реакции. Например, платина используется в каталитических реакциях для производства аммиака, который в дальнейшем применяется в производстве удобрений.
Реакции на металлы также играют важную роль в процессе обработки материалов. Металлы могут подвергаться различным термическим или химическим обработкам, которые изменяют их свойства и структуру. Например, отжиг – это термическая обработка металла, которая позволяет улучшить его механические свойства и устранить внутреннее напряжение. Также металлы могут быть покрыты различными защитными покрытиями, которые защищают их от коррозии или обеспечивают декоративный эффект.
В заключение можно сказать, что применение реакций на металлы в промышленности имеет огромное значение для различных отраслей. Благодаря реакциям на металлы, создаются новые материалы и сплавы с уникальными свойствами, производятся различные химические соединения, а также проводятся обработка и покрытие металлов, что позволяет получать продукты высокого качества и расширять возможности промышленных процессов.
Практические примеры реакций металлов
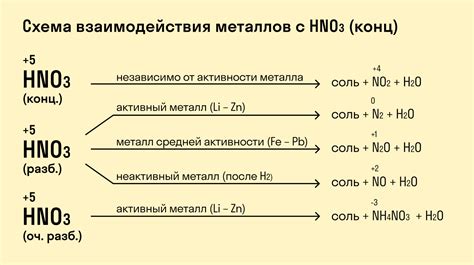
Металлы имеют способность вступать в различные химические реакции, проявляя свою активность. На практике эти реакции используются для получения нужных веществ, проведения анализа и определения металлов, а также в различных процессах производства.
Одним из практических примеров реакций металлов является реакция железа с кислородом. При взаимодействии этих веществ происходит окисление железа, при котором образуется ржавчина. Это явление широко применяется в повседневной жизни для защиты металлических поверхностей от коррозии.
Другим примером реакции металлов является взаимодействие алюминия с кислородом. При такой реакции алюминий окисляется, образуя оксид алюминия. Этот процесс используется в производстве алюминиевых изделий, таких как фольга или конструкционные материалы.
Еще одной практической реакцией металлов является их растворение в кислотах. Например, цинк при взаимодействии с соляной кислотой образует хлорид цинка и выделяется водород. Эта реакция используется в производстве гальванических элементов и батарей.
Также металлы могут вступать в реакцию с растворами солей. Например, при взаимодействии меди с раствором серной кислоты образуется сульфат меди и выделяется диоксид серы. Эта реакция используется для изготовления пигментов и красителей.
Взаимодействие металлов с веществами и растворами позволяет использовать эти реакции в различных областях науки и промышленности, от химических анализов до процессов получения новых материалов.
Перспективы развития и изучения реакций на металлы в химии
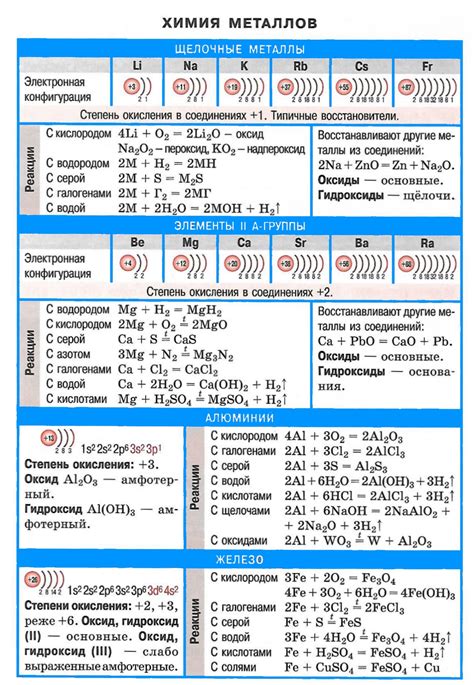
Изучение реакций металлов является важной областью в химии и имеет огромный потенциал для развития в будущем. Перспективы развития этой области связаны с разработкой новых методов исследования, а также с использованием современной аппаратуры и технологий.
Одной из перспективных областей изучения реакций на металлы является их роль в экологически чистых процессах. Металлы могут быть использованы в качестве катализаторов, участвующих в различных химических реакциях, например, в процессах очистки воды или утилизации отходов. Это открывает возможности для разработки новых эффективных и экологически безопасных методов обработки промышленных отходов и загрязненных веществ.
Другой перспективной областью развития является изучение взаимодействия металлов с биологическими системами. Металлы играют важную роль во многих биологических процессах, таких как ферментативная активность, регуляция генов и передача сигналов между клетками. Изучение этих реакций позволяет понять основы биохимических процессов и создать новые препараты на основе металлов для лечения различных заболеваний.
Также перспективы развития и изучения реакций на металлы в химии связаны с созданием новых материалов с улучшенными свойствами. Металлы могут быть использованы в производстве различных конструкционных материалов, сплавов и покрытий, которые обладают высокой прочностью, коррозионной стойкостью и другими важными свойствами. Развитие новых методов синтеза и модификации металлических материалов позволяет создавать материалы с уникальными свойствами, которые могут быть использованы в различных отраслях промышленности и научных исследованиях.
В целом, развитие и изучение реакций на металлы в химии имеет широкие перспективы и может привести к созданию новых технологий, материалов и методов, которые будут иметь значительное влияние на различные области науки и промышленности.
Вопрос-ответ

Какие методы использовались для изучения реакций металлов в химии?
Для изучения реакций металлов в химии было использовано множество методов, включая спектроскопические методы, электрохимические методы, рентгеноструктурный анализ, термический анализ и многое другое.
Какие методы спектроскопии применяются для изучения реакций металлов в химии?
Для изучения реакций металлов в химии часто используются методы спектроскопии, такие как УФ-видимая спектроскопия, инфракрасная спектроскопия и ЯМР-спектроскопия. Эти методы позволяют определить структуру и свойства реакционных промежуточных и конечных продуктов реакций металлов.
