Реакции металлов с солями других металлов являются одной из основных областей исследований в химии и имеют огромное практическое применение. Эти реакции включают в себя взаимодействие различных металлов, которые, в зависимости от своих химических свойств, могут образовывать разнообразные соединения.
Особенности таких реакций заключаются в том, что они могут протекать при разных условиях, таких как температура, концентрация реагентов и окружающая среда. Некоторые металлы могут образовывать стабильные и нерастворимые соединения, в то время как другие могут быть более реакционноспособными и образовывать растворимые соединения.
Применение реакций металлов с солями других металлов может быть разнообразным. Одним из таких применений является получение сплавов – материалов, состоящих из двух или более металлов. Сплавы обладают уникальными свойствами, которые не встречаются у исходных металлов. Также, данные реакции могут использоваться в процессе изготовления электроники и других технических устройств.
Внимание к реакциям металлов с солями других металлов не только связано с научно-исследовательскими целями, но и с практическим применением таких соединений в различных отраслях промышленности. Изучение особенностей этих реакций позволяет улучшить процессы производства и создать новые материалы с улучшенными свойствами.
Химические реакции металлов в солях

Металлы обладают способностью взаимодействовать с солями других металлов, что приводит к химическим реакциям. Результатом таких реакций может быть образование новых соединений, выпадение осадка или выделение газа. При этом важно учитывать различные особенности и условия, в которых проходят эти реакции.
Некоторые металлы, такие как медь, железо, цинк, могут взаимодействовать с солями других металлов, образуя сложные ионы. Например, ион меди Cu2+ может образовывать комплексные соединения с солями никеля, железа и других металлов. Эти соединения могут иметь различные свойства и применяться в различных областях, от промышленности до медицины.
Другие металлы, такие как алюминий и магний, могут реагировать с солями других металлов, образуя осадки. Например, при добавлении алюминия в раствор медного купороса (CuSO4), происходит образование осадка меди. Такие реакции могут быть использованы для выделения определенных металлов или очистки растворов.
Еще одним примером реакции металлов с солями может служить выделение газа. Например, при реакции цинка с соляной кислотой (HCl) выделяется водородный газ. Этот процесс широко используется в химической промышленности для получения водорода.
- Металлы могут образовывать комплексные соединения с солями других металлов.
- Некоторые металлы могут реагировать с солями и образовывать осадки.
- Реакции металлов с солями могут приводить к выделению газа.
Таким образом, химические реакции металлов в солях являются важным аспектом в химии и имеют различные применения в различных областях науки и промышленности.
Взаимодействие металлов разных групп

Взаимодействие металлов разных групп является одной из основных тем в химии. При этом происходят различные химические реакции, которые могут быть использованы в различных областях науки и промышленности.
Одной из наиболее распространенных реакций является образование агрегатов или сплавов металлов разных групп. Эта реакция позволяет создавать материалы с новыми свойствами, такими как повышенная прочность или стойкость к коррозии. Сплавы также могут быть использованы для создания различных изделий, включая автомобили, суда и промышленное оборудование.
Взаимодействие металлов разных групп также может приводить к образованию органометаллических соединений. Эти соединения широко применяются в органической химии, например, в качестве катализаторов реакций или в синтезе органических соединений. Органометаллические соединения также находят применение в фармацевтической и пищевой промышленности.
Кроме того, взаимодействие металлов разных групп может приводить к образованию растворимых комплексных соединений. Эти соединения находят применение в аналитической химии, так как они обладают определенными спектральными или кольцевыми свойствами, которые позволяют их использовать для определения концентрации металлов в растворе.
Таким образом, взаимодействие металлов разных групп является важным аспектом химии и имеет широкое практическое применение в различных областях науки и промышленности.
Влияние концентрации солей на реакцию
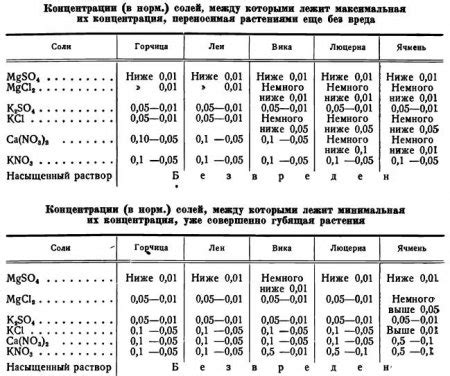
При взаимодействии металлов с солями других металлов важную роль играет концентрация солей. Концентрация влияет на скорость реакции, образование осадка и его количество, а также на степень окисления и восстановления металлов.
Высокая концентрация солей может способствовать более интенсивной реакции металла с солями. Это связано с тем, что высокая концентрация солей обеспечивает большее количество ионов, что усиливает их взаимодействие с металлом. В результате уменьшается время, необходимое для проведения реакции.
Однако при очень высокой концентрации солей может произойти обратная реакция - осадок начнет растворяться в растворе, образуя ионы, и реакция будет протекать в обратном направлении.
Концентрация соли также влияет на образование осадка и его количество. При высокой концентрации солей, образуется большее количество осадка, что может привести к увеличению его массы и объема. При низкой концентрации солей осадок может образовываться меньшими пластинками или же отсутствовать вообще.
Таким образом, концентрация солей играет важную роль в реакциях металлов с солями других металлов. Она влияет на скорость реакции, образование осадка и его количество, а также на степень окисления и восстановления металлов. Необходимо учитывать этот фактор при проведении экспериментов и применении реакции в практических целях.
Особенности взаимодействия различных металлов

Взаимодействие различных металлов может происходить при контакте между собой или при взаимодействии с солями других металлов. Это важный процесс, который находит широкое применение в различных областях.
Когда два разных металла соприкасаются, возникает электрохимическая реакция, известная как гальваническая коррозия. При этом один металл (анод) окисляется и переходит в ионное состояние, а другой металл (катод) получает электроны и выполняет роль электродного материала. Такое взаимодействие может привести к разрушению или образованию защитной пленки на поверхности металлов.
Однако, не все металлы способны взаимодействовать между собой или реагировать с солями других металлов. Некоторые металлы активны, то есть имеют высокую степень химической активности и легко реагируют с другими металлами или солями.
Другие металлы, например платина или золото, являются пассивными и не подвержены коррозии при контакте с большинством других металлов или реагентов.
Взаимодействие различных металлов используется в различных отраслях промышленности и науки. Например, в производстве батарей, гальванической обработке поверхности, а также в химическом анализе. Также оно может применяться для создания сплавов с новыми физическими и химическими свойствами.
В целом, взаимодействие металлов представляет большой интерес для исследователей и инженеров, поскольку позволяет создавать новые материалы и расширять границы применения уже существующих.
Роль реакций металлов с солями в промышленности
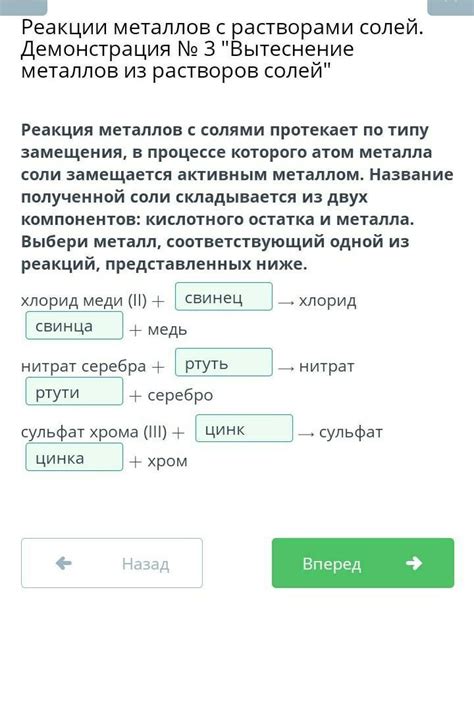
Реакции металлов с солями широко применяются в промышленности для получения различных продуктов и материалов. Одним из основных направлений использования таких реакций является получение металлов по электролизу и металлоизвлечению. Например, реакция алюминия с солями других металлов позволяет получать сплавы с заданными физическими и механическими свойствами, такие как прочность, твердость, коррозионная стойкость и др.
В процессе производства различных металлических изделий, таких как трубы, листы, провода, используются реакции металлов с солями для покрытия поверхности изделий защитными покрытиями. Например, реакция цинка с солями позволяет получить цинковое покрытие на стали, которое защищает ее от коррозии.
Реакции металлов с солями также используются в процессе производства красителей, керамических и стекловидных материалов. Например, реакция меди с солями в кислой среде позволяет получать красные пигменты, которые широко применяются в производстве красок и красителей.
Кроме того, реакции металлов с солями играют важную роль в процессе очистки промышленных сточных вод. Например, реакция железа с солями фосфорной кислоты позволяет осаждать фосфаты и тем самым уменьшать содержание фосфора в сточных водах предприятий, что способствует охране окружающей среды и экономии ресурсов.
Таким образом, реакции металлов с солями имеют широкий спектр применения в промышленности и являются неотъемлемой частью многих технологических процессов, позволяя получать различные продукты и материалы с заданными свойствами.
Применение реакций металлов с солями в лаборатории
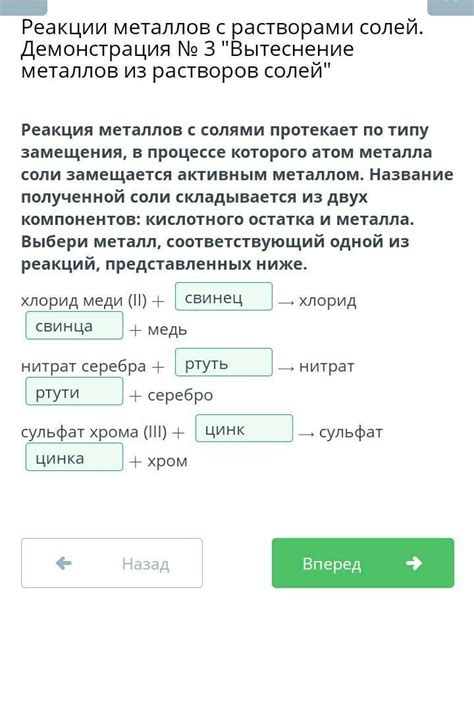
Реакции металлов с солями других металлов широко применяются в лабораториях для различных целей и исследований.
Одним из основных применений таких реакций является определение наличия и количества определенного металла в образце. Для этого проводятся реакции металла с солью этого же металла, и на основе образования осадка или изменения окраски раствора можно сделать вывод о наличии того или иного металла в образце.
Другим важным применением данных реакций является возможность получения новых соединений металлов и солей. Путем соединения различных металлов со солями других металлов можно получить разнообразные соединения с определенными свойствами, которые могут использоваться в дальнейших исследованиях или в промышленности.
Также реакции металлов с солями в лаборатории часто используются для проведения качественного анализа различных проб. Проведение таких реакций позволяет установить наличие или отсутствие определенных элементов и провести идентификацию пробы.
Важно отметить, что для успешного проведения реакций металлов с солями в лаборатории необходимо правильно подобрать соответствующие реагенты и условия. Также необходимо учитывать химические свойства и особенности каждого металла и соли, чтобы избежать нежелательных побочных реакций и получить точные результаты.
Значение реакций металлов с солями в химической аналитике
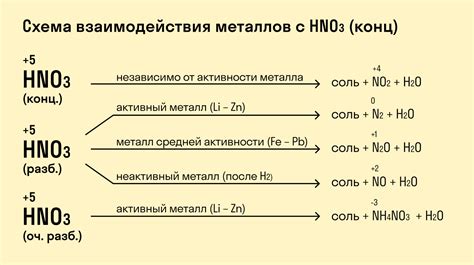
Реакции металлов с солями других металлов имеют важное значение в химической аналитике. Эти реакции позволяют проводить качественный и количественный анализ веществ, определять присутствие и концентрацию определенных металлов.
Качественный анализ на основе реакций металлов с солями позволяет выявлять наличие определенного металла в образце. Например, можно определить присутствие меди в растворе, добавив алюминий. В результате реакции образуется осадок меди, который можно идентифицировать.
Количественный анализ с использованием реакций металлов с солями позволяет определить концентрацию металла в образце. Например, можно определить содержание железа в воде, добавив цинк. В результате реакции образуется осадок гидроксида железа, который после фильтрации и взвешивания позволяет определить содержание железа.
Реакции металлов с солями широко применяются в различных областях химической аналитики, включая анализ пищевых продуктов, медицинский анализ, анализ сельскохозяйственных образцов и многое другое. Они позволяют определять содержание металлов в различных материалах и контролировать их качество.
Реакции металлов с солями - это надежный и удобный метод анализа, который позволяет идентифицировать и определить содержание металлов в образце. Эти реакции имеют большое значение в химической аналитике и находят применение во многих областях науки и промышленности.
Вопрос-ответ

Какие особенности реакции металлов с солями других металлов?
Реакция металлов с солями других металлов является обменной реакцией, при которой происходит обмен ионами. Это значит, что ионы металла из соли замещают ионы металла из раствора. Реакция может быть как спонтанной, так и индуцированной при добавлении катализатора или изменении условий окружающей среды. Особенности реакции зависят от свойств металлов, их электрохимических потенциалов и концентраций ионов в растворах.
Какие металлы реагируют с солями других металлов?
Многие металлы могут реагировать с солями других металлов, но скорость и характер реакции зависят от их электрохимического потенциала. Металлы с более высоким электрохимическим потенциалом (такие как щелочные металлы и щелочноземельные металлы) более активны и обычно замещают ионы металлов с более низким электрохимическим потенциалом. Например, натрий может реагировать с солями многих металлов, включая железо и медь.
Какие применения имеют реакции металлов с солями других металлов?
Реакции металлов с солями других металлов имеют широкий спектр применений. Одно из основных применений - получение металлов из их руд и концентратов. Например, при использовании цинка в качестве реагента можно получить медь из ее солей. Кроме того, реакции металлов с солями других металлов обычно используются в химической промышленности для получения соединений металлов, таких как сульфаты или нитраты, которые в дальнейшем могут использоваться в различных отраслях промышленности.
