В химии существует группа металлов, которые проявляют особую активность и способны взаимодействовать как с кислотами, так и с щелочами. Эти металлы называются амфотерными. Классическим примером амфотерного металла является алюминий. Реакция амфотерного металла с водой обладает своими особенностями, которые определяются его электрохимическими свойствами.
Вода, будучи биполярной молекулой, может выступать как кислотой (принимая электроны), так и щелочью (отдавая электроны). Взаимодействие амфотерного металла с водой зависит от его электрохимической активности и силы окислительно-восстановительного потенциала. К примеру, алюминий при контакте с водой образует гидроксид алюминия и выделяет водород. Поэтому на практике нередко применяется реакция амфотерного металла с водой для получения нужных соединений или очистки от нежелательных примесей.
Однако, не все амфотерные металлы проявляют такую высокую реактивность с водой, как алюминий. Например, цинк или свинец не реагируют с водой столь интенсивно и образуют лишь небольшое количество соответствующих гидроксидов.
Реакции амфотерных металлов с водой можно встретить в различных областях. В промышленности они используются при производстве кислот и щелочей, при получении специальных сплавов и соединений, а также в процессах очистки и обработки различных материалов. При изучении этих реакций, ученые получают новые сведения о химической активности веществ и разрабатывают методы улучшения технологических процессов с использованием амфотерных металлов.
Амфотерные металлы: свойства и назначение
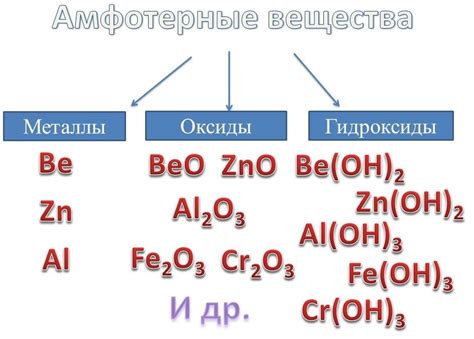
Амфотерные металлы - это класс элементов, обладающих способностью проявлять кислотные и основные свойства при взаимодействии с различными соединениями. Это делает их уникальными и широко используемыми в разных отраслях.
Главной особенностью амфотерных металлов является возможность вступать в реакции с кислотами и основаниями. При контакте с кислотами они образуют соли, а при контакте с основаниями происходит образование гидроксокомплексов. Эта свойственная им двойственность позволяет использовать амфотерные металлы в широком спектре применений.
Одним из важнейших применений амфотерных металлов является использование их в производстве лекарственных препаратов. Например, амфотерный металл алюминий часто используется в производстве препаратов от гастроэнтерологических заболеваний, а также препаратов для лечения ожогов.
Кроме того, амфотерные металлы применяются в качестве катализаторов в химической промышленности. Благодаря своей способности менять степень окисления, амфотерные металлы могут участвовать в различных химических реакциях, ускоряя их протекание. Это делает их незаменимыми при производстве различных органических соединений, полимеров и других химических продуктов.
Кроме того, амфотерные металлы также применяются в электронике и металлургии. Они используются для создания специальных сплавов, которые отличаются особыми характеристиками: высокой прочностью, устойчивостью к коррозии и теплостойкостью. Такие сплавы применяются, например, в авиационной и космической промышленности.
Реакции амфотерных металлов с водой: химические процессы
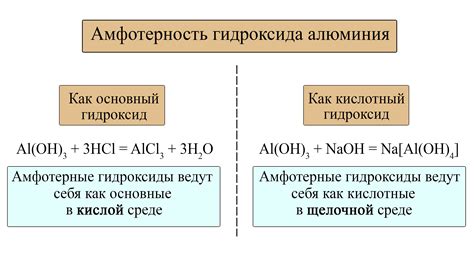
Амфотерные металлы являются особой группой химических элементов, которые способны взаимодействовать с водой и проявлять свойства и щелочных, и кислотных оксидов. Под воздействием воды происходят химические процессы, которые определяются электрохимическими свойствами данных металлов.
В случае амфотерных металлов, реакция с водой зависит от оксидационного состояния металла. Если металл находится в оксидационном состоянии +2, то он образует гидроксид, который обладает щелочными свойствами. Примером такого металла может служить цинк (Zn), который реагирует с водой и образует гидроксид цинка (Zn(OH)2).
С другой стороны, если амфотерный металл находится в оксидационном состоянии +3, то он образует кислотный гидроксид. Например, алюминий (Al) взаимодействует с водой и образует кислотный гидроксид алюминия (Al(OH)3). Это свойство амфотерных металлов позволяет им проявлять кислотные свойства в контакте с основаниями и щелочами, и щелочные свойства в контакте с кислотами.
Таким образом, реакции амфотерных металлов с водой являются результатом электрохимических процессов и зависят от оксидационного состояния данных металлов. Это явление отличает амфотерные металлы от других групп в периодической системе элементов и позволяет им проявлять свойства как кислот, так и оснований.
Примеры реакций амфотерных металлов с водой: алюминий, цинк, олово
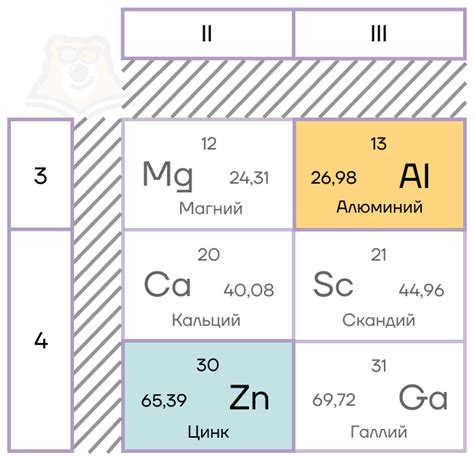
Амфотерные металлы - это металлы, которые могут реагировать как с кислотами, так и с основаниями. Они обладают особенной реакционной способностью, которая проявляется при контакте с водой. Некоторые примеры таких металлов включают алюминий, цинк и олово.
Алюминий является одним из самых распространенных амфотерных металлов. При реакции с водой образуется оксид алюминия (Al2O3) и водород. Данная реакция протекает медленно и не столь интенсивно, что делает алюминий пригодным для использования в различных областях, например, в строительстве и производстве авиационной техники.
В случае с цинком, реакция с водой происходит более активно. Цинк вступает в реакцию с водой, образуя оксид цинка (ZnO) и водород. Реакция с водой является одной из основных реакций, происходящих с цинком, что позволяет использовать его в различных промышленных и химических процессах.
Олово также реагирует с водой, образуя оксид олова (SnO2) и водород. Реакция проходит достаточно интенсивно, особенно при нагревании, и может использоваться в процессе производства сплавов и других химических соединений, где требуется активное участие металла.
Вопрос-ответ

Какие металлы относятся к амфотерным?
К амфотерным металлам относятся алюминий, цинк, свинец и несколько других.
Можете привести примеры амфотерных металлов?
Примеры амфотерных металлов: алюминий, цинк, свинец, железо, титан и хром.
Что происходит при реакции амфотерных металлов с водой?
При реакции амфотерных металлов с водой образуется гидроксид металла и выделяется водород.
Какие особенности имеют реакции амфотерных металлов с водой?
Особенности реакций амфотерных металлов с водой включают образование гидроксидов металлов различной степени основности и выделение водорода.
