Взаимодействие активных металлов с кислородом является одним из основных процессов в химии и физико-химии. Это взаимодействие имеет важное значение как в естественных, так и в промышленных процессах. Кислород присутствует повсеместно в окружающей среде, а активные металлы, такие как натрий, калий и литий, широко используются в различных областях, включая энергетику, электронику и металлургию.
Механизм взаимодействия активных металлов с кислородом в основном определяется электронным распределением в атомах и их химическими свойствами. Активные металлы обладают относительно низкими энергиями ионизации, что позволяет им легко отдавать электроны. Кислород, с другой стороны, имеет высокую электроотрицательность и способен принимать электроны. В результате, при взаимодействии активных металлов с кислородом происходит передача электронов, что вызывает образование ионов металла и кислорода.
Особенности взаимодействия активных металлов с кислородом могут быть связаны с различными факторами, такими как температура, концентрация металла и кислорода, а также наличие катализаторов или ингибиторов. Например, при повышенной температуре и высокой концентрации активного металла взаимодействие с кислородом может проходить с большей интенсивностью и образование оксидов будет более активным. Наличие катализаторов может значительно ускорить реакцию взаимодействия активного металла с кислородом, тогда как ингибиторы могут замедлить или предотвратить данную реакцию.
Активные металлы: свойства и реактивность
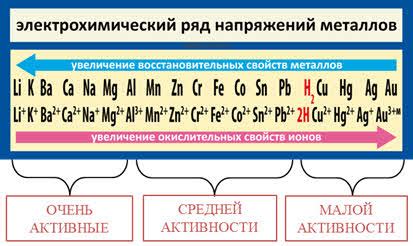
Активные металлы – это группа химических элементов, которые высоко реактивны и способны активно взаимодействовать с различными веществами. Такие металлы, как натрий, калий, литий, магний, алюминий и другие, характеризуются наличием одной или двух валентностей.
Одно из ключевых свойств активных металлов - их реакция с кислородом. При контакте с воздухом или кислородом происходит окисление активных металлов. При этом металлическая поверхность покрывается слоем оксида, который защищает металл от дальнейшего взаимодействия с кислородом.
Активные металлы также проявляют способность гореть в кислороде. Горение активных металлов сопровождается выделением яркого пламени и образованием соответствующих оксидов металлов.
Взаимодействие активных металлов с кислородом основано на электрохимических процессах, в результате которых происходит передача электронов от металла к кислороду. Такие реакции играют важную роль в промышленности и используются для получения металлических оксидов и кислорода.
Наблюдая за взаимодействием активных металлов с кислородом, можно увидеть яркие взрывы, высокую температуру и образование важных продуктов, которые широко применяются в нашей повседневной жизни.
Механизм взаимодействия металлов с кислородом

Механизм взаимодействия металлов с кислородом зависит от свойств конкретного металла и условий окружающей среды. Одним из основных способов взаимодействия металлов с кислородом является окисление металла в результате реакции с кислородом. Кислород может вступать в химическую реакцию с металлом путем передачи электронов, что приводит к образованию оксидов или других соединений металла с кислородом.
Часто механизм взаимодействия зависит от свойств металлической поверхности. Различные структуры поверхности и среды влияют на скорость и интенсивность реакции. Многие металлы имеют защитную оксидную пленку на поверхности, которая может предотвращать дальнейшее окисление металла. Однако, в некоторых условиях, таких как высокая температура или наличие агрессивных веществ, оксидная пленка может разрушаться и металл начинает активно реагировать с кислородом.
Кроме того, металлы могут взаимодействовать с кислородом через катализаторы или ферменты, участвующие в реакции. Катализаторы ускоряют скорость химических реакций, облегчая взаимодействие между металлом и кислородом. Ферменты также участвуют в реакциях окисления металлов и могут изменять механизм взаимодействия и скорость процесса.
Изучение механизмов взаимодействия активных металлов с кислородом имеет большое значение, так как позволяет понять процессы окисления и коррозии металлов. Это важно для разработки новых материалов с улучшенной стойкостью к окислительным реакциям и разработки новых методов защиты металлических конструкций от окисления и коррозии.
Влияние структуры металла на реакцию

Структура металла играет важную роль в его взаимодействии с кислородом. Кристаллическая решетка и форма металла определяют доступность активных центров для реакций и механизмы реакции.
Например, катализаторы на основе металлов могут иметь различные структуры, такие как наночастицы, пленки или порошки. В наночастицах повышается отношение поверхности к объему, что способствует усилению взаимодействия с кислородом и, следовательно, улучшению реакции.
Размер и форма наночастиц могут также повлиять на скорость реакции. Наночастицы с большой площадью поверхности имеют больше активных центров, что способствует эффективной реакции с кислородом. Кроме того, форма наночастицы может создавать эффекты синергии, когда сопряженные поверхности взаимодействуют, усиливая реакцию.
Структура металла также может влиять на механизм реакции с кислородом. Например, металлы с различными механизмами реакции могут обеспечивать различные продукты реакции или селективности. Это связано с различной способностью металла активировать и связывать кислород.
Дополнительно, некоторые металлы могут обладать специфическими свойствами и структурами, такими как покрытия, сплавы или оксиды. Эти структуры могут быть дополнительными факторами, которые влияют на реакцию с кислородом.
Особенности реакций с кислородом различных активных металлов

1. Натрий: Реакция натрия с кислородом приводит к образованию оксида натрия (Na2O). При этом натрий сгорает с ярким языком пламени и выделяется большое количество тепла. Реакция является экзотермической.
2. Калий: Реакция калия с кислородом аналогична реакции натрия и также приводит к образованию оксида калия (K2O). Калий также сгорает с ярким пламенем и выделяет большое количество тепла.
3. Литий: Реакция лития с кислородом более интенсивная по сравнению с натрием и калием. Литий сгорает с ярким светом, образуя оксид лития (Li2O). Кроме того, реакция лития с кислородом происходит при намного ниже температуре, чем у других активных металлов.
4. Магний: Реакция магния с кислородом приводит к образованию оксида магния (MgO). Однако, в отличие от натрия, калия и лития, реакция магния не сопровождается ярким пламенем и выделением большого количества тепла.
5. Алюминий: Реакция алюминия с кислородом приводит к образованию оксида алюминия (Al2O3), который имеет высокую степень твердости и низкую растворимость в воде. Реакция происходит при очень высокой температуре и требует наличия катализаторов для совершения.
6. Железо: Реакция железа с кислородом приводит к образованию оксида железа (Fe2O3), который известен как ржавчина. Реакция происходит медленно в обычных условиях, но прискорбно ускоряется во влажной среде.
7. Медь: Реакция меди с кислородом приводит к образованию оксида меди (CuO). Однако, медь имеет меньшую реакционную способность по сравнению с более активными металлами, поэтому реакция проходит медленно.
8. Цинк: Реакция цинка с кислородом приводит к образованию оксида цинка (ZnO). Цинк проявляет слабую реакционную способность с кислородом и образует пассивную защитную пленку оксида на поверхности, которая предотвращает дальнейшую реакцию.
Физические и химические свойства сформированных соединений
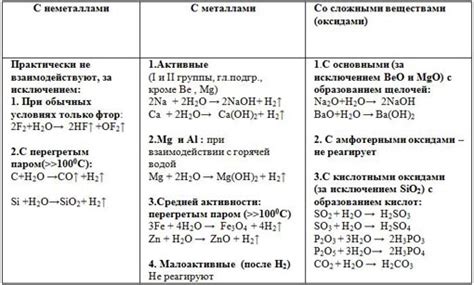
Физические свойства:
- Температура плавления и кипения соединений, образованных взаимодействием активных металлов с кислородом, может быть разной. Например, оксид алюминия (Al2O3) имеет высокую точку плавления и кипения, что делает его применимым в качестве термостойкого материала.
- Некоторые соединения обладают высокой плотностью, что делает их полезными в различных технических приложениях. Например, оксид железа (Fe2O3) обладает высокой плотностью и используется в производстве садовых инструментов.
- Известны соединения активных металлов с кислородом, которые обладают проводимостью электричества. Например, оксид меди (CuO) имеет полупроводниковые свойства и находит применение в электронике.
Химические свойства:
- Соединения, образованные в результате взаимодействия активных металлов с кислородом, обычно являются оксидами или пероксидами. Например, оксид алюминия (Al2O3) и пероксид водорода (H2O2) - это основные продукты реакции алюминия с кислородом.
- Некоторые соединения могут обладать кислотными свойствами и реагировать с щелочами. Например, оксид натрия (Na2O) реагирует с водой, образуя щелочной раствор.
- Соединения активных металлов с кислородом обычно являются реактивными и могут оказывать влияние на окружающую среду. Например, оксид серы (SO2) является вредным веществом, который может вызывать ожоги и раздражение дыхательных путей.
Таблица с примерами соединений активных металлов с кислородом и их физическими и химическими свойствами:
| Соединение | Физические свойства | Химические свойства |
|---|---|---|
| Оксид алюминия (Al2O3) | Высокая т.п. и т.к., термостойкость | Не обладает кислотными свойствами, нерастворим в воде |
| Оксид железа (Fe2O3) | Высокая плотность | Не обладает кислотными свойствами, используется в качестве красителя |
| Оксид меди (CuO) | Полупроводниковые свойства | Не обладает кислотными свойствами, используется в электронике |
Применение реакций активных металлов с кислородом

Взаимодействие активных металлов с кислородом - важная область химических исследований, которая находит применение в различных сферах. Одним из наиболее распространенных применений реакций активных металлов с кислородом является получение металлических оксидов.
Металлические оксиды имеют широкий спектр применений, включая использование в качестве катализаторов, сырья для производства электроники, стекла и керамики, а также в процессах очистки воды и воздуха. Реакция активных металлов с кислородом позволяет получать оксиды различной структуры и свойств, что позволяет удовлетворить потребности различных отраслей промышленности.
Кроме того, реакции активных металлов с кислородом могут активировать катализаторы для различных химических процессов. Например, активация палладиевых катализаторов на поверхности активного металла позволяет повысить их активность и селективность при процессах окисления органических веществ.
Уникальные свойства активных металлов также позволяют использовать их в процессах хранения и переноса кислорода. Например, в некоторых аккумуляторах и батареях используются материалы на основе активных металлов, которые обеспечивают высокую энергоемкость и длительную работу устройств.
Вопрос-ответ

Какие металлы взаимодействуют с кислородом?
С кислородом взаимодействуют активные металлы, такие как натрий, калий, кальций, магний и др.
Какой механизм взаимодействия между активными металлами и кислородом?
Механизм взаимодействия активных металлов с кислородом связан с образованием окислов металлов при воздействии кислорода.
Какие особенности имеет взаимодействие активных металлов с кислородом?
Особенностью взаимодействия активных металлов с кислородом является высокая реакционная способность металлов, что приводит к быстрому образованию окислов при контакте с кислородом.
Какова роль кислорода во взаимодействии с активными металлами?
Кислород играет роль окислителя во взаимодействии с активными металлами. Он принимает электроны от металла, образуя оксид металла.
