Ацетилен (этин) – один из наиболее используемых органических соединений в химической промышленности. В силу своих уникальных свойств, ацетилен является идеальным объектом для реакций с различными металлами. Эти реакции обладают ярко выраженными особенностями и находят широкое применение в различных областях науки и техники.
Реакции ацетилена с металлами протекают по-разному в зависимости от условий проведения и характера металла. Одним из наиболее известных примеров таких реакций является взаимодействие ацетилена с медью, в результате которого образуется вещество под названием ацетиленцианид. Этот сложный органический соединение обладает высокой степенью устойчивости и находит применение в производстве различных фармацевтических препаратов и пластиковых материалов.
Кроме того, реакции ацетилена с металлами могут привести к образованию металлоорганических соединений, которые являются прекурсорами для получения синтетических порошков и катализаторов. Так, реакция ацетилена с железом приводит к образованию железоценных соединений, которые с успехом применяют в процессах катализа.
Таким образом, реакции ацетилена с металлами представляют не только научный, но и практический интерес. Изучение этих реакций позволяет расширить наши знания о физико-химических свойствах металлов и разработать новые способы получения органических соединений с использованием этих металлов.
Взаимодействие ацетилена с металлами
Ацетилен, или этилендиин, CH≡CH, является одной из самых простых нециклических алкинов. Он может взаимодействовать с различными металлами, образуя разнообразные соединения.
Взаимодействие ацетилена с металлами может привести к образованию металлоорганических соединений, включающих комплексы ацетиленатов. Такие соединения могут проявлять различные физические и химические свойства, и их можно использовать в различных областях науки и промышленности.
Взаимодействие ацетилена с металлами может привести к образованию координационных связей между атомами углерода ацетилена и атомами металла. Это может приводить к образованию различных структурных форм ацетиленатных комплексов, в том числе линейных, квадратных планарных и трехгранниковых структур.
Взаимодействие ацетилена с металлами имеет большое значение в органическом синтезе, где ацетилен используется в качестве исходного сырья для получения различных органических соединений. Кроме того, металлоорганические соединения ацетилена могут использоваться в качестве катализаторов при проведении реакций гидрирования, полимеризации и других процессах.
- Примером реакции взаимодействия ацетилена с металлами является получение этиленовых металлоорганических соединений с помощью металлорганических соединений натрия, калия и других металлов.
- Ацетилен также может взаимодействовать с металлами, образуя ацетиленовые комплексы. При этом ацетиленатные комплексы могут иметь различную структуру и быть как нейтральными, так и зарядными.
Взаимодействие ацетилена с металлами и получаемые при этом металлоорганические соединения имеют широкое применение в различных областях, включая катализ синтеза органических соединений, процессы получения синтетических волокон, полимеризацию и другие химические реакции. Кроме того, ацетиленатные комплексы используются в промышленности для получения высокопрочных материалов, а также в качестве катализаторов при производстве пластмасс и резиновых изделий.
Химические свойства реакции ацетилена с металлами

Реакция ацетилена с металлами является одной из важных и широко изучаемых химических реакций. Ацетилен (этин) - это органическое соединение с формулой C2H2, представляющее собой наиболее простой алкин. Ацетилен обладает высокой реакционной способностью, что позволяет ему взаимодействовать с различными элементами, в том числе с металлами.
У металлов реакция ацетилена протекает с образованием металлоорганических соединений, таких как металлоцены. Металлоцены представляют собой комплексные соединения, в которых ацетилен связывается с атомом металла. Эти соединения обладают разнообразными свойствами и находят применение в различных областях, таких как каталитические реакции, синтез органических соединений и полимеров.
Реакция ацетилена с металлами проходит при высоких температурах и в присутствии катализатора. Процесс протекает по следующей схеме: ацетилен взаимодействует с металлом, образуя металлокарбид, затем происходит образование металлоорганического соединения. Для ускорения реакции могут использоваться различные катализаторы, например никель, палладий или платина.
Кроме того, реакция ацетилена с металлами может приводить к образованию сажи или графита. Это связано с тем, что ацетилен является источником углерода, который может осаждаться на поверхности металла и образовывать графитовые структуры. Этот процесс имеет большое значение в производстве электродов для различных электрических устройств.
Реактивность ацетилена в зависимости от металла

Реакция ацетилена с металлами в зависимости от их природы и свойств может проходить по-разному. Ацетилен обладает высокой реакционной способностью благодаря своей тройной связи, которая может быть атакована металлами.
Металлы, обладающие большой электроотрицательностью, отрицательным электродным потенциалом и способностью образовывать стабильные катионы, обычно сильно взаимодействуют с ацетиленом. Они могут реагировать с ним сверхстехиометрически, образуя металлоациклические соединения типа металлокарбенов или комплексы с уже образовавшимся карбеновым кольцом.
Среди таких металлов можно выделить платину, палладий и никель. Они образуют стабильные катионы и способны к образованию комплексов с ацетиленом. Реакция ацетилена с платиной, например, приводит к образованию платинового комплекса [Pt(C₂H₂)₂], который используется в качестве смачивающего агента в катализаторах и применяется в производстве важных органических соединений.
Однако не все металлы так сильно реагируют с ацетиленом. Некоторые металлы, например железо или медь, не образуют стабильные катионы и не обладают достаточной электроотрицательностью для образования комплексов с ацетиленом. Вместо этого они могут просто образовывать ацетиленовые радикалы и участвовать в дальнейших реакциях, например, в полимеризации ацетилена.
Таким образом, реактивность ацетилена в зависимости от металла может варьировать от сильно взаимодействующих металлов, образующих комплексы с ацетиленом, до металлов, образующих ацетиленовые радикалы и участвующих в других реакциях. Это открывает возможности для применения ацетилена в различных областях органической химии и катализа.
Применение реакции ацетилена с металлами в промышленности
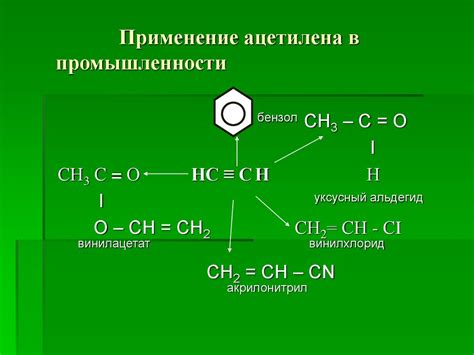
Реакция ацетилена с металлами находит широкое применение в различных отраслях промышленности благодаря своим уникальным свойствам и возможностям.
Одной из основных областей применения данной реакции является производство ацетиленовых горелок. Это высокоэффективные источники тепла, которые находят применение в металлургии, строительстве, машиностроении и других отраслях. Реакция ацетилена с металлами позволяет получать высокотемпературное пламя, которое используется для пайки, сварки и расплавления металлов.
Также реакция ацетилена с металлами применяется в производстве органических соединений, таких как уксусная кислота и ацетаты. Ацетилен является важным сырьем для синтеза этих веществ, и обратная реакция с металлами позволяет эффективно получать необходимые продукты.
В нефтегазовой промышленности реакция ацетилена с металлами используется для очистки нефти и газа от сероводорода и других сернистых соединений. Металлические катализаторы способствуют превращению этих вредных веществ в более безопасные и полезные соединения.
Благодаря своей высокой активности и возможности восстановления, металлические катализаторы, полученные в результате реакции ацетилена с металлами, используются в химической промышленности для проведения различных реакций синтеза органических соединений. Такие катализаторы позволяют упростить процесс синтеза, повысить его эффективность и получить более высокую выходную продукцию.
Таким образом, применение реакции ацетилена с металлами в промышленности является важным и перспективным направлением, которое находит применение в различных отраслях и способствует созданию новых эффективных технологий и продуктов.
Влияние условий реакции на результат

Реакции ацетилена с металлами в значительной степени зависят от условий, в которых они происходят. Различные параметры, такие как температура, давление, концентрация реагентов и наличие катализаторов, могут существенно влиять на ход и результат реакции.
Температура является одним из наиболее важных факторов, определяющих путь реакции. Повышение температуры может привести к ускорению реакции и образованию большего количества продуктов. Однако слишком высокая температура может также способствовать образованию нежелательных побочных продуктов или деструкции реагентов.
Давление также может оказывать влияние на реакцию ацетилена с металлами. Повышенное давление может способствовать ускорению реакции, так как более высокая концентрация реагентов обеспечивает большую вероятность их взаимодействия. Однако, слишком высокое давление может оказывать негативное влияние на стабильность реагентов или приводить к образованию нежелательных побочных продуктов.
Концентрация реагентов также может оказывать важное влияние на результат реакции. Повышение концентрации ацетилена или металла может привести к увеличению скорости реакции и образованию большего количества продуктов. Однако, высокая концентрация реагентов может также способствовать образованию побочных продуктов или вызывать конкуренцию между различными реакциями.
Наличие катализаторов может существенно изменять ход реакции ацетилена с металлами. Катализаторы могут активировать реагенты, снижить температуру и давление необходимые для реакции или повысить специфичность реагентов. Однако, неправильный выбор катализатора или его недостаточное количество может привести к неселективной или неполной реакции.
Вопрос-ответ

Какие металлы могут реагировать с ацетиленом?
Ацетилен может реагировать с металлами, такими как медь, никель, платина, серебро, золото и др.
В чем заключается особенность реакции ацетилена с металлами?
Особенностью реакции ацетилена с металлами является образование ацетиленида металла, который может иметь различные полезные свойства, такие как катализаторы, сопротивление коррозии и др.
