Нитраты металлов являются важными соединениями, которые используются в различных областях науки и техники. Одной из важных задач является разложение нитратов с целью получения металлического вещества. При этом важно понимать механизмы разложения нитратов металлов разной активности, а также возможные пути применения полученных продуктов.
Механизмы разложения нитратов металлов разной активности могут существенно отличаться друг от друга. Однако существует несколько общих принципов, которые применимы к большинству случаев. Во-первых, разложение нитратов может происходить под воздействием тепла или катализаторов. Во-вторых, процесс может сопровождаться образованием газов или окислителей. В-третьих, различные физические и химические условия могут влиять на скорость и эффективность разложения нитратов.
Применение разложения нитратов металлов разной активности может быть очень разнообразным. Полученные продукты могут использоваться в производстве катализаторов, взрывчатых веществ, пигментов, а также в других областях, связанных с металлургией и химической промышленностью. Кроме того, разложение нитратов может быть важным этапом в процессе очистки воды от нитратов, которые могут быть опасными для здоровья человека.
Таким образом, изучение механизмов разложения нитратов металлов разной активности является важной задачей, которая имеет широкий практический потенциал. Этот процесс может привести к получению ценных продуктов, а также может быть полезным для решения экологических проблем. Дальнейшие исследования в этой области помогут расширить наши знания и применение разложения нитратов металлов разной активности в будущем.
Исследование разложения нитратов металлов: механизмы и применение

Нитраты металлов - это соединения, в которых металл основу образуется положительным ионом, а нитратная группа — отрицательным ионом, содержащим атом азота и атомы кислорода. Исследование разложения нитратов металлов играет важную роль в химии, так как оно позволяет понять механизмы реакции и найти применение полученным результатам.
Механизмы разложения нитратов металлов могут быть разными в зависимости от конкретного металла и условий реакции. Для некоторых металлов, таких как магний или алюминий, разложение происходит при подогревании нитратов и образовании оксида металла и оксида азота. Для других металлов, таких как свинец или медь, разложение может происходить при взаимодействии с другими химическими веществами, например, солями или кислотами.
Применение разложения нитратов металлов может быть разнообразным. Одним из основных применений является получение металлических оксидов, которые имеют широкое применение в различных отраслях промышленности, например, в производстве керамики, электроники, лакокрасочных материалов и других материалов. Кроме того, разложение нитратов металлов может быть использовано для получения нитритов, которые являются важными компонентами в производстве пищевых добавок и консервантов. Также, изучение механизмов разложения нитратов металлов может применяться для разработки новых способов синтеза металлических соединений и оптимизации процессов получения материалов с определенными свойствами.
В целом, исследование разложения нитратов металлов является актуальной и важной задачей в химии. Понимание механизмов реакции и применение полученных результатов позволяет разрабатывать новые способы синтеза материалов и использовать их в различных областях промышленности и научных исследований.
Металлы различной активности в разложении нитратов
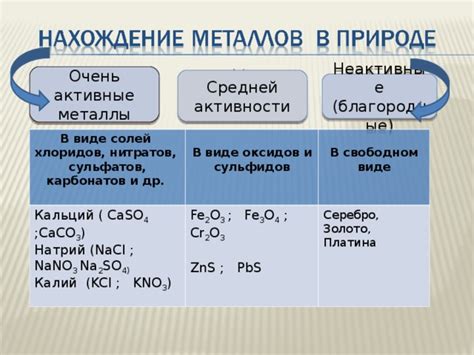
Разложение нитратов металлов разной активности является важной химической реакцией, которая применяется в различных областях науки и техники. Металлы различной активности имеют разную способность к взаимодействию с окислительными и восстановительными средствами, что определяет их роль в разложении нитратов.
Активные металлы, такие как калий (K) и натрий (Na), имеют высокую активность и легко взаимодействуют с нитратами, образуя оксиды и освобождая азотную кислоту в виде газа. Такие реакции эффективно используются в промышленности для получения азотной кислоты и ее производных.
Менее активные металлы, например, алюминий (Al) и железо (Fe), не реагируют с нитратами при комнатной температуре, но могут разлагаться при нагревании или в присутствии катализаторов. Такие реакции разложения нитратов металлов различной активности могут использоваться в аналитической химии для определения содержания нитратов в образцах.
Металлы разной активности в разложении нитратов также могут быть использованы в химическом синтезе для получения сложных соединений. Например, взаимодействие нитрата меди (Cu(NO3)2) с нитратом калия (KNO3) и нитратом свинца (Pb(NO3)2) может привести к образованию сложных соединений меди, калия и свинца.
Механизмы разложения нитратов металлов

Разложение нитратов металлов является важным процессом, который используется в различных областях, включая промышленность, медицину и научные исследования. Механизмы разложения нитратов металлов могут быть разными в зависимости от активности металла и условий процесса.
Один из основных механизмов разложения нитратов металлов - это термическое разложение. При нагревании нитратов металлов происходит распад на оксид металла и окислительный газ, обычно оксид азота. Температура разложения зависит от активности металла и его соединения с другими элементами.
Еще одним механизмом разложения нитратов металлов является электролитическое разложение. В этом случае нитрат металла подвергается воздействию электрического тока, что приводит к разложению на ионы металла и ионы нитрата. Этот процесс широко используется для получения высокочистых металлических соединений и наноматериалов.
Кроме того, нитраты металлов могут разлагаться под действием других химических реагентов, таких как кислоты или щелочи. При взаимодействии с кислотами нитраты металлов могут превращаться в соответствующие соли кислот, а с щелочами - в гидроксиды. Это может быть полезно при получении определенных соединений для промышленных или научных целей.
В заключение, механизмы разложения нитратов металлов могут быть разнообразными и зависят от множества факторов. Изучение этих механизмов позволяет лучше понять и контролировать процессы разложения нитратов металлов, а также использовать их в различных сферах деятельности.
Факторы, влияющие на скорость разложения нитратов металлов
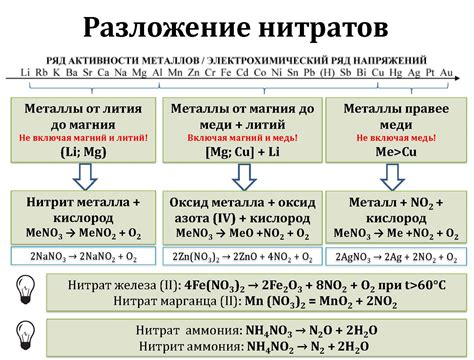
Скорость разложения нитратов металлов может зависеть от нескольких факторов. Важным фактором является активность самого металла. Самые активные металлы, такие как калий и натрий, обладают большей скоростью разложения своих нитратов, поскольку они легко взаимодействуют с окружающей средой и могут передавать электроны более эффективно.
Температура также оказывает влияние на скорость разложения нитратов металлов. При повышении температуры, скорость химических реакций обычно увеличивается. Таким образом, при повышении температуры, скорость разложения нитратов металлов также увеличивается. Однако, слишком высокие температуры могут привести к нежелательным побочным реакциям или разрушению продуктов.
Концентрация реагирующих веществ также играет роль в скорости разложения нитратов металлов. Принцип Ле Шателье гласит, что концентрация реагентов может влиять на положение равновесия химической реакции. Поэтому, повышение концентрации нитратов металлов может увеличить скорость их разложения.
Наличие катализатора также может существенно влиять на скорость разложения нитратов металлов. Катализатор обеспечивает альтернативный механизм реакции, который ускоряет процесс. Например, некоторые металлы могут выступать в роли катализаторов и повышать скорость разложения нитратов металлов.
Каталитическое применение разложения нитратов металлов
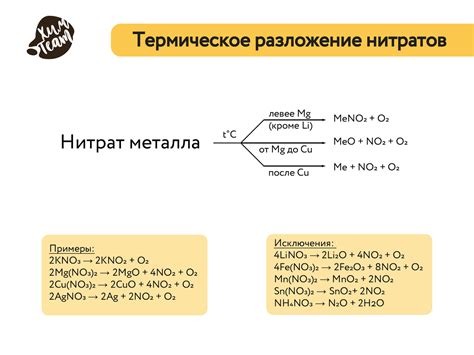
Разложение нитратов металлов является важным процессом, который может использоваться в качестве каталитической реакции. Каталитическое применение разложения нитратов металлов имеет широкий спектр применения и может быть использовано в различных отраслях промышленности и науки.
Одно из возможных применений разложения нитратов металлов в каталитических реакциях связано с производством аммиака. Реакция разложения нитрата аммония может использоваться для получения аммиака, который является важным сырьем для производства удобрений. Каталитическое разложение нитратов металлов может значительно повысить эффективность процесса и снизить затраты на производство.
Кроме того, разложение нитратов металлов может быть применено в процессе очистки промышленных сточных вод. Реакция разложения нитратов может использоваться для удаления нитратов из сточных вод, что является значительной проблемой во многих отраслях промышленности. Каталитическое разложение нитратов металлов может быть эффективным и экологически безопасным методом очистки сточных вод.
Более того, разложение нитратов металлов может быть использовано в процессе синтеза экологически чистых катализаторов. Реакция разложения нитратов металлов может быть использована для получения наночастиц металлов, которые могут быть использованы в качестве катализаторов в различных химических процессах. Каталитическое разложение нитратов металлов позволяет получить катализаторы с определенными размерами и формами, что может значительно повысить их активность и селективность.
Применение разложения нитратов металлов в синтезе материалов
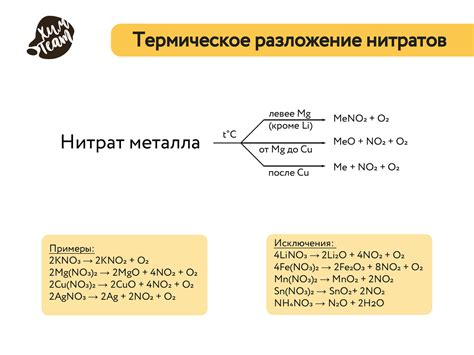
Разложение нитратов металлов является важной реакцией в синтезе различных материалов. Это процесс, при котором нитратные соединения металлов распадаются на оксиды и/или кислород. Применение этой реакции позволяет получать различные материалы с заданными свойствами и структурой.
Одним из основных применений разложения нитратов металлов является получение металлических оксидов. Например, разложение нитрата железа(III) позволяет получить оксид железа(III), который широко используется в производстве магнитов, катализаторов, электродов и других материалов.
Разложение нитратов металлов также применяется в синтезе катализаторов. Нитраты содержат кислород, который может служить как активный компонент катализатора. При разложении нитратов металлов образуются оксиды, которые встраиваются в структуру катализатора и обеспечивают его активность и селективность в различных химических реакциях.
Кроме того, разложение нитратов металлов может быть использовано для получения наночастиц металлов или их оксидов. Это связано с тем, что разложение нитратов металлов происходит при относительно низких температурах, что позволяет избежать слипания и агрегации частиц при синтезе. Таким образом, разложение нитратов металлов является эффективным методом получения наноматериалов с контролируемыми размерами и формой.
Роль разложения нитратов металлов в процессе очистки воды

Разложение нитратов металлов является важной стадией процесса очистки воды от загрязнений. Этот процесс основан на способности нитратов металлов к разложению вредных соединений, таких как аммонийные соединения, которые могут быть образованы в результате разложения органического вещества.
Разложение нитратов металлов происходит в несколько этапов. Сперва нитраты превращаются в нитриты, а затем нитриты окисляются до азота и аммиака. Этот процесс осуществляется при участии бактерий, которые обитают в водной среде. Бактерии, известные как денитрификанты, способны эффективно разлагать нитраты металлов, что способствует очистке воды.
Разложение нитратов металлов имеет большое значение для поддержания экологического баланса в водных средах. Высокая концентрация нитратов может вызывать проблемы для водных организмов, так как они могут стать источником токсинов, которые могут негативно влиять на жизнь и развитие организмов. Поэтому процесс разложения нитратов металлов является важным этапом в процессе очистки воды, так как он обеспечивает сохранение жизни в водных экосистемах.
Перспективы исследований разложения нитратов металлов
Исследования в области разложения нитратов металлов предоставляют широкий спектр перспектив для различных областей науки и технологий. Одним из главных направлений исследований является разработка эффективных методов и катализаторов, позволяющих осуществлять разложение нитратов металлов с высокой скоростью и высокой степенью выбора. Благодаря этому можно получить различные продукты разложения, которые могут быть использованы в разных отраслях промышленности.
Одной из перспектив исследований является поиск катализаторов, обладающих высокой активностью и стабильностью в различных условиях. Такие катализаторы позволят проводить разложение нитратов металлов как в жидкой, так и в газовой фазе при разных температурах и давлениях. Таким образом, можно создать гибкую и эффективную систему, позволяющую обрабатывать разные типы отходов, содержащих нитраты металлов.
Еще одной перспективой исследований является изучение механизма разложения нитратов металлов. Понимание всех этапов этого процесса позволит рационально проектировать и оптимизировать катализаторы и условия реакции разложения. Кроме того, изучение механизма разложения нитратов металлов может способствовать разработке новых методов синтеза и отделения ценных продуктов, получаемых в результате данной реакции.
Применение результатов исследований в области разложения нитратов металлов имеет широкие перспективы в разных областях науки и промышленности. Например, продукты разложения нитратов металлов могут использоваться в железнодорожной и авиационной промышленности в качестве покрытий и топлива. Также они могут быть использованы в производстве катализаторов и электродов для различных электрохимических процессов и устройств. Это открывает новые возможности для создания энергоэффективных и экологически чистых технологий.
Вопрос-ответ

Что такое разложение нитратов металлов?
Разложение нитратов металлов - это процесс, при котором нитраты металлов разлагаются на оксиды или оксиды и кислород. Этот процесс происходит под воздействием различных факторов, таких как температура, давление, наличие катализаторов и т. д. Разложение нитратов металлов имеет широкое применение в различных областях, таких как химическая промышленность, аналитическая химия, производство материалов и т. д.
Какие механизмы разложения нитратов металлов существуют?
Существует несколько механизмов разложения нитратов металлов, в зависимости от активности металла. Для активных металлов, таких как калий или натрий, разложение нитратов происходит с выделением кислорода в газообразной форме. Для менее активных металлов, таких как медь или свинец, нитрат может разлагаться на оксид и кислород. Для некоторых металлов, например ртути, нитрат может разлагаться только при наличии катализаторов или при повышенной температуре.
