Разложение карбоната двухвалентного металла является одним из важных процессов в химии. Карбонаты двухвалентных металлов, таких как медь, железо, никель и другие, обладают широким спектром применений, однако при нагревании они разлагаются на соответствующие оксиды и углекислый газ.
Разложение карбоната двухвалентного металла происходит в несколько этапов. При нагревании карбоната, вначале происходит выделение углекислого газа. Это происходит благодаря тому, что при нагревании карбонат распадается на оксид металла и углекислый газ. Углекислый газ отходит в виде пузырьков, а оксид металла остается на месте.
Образование оксида при разложении карбоната двухвалентного металла является важным процессом в химической промышленности. Полученные оксиды могут использоваться в производстве стекла, керамики, электроники и других отраслях. Этот процесс также имеет большое значение в исследованиях и экспериментах, проводимых в химической лаборатории, для получения чистых и стабильных оксидов металлов.
Разложение карбоната двухвалентного металла: образование оксида

Разложение карбоната двухвалентного металла - это химический процесс, в результате которого из карбоната выделяется углекислый газ и образуется соответствующий оксид металла. Этот процесс может происходить как при нагревании карбоната, так и при взаимодействии с кислотами.
Во время разложения карбоната двухвалентного металла, молекула карбоната распадается на ионы металла и карбонат-ион. Карбонат-ион далее реагирует с водой или с кислотой, образуя углекислый газ и протекающий реакцию оксид металла. В результате, образуется оксид металла, который может быть использован в различных отраслях промышленности и научных исследований.
Разложение карбоната двухвалентного металла является эндотермическим процессом, то есть требует энергии для инициации и продолжения реакции. Углекислый газ, выделяющийся во время реакции, может быть использован в различных промышленных процессах или же рассеивается в атмосферу.
Процесс разложения карбоната двухвалентного металла является одной из основных реакций, которая используется в химической промышленности для получения оксида металла. Это важное преобразование позволяет использовать металлы в различных приложениях, начиная от производства керамики до разработки новых материалов для электроники и фотоники.
Механизм разложения карбоната двухвалентного металла

Разложение карбонатов двухвалентных металлов – это процесс, при котором карбонат превращается в оксид этого металла при нагревании. Этот процесс осуществляется в несколько этапов.
Первым этапом разложения является отщепление молекулярной воды, которая присутствует в составе карбоната. При нагревании карбоната двухвалентного металла до определенной температуры молекулы воды начинают распадаться на атомы водорода и кислорода.
На следующем этапе происходит разложение карбонатной группы (CO₃²⁻) с образованием оксида металла и выделением углекислого газа (CO₂). Молекулы углекислого газа высвобождаются из решетки карбоната в виде газообразного продукта.
Финальным этапом является образование оксида металла. Когда карбонатная группа распадается, формируются два новых компонента: металлический катион и кислород. Кислород занимает место, ранее занятое карбонатной группой, и образует оксид металла.
Таким образом, разложение карбоната двухвалентного металла в результате нагревания происходит поэтапно: отщепление молекулярной воды, разложение карбонатной группы и образование оксида металла. Этот механизм разложения является важным для понимания процессов в химических реакциях и применяется в различных областях науки и промышленности.
Факторы, влияющие на скорость разложения карбоната двухвалентного металла
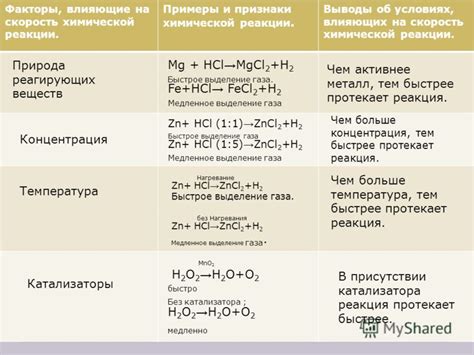
Скорость разложения карбоната двухвалентного металла может быть существенно повлияна несколькими факторами, которые важно учитывать при проведении соответствующих экспериментов.
1. Температура: Один из основных факторов, влияющих на скорость разложения карбоната двухвалентного металла, – это температура реакционной среды. Обычно с увеличением температуры скорость реакции увеличивается, так как увеличивается энергия в системе, что позволяет более эффективно протекать химическим реакциям. Однако, в зависимости от конкретного металла и условий реакции, может быть оптимальная температура, при которой скорость разложения будет максимальной.
2. Размер и форма частиц: Размер и форма частиц карбоната двухвалентного металла также могут оказывать существенное влияние на скорость его разложения. Более мелкие частицы имеют большую площадь поверхности, что увеличивает контактные возможности с реагентами и способствует более быстрому разложению. Также форма частиц может влиять на доступность активных центров, что может также повлиять на скорость реакции.
3. Концентрация реагентов: Концентрация реагентов является еще одним важным фактором, влияющим на скорость разложения карбоната двухвалентного металла. Высокая концентрация реагентов может привести к большему количеству столкновений между молекулами, что повышает вероятность успешных реакций и ускоряет процесс разложения. Однако, также следует учитывать, что слишком высокая концентрация может приводить к насыщению реакционной среды, что может замедлить реакцию из-за наличия большого количества неактивных частиц.
4. Наличие катализаторов: Наличие катализаторов может значительно увеличить скорость разложения карбоната двухвалентного металла. Катализаторы, как правило, снижают энергию активации реакции и ускоряют процесс разложения карбоната. Они могут быть в виде специальных веществ или добавок, которые стимулируют реакцию и увеличивают скорость разложения.
5. Реакционная среда: Кроме того, состав и свойства реакционной среды могут существенно повлиять на скорость разложения. Например, кислотная среда или наличие определенных ионов может активировать реакцию и увеличить скорость разложения карбоната двухвалентного металла.
Все эти факторы следует учитывать при планировании и проведении экспериментов по разложению карбоната двухвалентного металла, так как они могут существенно повлиять на скорость и результаты реакции. Детальное изучение и контроль этих факторов поможет получить более точные и надежные результаты и более полно понять механизмы и закономерности разложения карбоната двухвалентного металла.
Химический состав образующегося оксида при разложении карбоната двухвалентного металла

Разложение карбоната двухвалентного металла является химической реакцией, при которой из карбоната образуется оксид. Химический состав образующегося оксида зависит от конкретного металла, что определяет его физические и химические свойства.
При разложении карбоната двухвалентного металла, такого как медь (CuCO3), образуется оксид меди (CuO). Оксид меди является черным кристаллическим веществом, которое обладает полупроводниковыми свойствами. Он имеет высокую температуру плавления и высокую теплопроводность.
Оксид меди обладает твердыми и хрупкими свойствами, а также химической инертностью. Он не растворяется в воде и слабых кислотах, но может растворяться в сильных кислотах и аммиаке. Оксид меди является важным компонентом в производстве медных сплавов, электрических проводов и полупроводниковых приборов.
Помимо меди, карбонаты двухвалентных металлов, таких как цинк (ZnCO3) и свинец (PbCO3), также разлагаются при нагревании, образуя соответствующие оксиды. Оксид цинка (ZnO) является белым порошком, используемым в производстве резин, керамики и косметики. Оксид свинца (PbO) является желтоватым порошком, применяемым в производстве стекла, красок и аккумуляторов.
Таким образом, химический состав образующегося оксида при разложении карбоната двухвалентного металла зависит от самого металла и имеет важные применения в различных отраслях промышленности.
Влияние температуры на разложение карбоната двухвалентного металла

Температура является одним из основных факторов, влияющих на протекание реакции разложения карбоната двухвалентного металла и образование соответствующего оксида. Изменение температуры может значительно влиять на скорость и полноту процесса разложения.
При повышении температуры происходит увеличение скорости разложения карбоната двухвалентного металла. Это объясняется более активным движением молекул и увеличением энергии их коллизий. Большая энергия коллизий приводит к нарушению связей между атомами карбоната и образованию оксида, что ускоряет реакцию.
Однако, при очень высоких температурах процесс разложения карбоната двухвалентного металла может протекать не полностью из-за обратной реакции, при которой оксид может диссоциировать и образовывать карбонат. Также высокая температура может вызвать дополнительные реакции с окружающей средой, что может оказать влияние на химические свойства образующегося оксида.
Изучение влияния температуры на разложение карбоната двухвалентного металла позволяет определить оптимальные условия для синтеза оксидов с нужными физическими и химическими свойствами. Контроль температуры в процессе разложения может быть важным фактором, позволяющим управлять структурой и кристаллической формой образующегося оксида.
Таким образом, при изучении разложения карбоната двухвалентного металла и образования соответствующего оксида, температура играет решающую роль. Варьирование температуры позволяет контролировать скорость реакции и степень разложения, что важно для создания материалов с определенными свойствами.
Практическое применение разложения карбоната двухвалентного металла для получения оксида

Разложение карбоната двухвалентного металла - это химическая реакция, при которой из карбоната двухвалентного металла образуется соответствующий оксид и выделяется углекислый газ. Эта реакция имеет широкое практическое применение в разных областях науки и промышленности.
Процесс разложения карбоната двухвалентного металла используется в производстве различных оксидов. Например, разложение карбоната кальция (CaCO3) приводит к образованию оксида кальция (CaO). Оксид кальция используется в строительной отрасли для производства цемента и извести, а также в металлургии для удаления примесей из руды.
Другой пример - разложение карбоната меди (CuCO3) приводит к образованию оксида меди (CuO). Оксид меди используется в электронике, для производства солнечных панелей, керамики, пигментов и других материалов.
Процесс разложения карбоната двухвалентного металла также находит применение в аналитической химии. Он используется для определения содержания определенного металла в образце. Путем разложения карбоната металла и получения оксида можно определить массовую долю этого металла в исследуемом образце.
В заключение, разложение карбоната двухвалентного металла для получения оксида имеет множество практических применений. Это важная химическая реакция, которая используется в разных отраслях науки и промышленности для производства оксидов, а также для аналитического определения содержания металлов в образцах.
Вопрос-ответ

Какое вещество образуется при разложении карбоната двухвалентного металла?
При разложении карбоната двухвалентного металла образуется оксид этого металла.
Как происходит разложение карбоната двухвалентного металла?
Разложение карбоната двухвалентного металла происходит при нагревании вещества, при этом из карбоната выделяется углекислый газ, а образуется оксид металла.
