Распознавание соединений металлов является важной задачей в химической аналитике. Одним из таких соединений является сульфат магния (MgSO4) – бинарное химическое соединение металла магния и группы сульфата. Его свойства и реакции активно изучаются в химии, а его распознавание может быть полезным в различных приложениях. Еще одним соединением, которое часто связывают с MgSO4, является гидроксид натрия (NaOH) - щелочное соединение металла натрия и группы гидроксида.
Основным аспектом распознавания соединений MgSO4 и NaOH является их реакция с различными реактивами. Например, встречая NaOH, можно применить реакцию образования гидроксида магния (Mg(OH)2) и хлорида натрия (NaCl). Реакция между MgSO4 и NaOH может привести к образованию гидроксида магния и сульфата натрия (Na2SO4). Такие реакции могут быть использованы для идентификации и распознавания данных соединений.
Применение распознавания соединений MgSO4 и NaOH широко встречается в различных областях науки и промышленности. Например, в медицине и фармакологии этот процесс может использоваться для анализа проб мочи или крови на наличие магния или натрия. В промышленности данный процесс может быть полезен для контроля качества продуктов, содержащих эти металлы, или для идентификации загрязнения в воде или почве.
Основные аспекты
Распознавание соединений металлов MgSO4 и NaOH является важным процессом в химической лаборатории. Эти соединения имеют применение в различных сферах, таких как медицина, сельское хозяйство и промышленность.
Магнийсульфат (MgSO4) является бесцветным соединением, которое обладает множеством полезных свойств. Оно широко используется в медицине для лечения простудных заболеваний, мышечных спазмов и отеков. Также магнийсульфат применяется в качестве компонента питательных сред для растений в сельском хозяйстве.
Гидроксид натрия (NaOH) представляет собой белый порошок или хлопья, популярно известный как "прачечная сода". Он обладает сильными щелочными свойствами и широко используется в промышленности для производства мыла, стекла и бумаги. Кроме того, гидроксид натрия является важным ингредиентом в процессе очистки воды и в производстве пищевых продуктов.
Распознавание соединений металлов MgSO4 и NaOH может быть осуществлено с помощью различных методов, включая химические реакции, физическую характеристику и спектроскопические методы. Это позволяет определить наличие и концентрацию этих соединений в образцах и провести детальный анализ их свойств.
В целом, распознавание соединений металлов MgSO4 и NaOH является важным этапом в химическом анализе и имеет широкое применение в различных областях науки и промышленности.
Химический состав соединений
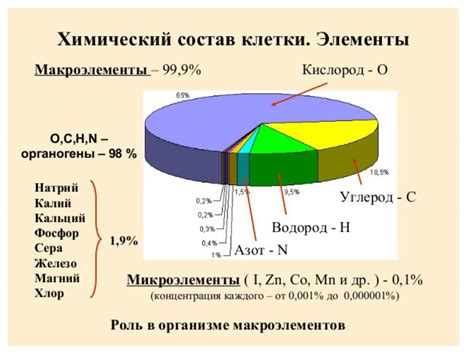
Магнийсульфат (MgSO4) – это бинарное неорганическое соединение, состоящее из атомов магния (Mg), серы (S) и кислорода (O). Оно является солью, образующей кристаллы, которые легко растворяются в воде. Химическая формула магнийсульфата указывает на то, что в каждом молекуле соединения присутствуют один атом магния, один атом серы и четыре атома кислорода.
Гидроксид натрия (NaOH) – это также бинарное неорганическое соединение, состоящее из атомов натрия (Na), кислорода (O) и водорода (H). Оно является сильным основанием, широко используется в различных отраслях промышленности. Химическая формула гидроксида натрия указывает на наличие одного атома натрия, одного атома кислорода и одного атома водорода в каждой молекуле соединения.
При реакции между магнийсульфатом и гидроксидом натрия происходит ионный обмен, в результате которого образуются новые соединения. Водные растворы магнийсульфата и гидроксида натрия содержат ионы магния (Mg2+), серы (SO4^2-) и натрия (Na+). При ионном обмене ионы гидроксида натрия соединяются с ионами магния, образуя осадок гидроксида магния (Mg(OH)2), а ионы натрия реагируют с ионами серы, образуя нерастворимый осадок сульфата натрия (Na2SO4).
Физические свойства

Магнийсульфат (MgSO4) - бесцветные кристаллы или порошок с характерным горьким вкусом. В природе обычно находится в виде гидратов, наиболее распространенный из которых - гексагидрат. Магнийсульфат хорошо растворяется в воде, не растворяется в спирте и эфире. Когда растворяется в воде, образует ди - и шестиводные соединения с молекулами воды.
Гидроксид натрия (NaOH) - белые кристаллические гранулы или хлопья сильного щелочного запаха. Нерастворим в спирте и эфире, хорошо растворяется в воде, при этом происходит выделение тепла. Раствор гидроксида натрия является сильным основанием.
Смесь магнийсульфата и гидроксида натрия обладает следующими физическими свойствами. Она образует белый осадок, который постепенно выпадает из раствора при взаимодействии двух соединений. Осадок является хорошо растворимым в воде и имеет щелочную реакцию. Вещество не растворимо в спирте и эфире. Кроме того, смесь обладает белоснежным цветом и химическим запахом.
Химические свойства

Магнийсульфат (MgSO4) является солью, обладающей рядом химических свойств. При взаимодействии с гидроксидом натрия (NaOH) происходит химическая реакция, в результате которой образуется осадок белого цвета.
Реакция между магнийсульфатом и гидроксидом натрия является двойной заменой. Гидроксид натрия расщепляется на катионы натрия (Na+) и гидроксидные анионы (OH^-), а магнийсульфат расщепляется на катионы магния (Mg2+) и сульфатные анионы (SO4^2-). В результате образуются новые соли: натрийсульфат (Na2SO4) и магнийгидроксид (Mg(OH)2).
Осадок магнийгидроксида обладает щелочными свойствами и может использоваться в качестве антацида для снижения кислотности желудочного сока при избыточном пищеварении. Магнийгидроксид образует слабоскорректирующую щелочь, которая нейтрализует избыток соляной кислоты в желудке и уменьшает симптомы изжоги. Также он может применяться в качестве слабительного.
Магнийсульфат и гидроксид натрия являются широко используемыми химическими соединениями, как ингредиенты в производстве лекарственных препаратов, удобрений, косметических средств и др. Их свойства и возможные реакции активно изучаются в химических исследованиях.
Процесс распознавания
Процесс распознавания соединений металлов MgSO4 и NaOH происходит путем проведения химической реакции между этими веществами. В ходе этой реакции происходит образование новых веществ с характерными свойствами, которые можно определить и идентифицировать.
Основным методом распознавания соединений является наблюдение за изменениями внешнего вида образовавшихся веществ. Например, при взаимодействии между MgSO4 и NaOH образуется осадок белого цвета, который можно визуально определить.
Также в процессе распознавания может использоваться анализ химических свойств и реакций образовавшихся веществ. Например, проведение реакции образовавшегося осадка с кислородом или серной кислотой позволяет определить его состав и тип соединения.
Важным аспектом процесса распознавания является использование специального оборудования и химических реактивов, которые позволяют провести точный и надежный анализ. Для определения химических свойств веществ могут использоваться такие методы, как титрование, спектральный анализ, хроматография и другие.
Применение распознавания соединений металлов MgSO4 и NaOH широко распространено в различных областях науки и промышленности. Например, в химической промышленности это может быть использовано для контроля качества продукции или определения содержания различных веществ. В медицине и биологии такие исследования помогают выявить наличие или отсутствие определенных элементов в организмах или образцах.
Применение

Распознавание соединений металлов MgSO4 и NaOH имеет широкий спектр применения в различных областях научных и технических исследований, а также в промышленности.
В химической аналитике распознавание этих соединений часто используется для определения содержания магния и серы в различных образцах. Это позволяет контролировать качество продукции и проводить анализы состава материалов.
Благодаря высокой реакционной способности магния и натрия с серной кислотой и щелочью соответственно, распознавание соединений MgSO4 и NaOH применяется в сельском хозяйстве для удобрения почвы и корректировки ее кислотности. Магний является важным макроэлементом для растений, а натрий играет роль буфера уровня pH.
Кроме того, распознавание соединений металлов MgSO4 и NaOH нашло применение в медицине. Магнийсодержащие препараты на основе MgSO4 используются для профилактики и лечения некоторых заболеваний, в том числе гипомагниемии и преэклампсии у беременных женщин. Натрий, в свою очередь, является неотъемлемой частью физиологических растворов, используемых для восстановления электролитного баланса в организме.
Вопрос-ответ

Какие основные аспекты распознавания соединений металлов MgSO4 и NaOH стоит учитывать?
Основные аспекты распознавания соединений металлов MgSO4 и NaOH включают в себя определение идентичности элементов, анализ химических свойств и реакций данных соединений, а также практическое применение полученных результатов.
Какие методы можно использовать для распознавания соединений металлов MgSO4 и NaOH?
Для распознавания соединений металлов MgSO4 и NaOH можно использовать различные методы анализа, такие как спектральный анализ, хроматография, электрохимический анализ и другие. В зависимости от конкретной цели исследования можно выбрать наиболее подходящий метод.
Какое практическое применение имеют результаты распознавания соединений металлов MgSO4 и NaOH?
Результаты распознавания соединений металлов MgSO4 и NaOH имеют широкий спектр практического применения. Например, полученные данные могут быть использованы в медицинской, фармацевтической и пищевой промышленности для контроля качества, в научных исследованиях, а также при производстве различных химических веществ и материалов.
Какие химические свойства имеют соединения металлов MgSO4 и NaOH?
Соединение металла MgSO4 (сульфат магния) обладает растворительными свойствами, образуя растворимые соли. Соединение металла NaOH (гидроксид натрия) также обладает растворительными свойствами и, кроме того, является сильным основанием. Оба соединения могут участвовать в химических реакциях с другими веществами, образуя новые продукты.
