Радиус элементов – это один из основных параметров, описывающих строение и свойства химических элементов. Этот параметр важен для понимания структуры атома, его электронной оболочки и способности взаимодействовать с другими атомами. В данной статье рассмотрим разницу в радиусе элементов между металлами и неметаллами.
Металлы – это класс элементов, обладающих свойствами, такими как гибкость, тепло- и электропроводность, блеск и высокая плотность. Важным свойством металлов является их большой атомный радиус, который определяется размерами атомной оболочки и количеством электронов в ней. Металлы, как правило, имеют больший радиус по сравнению с неметаллами, что обусловлено особенностями строения атома и его электронной оболочки.
Неметаллы, напротив, обладают совершенно другими свойствами, такими как хрупкость, низкая плотность и отсутствие блеска. Атомный радиус неметаллов меньше по сравнению с радиусом металлов. Это связано с тем, что неметаллы имеют меньшую атомную оболочку и количество электронов в ней. Кроме того, строение атома неметалла обусловливает его способность принимать электроны от других атомов, что влияет на радиус элемента.
Итак, радиус элементов имеет важное значение при изучении и понимании их свойств и взаимодействий. Металлы имеют больший атомный радиус, что определяет их способность к проводимости тепла и электричества, а также гибкость. Неметаллы, в свою очередь, имеют меньший радиус и обладают другими специфическими свойствами, такими как кристаллическая структура и хрупкость.
Металлы с разным радиусом элементов: как они отличаются от неметаллов
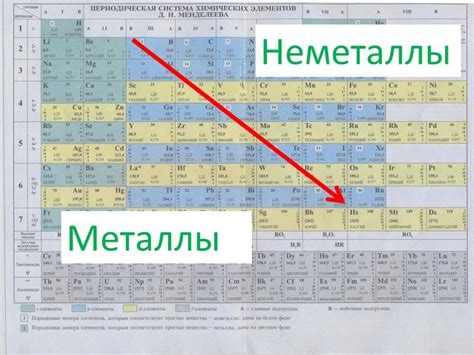
Металлы и неметаллы — основные типы элементов в периодической таблице химических элементов. Хотя оба класса включают различные элементы, металлы и неметаллы имеют существенные различия во многих аспектах, включая радиус своих атомов.
Металлы обычно имеют больший радиус атомов по сравнению с неметаллами. Это объясняется тем, что металлы обладают меньшим количеством электронов в своей внешней оболочке, что позволяет атомам металлов быть более расположенными и свободными, увеличивая их радиус. Например, натрий и калий, два металлических элемента, имеют значительно больший атомный радиус по сравнению с хлором, неметаллическим элементом.
Разница в радиусе атомов металлов и неметаллов также связана с их положением в периодической таблице. Металлы находятся слева от ступенчатой линии в таблице, где находятся неметаллы. Ступенчатая линия представляет собой границу между металлами и неметаллами и разделяет их свойства, включая радиусы атомов.
Однако радиус атома не является единственным фактором, отличающим металлы от неметаллов. Металлы также обладают высокой теплопроводностью и электропроводностью, хорошей деформируемостью и нередко образуют положительные ионы. В то время как неметаллы, как правило, выступают в качестве непроводников тепла и электричества, имеют отрицательные ионы и обычно образуют ковалентные связи.
В заключение, металлы и неметаллы отличаются не только радиусом своих атомов, но и другими физическими и химическими свойствами. Различный радиус атомов металлов и неметаллов объясняется количеством электронов в их внешней оболочке и их положением в периодической таблице химических элементов.
Металлы: особенности и свойства

Металлы - это группа химических элементов, которые обладают рядом характерных особенностей и свойств. Они являются отличными проводниками электричества и тепла, что делает их незаменимыми материалами во многих отраслях промышленности и техники.
Металлы обладают высокой пластичностью и прочностью, что позволяет их легко подвергать различным видам обработки, включая литье, ковку, прокатку и тяжение. Это делает возможным создание разнообразных форм и конструкций из металлов, а также их использование в строительстве и производстве механизмов.
Одной из характерных особенностей металлов является их способность образовывать ионные соединения с неметаллами, что позволяет им образовывать соли и совершать химические реакции. Однако, не все металлы схожи по своим химическим свойствам, они различаются по реактивности и способности к окислению.
Еще одним важным свойством металлов является их способность образовывать сплавы с другими металлами, что позволяет расширять их применение и получать материалы с новыми свойствами. Сплавы можно получать путем плавления и смешивания металлов в определенных пропорциях.
Металлы имеют широкий диапазон плавления и кипения, а также различные степени магнитной проницаемости. Они обладают высокой плотностью и являются тяжелыми материалами. Некоторые металлы также отличаются особым блеском и цветом, что делает их привлекательными для использования в ювелирном искусстве.
Все эти свойства делают металлы важными материалами для различных сфер жизни человека. Они находят широкое применение в производстве машиностроительных изделий, электроники, автомобилей, строительных материалов и многого другого.
Неметаллы: основные характеристики и признаки

Неметаллы - это класс элементов химической системы, которые обладают рядом характеристик и признаков, отличных от металлов. Они играют важную роль в химии и имеют большое значение в разных сферах жизни, включая промышленность, энергетику и медицину.
Основной признак неметаллов - это их электроотрицательность, которая гораздо выше, чем у металлов. Электроотрицательность влияет на химические свойства неметаллов, такие как способность принимать или отдавать электроны, образование ковалентных связей, а также ионизационные свойства.
Неметаллы обладают жидким или газообразным агрегатным состоянием при комнатной температуре и давлении, хотя есть и такие, которые могут быть твердыми. Они обычно имеют низкую плотность и температуру плавления, а также не обладают характерной металлической блеской.
Общие химические свойства неметаллов включают их способность образовывать связи с металлами и другими неметаллами, образовывать кислоты и основания, а также участвовать в окислительно-восстановительных реакциях. Некоторые неметаллы могут быть токсичными и вредными для организмов живых существ.
Неметаллы присутствуют в периодической системе химических элементов, их количество и разнообразие помогают удовлетворить жизненно важные потребности человека. Они используются в производстве пластмасс, лекарственных препаратах, углеродных материалах, электронике, косметической промышленности, пищевой промышленности и многих других областях науки и техники.
Радиус металлов: влияние на физические и химические свойства
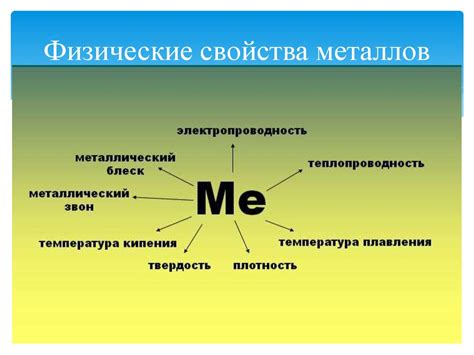
Радиус металлов играет существенную роль в определении их физических и химических свойств. Понимание и контроль этого параметра позволяет улучшить характеристики материалов и применять их в различных областях науки и промышленности.
Физические свойства металлов, такие как плавление, кипение, плотность и теплопроводность, зависят от их атомного радиуса. Большой радиус металла позволяет атомам свободно двигаться и образовывать кристаллическую решётку. Это обеспечивает высокую плотность и теплопроводность, что делает металлы эффективными материалами для передачи энергии и тепла.
Кроме того, радиус атомов металлов влияет на их химическую активность. Маленький радиус увеличивает плотность зарядов в атоме, что делает его более склонным к электронной деформации и реакции с другими веществами. Металлы с большим радиусом, наоборот, обладают меньшей химической активностью и могут быть более устойчивыми к окислению и коррозии.
Изучение и контроль радиуса металлов позволяет улучшить их свойства и разработать новые материалы с оптимальными характеристиками. Например, уменьшение атомного радиуса позволяет создать легкие и прочные металлические сплавы, которые могут использоваться в авиации и автомобилестроении. Также, модификация радиуса атомов может влиять на их ферромагнитные свойства, что открывает новые перспективы в области магнитных материалов и электроники.
Радиус неметаллов: взаимосвязь с электронной структурой и реакционной способностью

Радиус неметаллов является важным параметром, который характеризует размеры атома данного элемента. Размеры атома оказывают влияние на его электронную структуру, а также на реакционную способность элемента. Взаимосвязь между радиусом неметаллов и их свойствами может быть объяснена на основе их электронной конфигурации и химической активности.
Электронная структура атома неметалла определяется расположением электронов в его энергетических оболочках. Чем больше радиус атома неметалла, тем больше места для размещения электронов в энергетических оболочках, что позволяет атому иметь большее количество электронов и, следовательно, большую электроотрицательность. Большая электроотрицательность делает неметаллы способными к образованию ковалентных связей.
Реакционная способность неметаллов также зависит от их радиусов. Радиус неметаллов, как правило, увеличивается вдоль периодической таблицы, что связано с увеличением числа электронов в энергетических оболочках. Это влияет на процессы взаимодействия неметалла с другими веществами. Больший радиус позволяет неметаллам формировать более слабые и дальние связи с другими элементами, что делает их более реакционноспособными.
Особую роль играет электроотрицательность неметаллов, которая определяется их радиусами и электронной структурой. Высокая электроотрицательность неметалла свидетельствует о его способности притягивать электроны к себе. Это позволяет неметаллам легко образовывать ионные и ковалентные связи с другими веществами. Малые радиусы неметаллов способствуют более плотной электронной оболочке, что усиливает их химическую активность и реакционную способность.
Вопрос-ответ

Какие элементы являются металлами?
Металлами в таблице Менделеева являются элементы, расположенные в левой части таблицы. Они обладают характерными свойствами: высокой электропроводностью, теплопроводностью, металлическим блеском и возможностью формировать положительные ионы.
Какие элементы являются неметаллами?
Неметаллады представлены элементами, которые находятся в правой части таблицы Менделеева, за исключением газового галогена ибрида. Они имеют низкую электропроводность, их часто применяют в производстве изолирующих материалов или смол.
