Размер атома является одним из важных характеристик элементов, определяющих их химические и физические свойства. Одним из наиболее интересующих вопросов является определение того, какие элементы имеют меньший радиус - металлы или неметаллы?
Металлы и неметаллы - две основные группы элементов в периодической системе. Металлы, как правило, имеют положительный заряд и высокую электропроводность, в то время как неметаллы обладают отрицательным зарядом и низкой электропроводностью. Такие различия в свойствах между металлами и неметаллами частично обусловлены их атомными радиусами.
Атомный радиус - это расстояние от ядра атома до его электронной оболочки. Исследования показывают, что в целом металлы имеют большие атомные радиусы по сравнению с неметаллами. Это связано с тем, что металлы обычно имеют малое количество электронов на своей последней энергетической оболочке, что позволяет им "расширяться" и занимать больше пространства.
Размер атома: понятие и важность изучения
Размер атома - это важный физический параметр, который определяет геометрические характеристики атома. Он является фундаментальной характеристикой атома и влияет на его свойства и реактивность. Изучение размера атома имеет огромное значение как для теоретической физики, так и для различных областей науки и технологий.
Одним из основных методов изучения размера атома является рентгеноструктурный анализ, который позволяет определить расстояние между атомами в кристаллической решетке. Это позволяет получить информацию о размере атомов вещества и структуре кристаллической решетки. Также размер атома можно оценить с помощью различных спектроскопических методов, таких как спектроскопия рассеяния и эффект Мессбауэра.
Изучение размера атома имеет большое значение для различных научно-прикладных областей. Например, в химии размер атома влияет на химическую активность элементов и возможность образования химических связей. В материаловедении знание размера атома позволяет контролировать структуру и свойства различных материалов, таких как полупроводники, металлы и полимеры. В биологии изучение размера атома имеет значение для понимания структуры биологических молекул и процессов, происходящих в клетке.
Кроме того, изучение размера атома важно для понимания физических явлений. Например, размер атома влияет на оптические свойства вещества, такие как поглощение и рассеяние света. Изменение размера атома также может привести к изменению магнитных и электрических свойств вещества.
В целом, изучение размера атома является важной областью научных исследований, которая позволяет углубить наше понимание принципов строения и свойств вещества. Понимание размера атома имеет огромное практическое значение и может привести к разработке новых материалов и технологий, которые имеют более высокую эффективность и производительность.
Металлы и неметаллы: основные различия

Металлы и неметаллы - это две основные группы элементов в периодической таблице. Они имеют некоторые особенности, отличающие их друг от друга.
Металлы обладают следующими характеристиками:
- Высокая теплопроводность и электропроводность.
- Гибкость и пластичность, что позволяет им легко подвергаться обработке.
- Металлические связи между атомами, которые способствуют образованию ионных решеток.
- Гладкая, блестящая поверхность.
- Обычно твердые при комнатной температуре, за исключением ртути.
Неметаллы, в свою очередь, отличаются следующими свойствами:
- Низкая или отсутствующая электропроводность.
- Обычно хрупкие и не пластичные.
- Атомы неметаллов образуют ковалентные связи.
- Поверхность может быть матовой и непроводящей.
- Неметаллы могут быть различных состояний при комнатной температуре: газы (например, кислород), жидкости (например, бром) или твердые вещества (например, уголь).
Общим свойством металлов и неметаллов является то, что они играют важную роль в химических реакциях и находят широкое применение в различных отраслях науки и промышленности.
Размер атома металлов: факты и теории

Радиус атома - это важная характеристика атома и один из его основных параметров. Представим атом как сферу, радиус которой показывает, насколько далеко могут располагаться его электроны от ядра. Размер атома зависит от нескольких факторов, включая количество электронов, ядерный заряд и электронную конфигурацию.
Металлы - это элементы, у которых электронная оболочка частично заполняется электронами, что делает их хорошими проводниками тепла и электричества. Одним из фундаментальных свойств металлов является их большой размер атомов. Металлы обычно имеют больший радиус атома по сравнению с неметаллами.
Существует несколько теорий, объясняющих больший размер атомов металлов. Одна из таких теорий - теория металлической связи. Согласно этой теории, металлы имеют свободный электронный газ, который образуется из валентных электронов. Этот свободный электронный газ помогает "раздувать" атом, увеличивая его радиус.
Другая теория, объясняющая большой размер атомов металлов, - теория положительного ядра. Согласно этой теории, атомы металлов имеют сильно положительно заряженное ядро, что приводит к их большим размерам. Таким образом, металлы имеют больший эффективный ядерный заряд, который притягивает электроны и удерживает их ближе к ядру, что увеличивает радиус атома.
В целом, металлы характеризуются большим размером атома по сравнению с неметаллами. Это объясняется особенностями электронной структуры и теориями, такими как теория металлической связи и теория положительного ядра.
Факторы, влияющие на размер атома металлов

1. Энергия газообразного атома: Металлы имеют низкую энергию газообразного атома из-за таких факторов, как слабое ограничение электронов и большая эффективность экранирования ядра. Это приводит к уменьшению притяжения электронов к ядру и, следовательно, к увеличению радиуса атома.
2. Количество электронных слоев: Металлы имеют большое количество электронных слоев, что приводит к увеличению размера атома. Каждый новый электронный слой добавляет радиус атома.
3. Заряд ядра: Заряд ядра металла определяет силу притяжения электронов к ядру. Чем больше заряд ядра, тем сильнее притяжение и меньший радиус атома.
4. Экранирование электронов: Металлы имеют много электронов, которые экранируют друг друга от притяжения ядра. Это приводит к увеличению размера атома, так как притяжение электронов к ядру снижается.
5. Химическая связь: Металлы образуют металлическую связь, в которой электроны свободно двигаются между атомами. Это приводит к увеличению размера атома, так как электроны между атомами распределяются равномерно.
6. Периодическая система: Размер атома металлов увеличивается при движении вниз по группе в периодической системе элементов. Это связано с добавлением новых электронных слоев и увеличением экранирования электронов.
В итоге, комплексное воздействие этих факторов определяет размер атома металлов, который в целом больше, чем у неметаллов.
Размер атома неметаллов: особенности и исследования
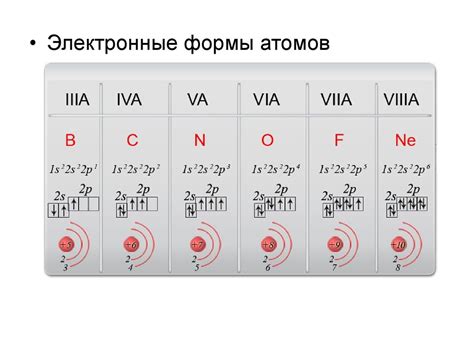
Размер атома является одним из важных характеристик химических элементов, влияющих на их физические и химические свойства. Неметаллы, как класс элементов, обладают своими особенностями и уникальными значениями радиуса своих атомов.
Изучение размера атомов неметаллов осуществляется с помощью различных экспериментальных методов, включая рентгеноструктурный анализ и измерение интератомных расстояний. Одним из применяемых методов является также использование электронных микроскопов, позволяющих получить более подробные данные о структуре атомов.
Радиусы атомов неметаллов обычно меньше, чем радиусы металлов. Это связано с особенностями строения атомной структуры неметаллов. Неметаллические элементы образуют ковалентные связи, в которых атомы разделяют электроны, образуя молекулы. Это приводит к сжатию атомов и уменьшению радиуса.
Кроме того, у неметаллов также есть свойство притягивать к себе электроны, образуя отрицательные ионы. Это также может влиять на размер атома неметаллов. Радиус атома у неметаллов может различаться в зависимости от ионизационного состояния элемента.
В целом, изучение размера атомов неметаллов играет важную роль в понимании их химических и физических свойств. Знание размера атомов позволяет установить взаимодействие элементов между собой, а также предсказать и объяснить реакционную способность неметаллов в различных химических процессах.
Влияние электроотрицательности на радиус неметаллов

Радиус атома неметаллов в значительной степени зависит от их электроотрицательности. Электроотрицательность - это способность атома притягивать к себе электроны. Чем выше электроотрицательность атома, тем сильнее он притягивает свои электроны и, следовательно, меньше его радиус.
Неметаллы, обладающие высокой электроотрицательностью, такие как фтор и кислород, имеют очень маленький радиус. Их маленький радиус обусловлен сильным взаимодействием электронных облаков с ядром атома. Притяжение электронов к себе практически не позволяет электронным облакам распространяться далеко от ядра, что приводит к уменьшению радиуса атома.
Высокая электроотрицательность неметаллов также связана с их способностью притягивать электроны при образовании химических связей. Это направленное притяжение электронов позволяет неметаллам образовывать ковалентные связи с другими атомами и создавать стабильные молекулы. Ковалентные связи в неметаллах играют важную роль во многих биологических, физических и химических процессах.
Неметаллы с меньшей электроотрицательностью, такие как сера и фосфор, имеют больший радиус, чем неметаллы с более высокой электроотрицательностью. Это связано с более слабым притяжением своих электронов и, следовательно, большей возможностью электронам находиться на большом расстоянии от ядра.
Малый радиус неметаллов обусловлен их химической активностью. Неметаллы стремятся заполнить свои внешние электронные оболочки путем получения электронов от других атомов. Из-за малого размера атома неметаллы легко проникают в структуры других веществ, что позволяет им проявлять свою высокую реакционность и часто образовывать стабильные химические соединения.
Экспериментальные методы измерения размера атомов

Установление размеров атомов является важной задачей в области химии и физики. Существует несколько экспериментальных методов, которые позволяют определить размеры атомов с высокой точностью.
Один из таких методов - рентгеноструктурный анализ. Этот метод основан на использовании рентгеновских лучей для исследования кристаллической структуры вещества. Путем анализа полученных дифракционных карт можно рассчитать расстояния между атомами и, следовательно, их размеры.
Другой метод - электронная микроскопия. Этот метод позволяет непосредственно наблюдать атомы с помощью электронного луча и детектировать рассеянные электроны. С помощью электронной микроскопии можно измерить расстояние между атомами и получить информацию о их размерах.
Существуют также методы на основе спектроскопии, такие как спектроскопия атомного поглощения и спектроскопия фотоэлектронов. Оба метода позволяют измерить энергию поглощения или эмиссии электронов, что позволяет определить энергетические уровни атомов и их размеры.
Следует отметить, что различные методы измерения размера атомов могут давать немного разные результаты в зависимости от используемых условий и критериев измерения. Однако, с помощью современных экспериментальных методов можно достичь высокой точности при определении размеров атомов металлов и неметаллов.
Вопрос-ответ

В чем заключается разница в размерах атомов металлов и неметаллов?
Разница в размерах атомов металлов и неметаллов обусловлена различными электронными структурами. У металлов внешний электронный слой относительно подвижен и образует общий электронный газ, что делает атомы металлов более крупными по сравнению с атомами неметаллов, у которых электроны внешнего слоя тесно связаны с ядром.
Кто имеет меньший радиус - металлы или неметаллы?
Обычно металлы имеют больший атомный радиус по сравнению с неметаллами. Это связано с тем, что у металлов внешний электронный слой является общим для всех атомов в металлической решетке и образует электронный газ, что делает атомы металлов более крупными.
Почему металлы имеют больший атомный радиус?
Металлы имеют больший атомный радиус из-за специфической структуры их электронных оболочек. У металлов внешний электронный слой является общим для всех атомов в металлической решетке и образует электронный газ, что делает атомы металлов более крупными.
Какой атом имеет меньший размер - металл или неметалл?
В общем случае, атомы неметаллов имеют меньший размер по сравнению с атомами металлов. Это связано с тем, что у неметаллов электроны внешнего слоя тесно связаны с ядром, в отличие от металлов, у которых внешний электронный слой является общим для всех атомов и образует электронный газ.
Влияет ли на размер атома его положение в Периодической системе элементов?
Да, положение атома в Периодической системе элементов влияет на его размер. В периоде размер атома обычно уменьшается с увеличением атомного номера, поскольку количество электронов внешнего слоя увеличивается, азотом активность этих электронов с ядром ослабевает, что делает атомы более компактными.