Щелочные металлы – это элементы первой группы периодической системы, включающие литий, натрий, калий, рубидий, цезий и франций. Одной из основных характеристик атома является его радиус – расстояние от центра атома до его внешней оболочки. Важно отметить, что с ростом порядкового номера щелочных металлов происходит увеличение размеров атома.
Причина увеличения радиуса атома щелочных металлов заключается в изменении электронной конфигурации. Все щелочные металлы имеют один внешний электрон, находящийся в s-орбитали. Порядковый номер атома соответствует числу электронов в атоме. Поэтому с ростом порядкового номера увеличивается количество электронов, занимающих u-s-орбиталь. В результате, электроны начинают занимать все более удаленные от ядра орбитали, что приводит к увеличению общего размера атома.
Увеличение радиуса атома щелочных металлов имеет важные практические последствия. Больший размер атома приводит к увеличению валентности элемента и его активности в реакциях. Щелочные металлы с ростом порядкового номера становятся все более реактивными и реагируют с веществами, с которыми малорадиусные металлы не взаимодействовали бы. Это свойство широко используется в различных сферах науки и техники.
Влияние порядкового номера на размер атома щелочных металлов
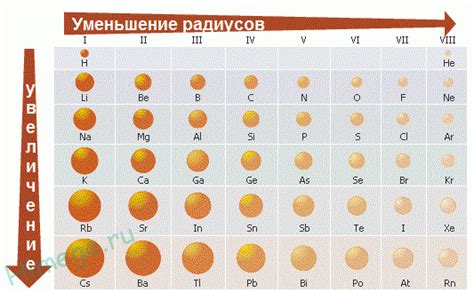
Размер атома щелочных металлов зависит от их порядкового номера в таблице элементов. Щелочные металлы (литий, натрий, калий, рубидий, цезий и франций) имеют общую особенность - с ростом порядкового номера увеличивается радиус их атомов.
Причина этой особенности связана с увеличением количества электронных оболочек и зарядового ядра атома щелочных металлов. С каждым новым элементом в периоде количество электронных оболочек увеличивается на одну, а заряд ядра увеличивается на единицу. Это приводит к возрастанию притяжения электронов к ядру и, как следствие, увеличению размера атома.
Увеличение радиуса атомов щелочных металлов ведет к ряду следствий. Во-первых, увеличивается расстояние между электронами, что способствует более слабому притяжению между ними и, следовательно, более слабым связыванию электронов. Вторым следствием увеличения радиуса атома щелочных металлов является их большая реактивность. Больший радиус облегчает доступ реагентов к активному центру молекулы, что в свою очередь увеличивает скорость химических реакций.
В сводной таблице ниже представлены данные о радиусах атомов щелочных металлов в пикометрах (1 пикометр = 10^-12 метров) с ростом их порядкового номера:
| Щелочный металл | Атомный радиус (пм) |
|---|---|
| Литий | 152 |
| Натрий | 186 |
| Калий | 227 |
| Рубидий | 248 |
| Цезий | 265 |
| Франций | - |
Из таблицы видно, что с ростом порядкового номера радиус атомов щелочных металлов постепенно увеличивается, что подтверждает зависимость размера атома от его порядкового номера.
Краткий обзор щелочных металлов
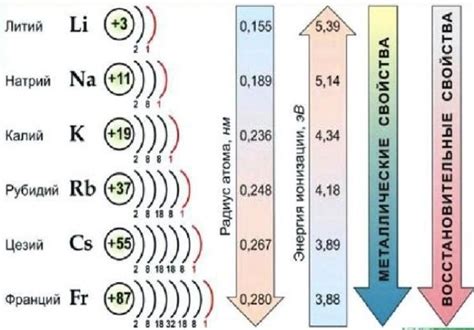
Щелочные металлы – группа элементов, относящихся к первой группе периодической таблицы. К ним относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Эти элементы отличаются низкой температурой плавления, высокой электропроводностью и химической активностью.
Щелочные металлы обладают одной электронной оболочкой, что делает их очень реактивными. Они легко реагируют с водой, воздухом и другими химическими веществами. К примеру, при контакте с водой, щелочные металлы образуют щелочные гидроксиды и выделяются водород.
Очень интересной особенностью щелочных металлов является их способность образовывать сплавы с другими металлами. Такие сплавы обычно обладают низкой температурой плавления, что делает их идеальными для использования в различных областях, таких как аэрокосмическая промышленность и электрическая инженерия.
Каждый следующий щелочный металл имеет больший атомный радиус и меньшую энергию ионизации по сравнению с предыдущими элементами этой группы. Это означает, что с ростом порядкового номера щелочных металлов, их атомы становятся все больше, что обуславливает увеличение радиуса атома.
Тренд увеличения размера с порядковым номером

Проявление тренда увеличения размера радиуса атомов щелочных металлов с ростом их порядкового номера играет важную роль в понимании свойств этих элементов. Увеличение радиуса атома связано с увеличением числа электронных оболочек и электронов в них. Каждый следующий щелочный металл имеет на одну оболочку больше, чем предыдущий, что приводит к увеличению размера атома.
Этот тренд можно наблюдать в таблице Менделеева. Начиная с лития (Li) и заканчивая францием (Fr), радиус атома увеличивается по мере увеличения порядкового номера. Например, калий (K), который имеет порядковый номер 19, имеет больший радиус, чем натрий (Na) с порядковым номером 11. Это объясняется тем, что в атоме калия на одну оболочку больше, чем в атоме натрия.
Увеличение радиуса атома щелочных металлов с порядковым номером влияет на их химические свойства. Большие радиусы атомов позволяют щелочным металлам проявлять активность во взаимодействиях с другими элементами. Это связано с возможностью больших атомов легче потерять один электрон и образовать положительный ион. Важно отметить, что тренд увеличения размера с порядковым номером не является абсолютным правилом и может быть нарушен в некоторых случаях вследствие дополнительных факторов, таких как особенности строения молекулярных оболочек или влияние других элементов.
Объяснение физических факторов
Увеличение радиуса атома щелочных металлов с ростом их порядкового номера обусловлено рядом физических факторов. Во-первых, достижение большего размера связано с увеличением количества электронных оболочек. Каждый следующий элемент в периодической таблице содержит на одну оболочку больше, что приводит к увеличению числа электронов и увеличению размера атома.
Во-вторых, увеличение радиуса атома также связано с эффективностью экранирования электронных оболочек. Чем больше электронных оболочек, тем больше других электронов, которые экранируют внешние оболочки от положительного заряда ядра. Это приводит к уменьшению притягивающей силы между ядром и электронами, и в результате размер атома увеличивается.
Кроме того, влияние на размер атома оказывает также эффективность образования ковалентных связей. В щелочных металлах с ростом порядкового номера увеличивается эффективность образования ковалентных связей, что приводит к более сильному сжатию электронных оболочек и уменьшению радиуса. Но влияние этого фактора оказывается незначительным по сравнению с остальными.
Таким образом, объяснение увеличения радиуса атома щелочных металлов с ростом порядкового номера связано с увеличением электронных оболочек, уменьшением притягивающей силы между ядром и электронами, а также с эффективностью образования ковалентных связей. Все эти факторы в совокупности определяют размер атома щелочных металлов в периодической таблице.
Практическое применение увеличения размера

Увеличение радиуса атома щелочных металлов с ростом их порядкового номера имеет важное практическое значение в различных отраслях науки и промышленности.
1. Энергетика:
Увеличение размера атома позволяет повысить эффективность использования щелочных металлов в энергетической отрасли. Больший размер атома способствует лучшей проходимости электронов в проводнике, что позволяет достичь более высоких значений электропроводности и электронной подвижности. Это делает их идеальным материалом для производства электродов и батарей.
2. Фармацевтика:
Большие атомы щелочных металлов могут образовывать стабильные соединения с различными органическими соединениями. Это свойство используется в фармацевтической промышленности для синтеза и производства лекарственных препаратов. Применение щелочных металлов позволяет увеличить стабильность и эффективность лекарственных соединений, а также улучшить усвоение и распределение препарата в организме.
3. Материаловедение:
Изменение размера атомов щелочных металлов имеет важное значение для разработки новых материалов. Использование щелочных металлов с большими атомами позволяет улучшить механические и термические свойства материалов, а также повысить их стабильность и долговечность. Такие материалы широко применяются в авиационной и космической промышленности, а также в производстве специальных конструкционных и защитных материалов.
4. Научные исследования:
Увеличение размера атомов щелочных металлов также играет важную роль в научных исследованиях. Большие атомы представляют интерес для ученых из-за своей способности образовывать устойчивые соединения и структуры. Это позволяет проводить более сложные эксперименты и изучать различные физические и химические свойства материалов. Практическое применение увеличения размера атома щелочных металлов включает в себя исследования новых материалов, разработку лекарственных препаратов, создание новых энергетических технологий и многие другие области.
Ограничения и недостатки

Увеличение радиуса атома щелочных металлов с ростом их порядкового номера имеет ряд ограничений и недостатков, которые необходимо учитывать при изучении данного явления.
Во-первых, стоит отметить, что увеличение радиуса атома щелочных металлов не является линейным процессом. Такое увеличение происходит по принципу убывания, что может привести к неточности в предсказании радиуса для определенных элементов.
Во-вторых, увеличение радиуса атома щелочных металлов с ростом их порядкового номера может быть ограничено группой добавочных факторов, таких как атомные связи и силы притяжения. В результате, предсказание точных значений радиуса атома может быть затруднительным и требует учета данных о контактной величине и ближайших атомных расстояниях.
Кроме того, соотношение между радиусом атома щелочных металлов и их порядковым номером также не учитывает другие факторы, которые могут влиять на размер атома. Например, влияние электронной структуры, зарядового состояния или валентности элемента может привести к отклонениям от ожидаемых значений радиуса атома.
В целом, несмотря на ограничения и недостатки, увеличение радиуса атома щелочных металлов с ростом их порядкового номера остается важным явлением для изучения и понимания химических свойств этих элементов. Результаты исследований в этой области могут иметь широкий практический применение в различных отраслях наук и технологий, от материаловедения до медицины.
Вопрос-ответ

Чем обусловлено увеличение радиуса атома щелочных металлов с ростом их порядкового номера?
Увеличение радиуса атома щелочных металлов с ростом их порядкового номера обусловлено тем, что с увеличением порядкового номера увеличивается число электронных оболочек в атоме, а также число электронов, что приводит к увеличению отталкивающих электрон-электронных репульсий и, следовательно, к увеличению радиуса атома. В то же время, сила притяжения электронов к положительно заряженному ядру остается постоянной, поэтому радиус атома увеличивается.
Какие еще факторы могут влиять на размер атомов щелочных металлов?
Кроме порядкового номера, на размер атомов щелочных металлов могут влиять различные факторы. Например, размер атома может меняться под воздействием внешних условий, таких как давление и температура. Также, размер атомов может быть изменен в результате взаимодействия с другими атомами и молекулами.
Какая закономерность наблюдается в изменении радиуса атома щелочных металлов с ростом порядкового номера?
Наблюдается закономерность, согласно которой радиус атома щелочных металлов увеличивается с ростом порядкового номера. Это объясняется тем, что с увеличением порядкового номера увеличивается число электронов в атоме, что в свою очередь приводит к увеличению отталкивающих электрон-электронных репульсий и, следовательно, к увеличению радиуса атома. В то же время, притяжение электронов к положительно заряженному ядру остается постоянным, поэтому радиус атома увеличивается.
Какие применения может иметь знание о размерах атомов щелочных металлов?
Знание о размерах атомов щелочных металлов может иметь широкий спектр применений в различных областях науки и технологий. Например, оно может быть полезным при проектировании и синтезе новых материалов, в каталитических процессах, в разработке новых лекарственных препаратов, а также в конструировании электронных компонентов и устройств.
