Химия металлов — это раздел химии, который изучает свойства и реакции различных металлических элементов. Металлы имеют множество уникальных химических свойств, что делает их одной из основных групп элементов в периодической системе.
Основные свойства металлов:
- Проводимость электричества и тепла: металлы обладают высокой электропроводностью и теплопроводностью. Это свойство объясняется наличием свободных электронов в их кристаллической решетке.
- Пластичность и деформируемость: металлы могут быть легко изменены в форме и размере без разрушения структуры. Они обладают высокой пластичностью и деформируемостью.
- Металлический блеск: металлы имеют характерный блеск, известный как металлический блеск. Он обусловлен отражением света свободными электронами.
- Коррозионная стойкость: многие металлы обладают хорошей устойчивостью к коррозии, особенно благодаря образованию защитных оксидных пленок на их поверхности.
Реакции металлов
Металлы могут реагировать с различными веществами, образуя новые соединения. Некоторые из основных классов реакций металлов:
- Реакция с кислотами: при контакте с кислотами металлы могут выделять водород и образовывать соли.
- Окислительные и восстановительные реакции: металлы могут окисляться при контакте с кислородом или другими веществами, а также восстанавливать окислы катионов в металлическую форму.
- Реакция с водой: некоторые металлы могут реагировать с водой, образуя оксиды и выделяя водород.
- Комплексообразование: металлы могут образовывать стабильные комплексы с различными лигандами, такими как аммиак или этиленид, что позволяет использовать их в различных катализаторах и процессах.
В рабочем листе по химии металлов представлены основные химические свойства и реакции металлов, которые имеют важное значение в химической науке и промышленности.
Что такое химия металлов

Химия металлов изучает свойства и реакции различных металлов, а также способы их получения и применение в различных областях. Металлы являются одной из основных групп химических элементов, которые обладают специфическими свойствами и имеют широкий спектр применения в жизни человека и промышленности.
Металлы отличаются от других элементов тем, что они обладают блеском, твердыми или пластичными состояниями в обычных условиях, высокой теплопроводностью и электропроводностью. Они также могут образовывать ионы положительного заряда, что делает их активными в реакциях с другими веществами.
Химия металлов изучает как основные свойства металлов, такие как плавление и кипение, плотность, теплота сгорания и образование соединений, так и реакции металлов с кислотами, щелочами, солями и другими веществами. Эти реакции могут приводить к образованию солей, осадков и выделению газов. Также изучаются методы получения металлов, такие как термическая и электролитическая обработка руды или возможность извлечения металлов из вторичных источников.
Изучение химии металлов имеет важное значение, так как металлы являются основными строительными материалами, используются в производстве различного оборудования и инструментов, а также широко применяются в металлургической, электротехнике, химической и других отраслях промышленности. Кроме того, химические свойства металлов влияют на их взаимодействие с окружающей средой, с известными последствиями для экологии.
Основные свойства металлов
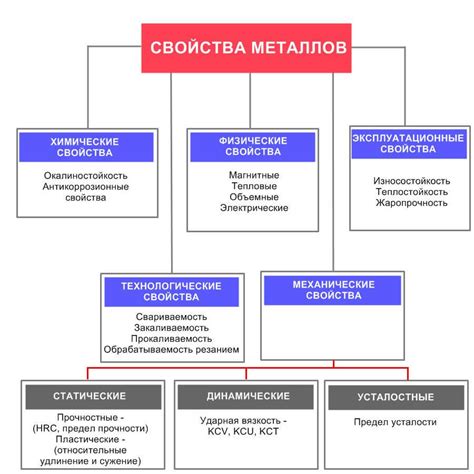
Металлы - это класс элементов, обладающих рядом характеристик, которые делают их уникальными и широко используемыми в различных областях нашей жизни.
- Проводимость электричества: Металлы отличаются высокой проводимостью электричества, благодаря свободным электронам в их валентной зоне. Именно поэтому многие металлы используются в производстве проводов и других электрических устройств.
- Теплопроводность: Металлы обладают отличной теплопроводностью, что делает их идеальными материалами для производства посуды и систем отопления. Благодаря способности быстро переносить тепло, металлы могут быть эффективно использованы в различных технических приложениях.
- Пластичность и формоизменяемость: Металлы могут быть легко обработаны и принять различные формы благодаря своей пластичности и формоизменяемости. Это позволяет создавать сложные конструкции и различные изделия, как в промышленности, так и в ежедневной жизни.
- Химическая активность: Металлы способны образовывать соединения с другими элементами за счет своей химической активности. Они могут образовывать соли, оксиды и гидроксиды, что делает их важными для производства различных материалов и даже лекарств.
Кроме того, металлы обладают высокой прочностью и устойчивостью к коррозии, что делает их долговечными и надежными материалами для различных конструкций и изделий.
Физические свойства металлов
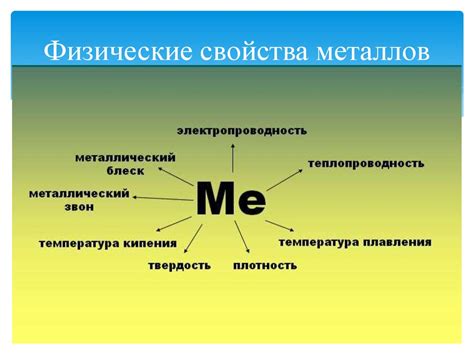
Плотность: Металлы обычно обладают высокой плотностью, что делает их отличным материалом для строительства и производства различных изделий.
Плавление и кипение: Большинство металлов имеют высокую температуру плавления и кипения. Например, железо плавится при приблизительно 1535 градусах Цельсия, а титан - даже приблизительно 1668 градусах Цельсия.
Электропроводность: Металлы, в основном, являются хорошими проводниками электричества. Это связано с наличием свободных электронов в их кристаллической структуре, которые могут двигаться свободно под воздействием электрического поля.
Теплопроводность: Большинство металлов обладают высокой теплопроводностью. Они прекрасно распространяют тепло, что делает их полезными в промышленности.
Относительная мягкость: Металлы обычно являются относительно мягкими материалами, однако некоторые металлы, такие как алмаз или хром, могут быть очень твёрдыми.
Магнитные свойства: Некоторые металлы обладают магнитными свойствами. Например, железо, никель и кобальт являются ферромагнитными металлами, то есть способны притягиваться к магниту и обладают постоянным магнитным полем.
Пластичность: Большинство металлов обладают высокой пластичностью, что позволяет легко формировать их в различные изделия. Это особенно полезно в металлообработке и производстве изделий.
Прочность: Металлы обычно обладают высокой прочностью, что позволяет им выдерживать большие нагрузки без разрушения. Это делает их идеальным материалом для строительства и машиностроения.
Расширяемость: Под воздействием нагревания металлы обычно расширяются. Это явление называется тепловым расширением и оно широко используется в промышленности и строительстве.
Химические свойства металлов

Металлы обладают рядом химических свойств, которые делают их особым классом веществ. Одной из основных характеристик металлов является их способность образовывать ионные соединения. В результате взаимодействия с не металлическими элементами, атомы металлов теряют электроны, превращаясь в положительно заряженные ионы. Это процесс называется ионизацией.
Металлы также обладают высокой электропроводностью, то есть способностью передавать электрический ток. Благодаря свободным электронам в своей структуре, металлы образуют электронное облако, которое позволяет электронам легко перемещаться по материалу. Это свойство делает металлы идеальными материалами для проводников электричества и создания электронных устройств.
Еще одно важное химическое свойство металлов - их способность образовывать сплавы с другими металлами или неметаллическими элементами. Сплавы - это гомогенные смеси двух или более компонентов, в которых металлы могут взаимодействовать, образуя твердые растворы или соединения. Сплавы обладают уникальными свойствами, такими как повышенная прочность, твердость, устойчивость к коррозии и теплоустойчивость.
Металлы также могут взаимодействовать с различными химическими соединениями и реагировать с ними. Одним из наиболее распространенных примеров является реакция металла с кислотой. В результате такой реакции образуется соль и выделяется водород. Это явление называется реакцией с металлом кислоты.
Реакции металлов с кислотами

Металлы реагируют с кислотами, образуя соли и выделяя водород. Эта реакция широко используется в лаборатории и в промышленности.
При контакте со сильными кислотами, такими как серная или соляная кислота, многие металлы могут растворяться или терять свою металлическую структуру. Например, железо реагирует с соляной кислотой, образуя хлорид железа и выделяя водород:
| Реакция | Уравнение |
|---|---|
| Реакция железа с соляной кислотой | Fe + 2HCl → FeCl2 + H2 |
Также металлы могут реагировать с более слабыми кислотами, такими как уксусная или лимонная кислота. Например, алюминий реагирует с уксусной кислотой, образуя ацетат алюминия и выделяя водород:
| Реакция | Уравнение |
|---|---|
| Реакция алюминия с уксусной кислотой | 2Al + 6CH3COOH → 2(CH3COO)3Al + 3H2 |
Реакции металлов с кислотами могут иметь разные скорости и интенсивность. Например, реакция железа с соляной кислотой происходит более активно и выделяет больше водорода, чем реакция алюминия с уксусной кислотой.
Реакции металлов с водой

Металлы имеют различную реакционную способность, особенно при контакте с водой. Некоторые металлы реагируют с водой активно и выделяются значительным количеством водорода, в то время как другие металлы могут быть пассивными и не реагировать с водой.
Наиболее активные металлы, такие как натрий и калий, реагируют с водой с отдельном подогреве. В результате реакции формируется гидроксид металла и выделяется водород. Например, натрий реагирует с водой по следующему уравнению: 2Na + 2H2O → 2NaOH + H2↑
Реактивность металлов с водой зависит от их потенциала окисления. Металлы с более высоким потенциалом окисления, такие как натрий и калий, имеют большую склонность к реакции с водой. Металлы с более низким потенциалом окисления, такие как медь и серебро, реагируют с водой гораздо слабее или не реагируют вообще.
Реакции металлов с водой имеют практическое применение, например, водород, получаемый при реакции металлов с водой, является важным промышленным сырьем для производства различных продуктов, таких как аммиак и магний.
Реакции металлов с кислородом

Кислород является одним из самых распространенных и активных элементов в природе. Он встречается в атмосфере и является неизбежным компонентом многих химических процессов. Металлы также реагируют с кислородом, что может иметь разные последствия и приводить к образованию различных соединений.
Реакция металлов с кислородом может приводить к образованию оксидов. Оксиды металлов обладают особыми свойствами и могут использоваться в различных областях, начиная от строительства до производства электроники. Например, оксид железа (Fe2O3), известный как ржавчина, обладает магнитными свойствами и используется в производстве магнитных материалов.
Некоторые металлы реагируют с кислородом горение, образуя оксиды и выделяя большое количество тепла и света. Например, реакция магния с кислородом приводит к образованию белого порошка – оксида магния (MgO). Этот процесс сопровождается ярким свечением и высокой температурой. Реакция алюминия с кислородом также сопровождается ярким свечением и выделяет большое количество тепла.
Однако не все металлы легко реагируют с кислородом. Некоторые металлы, такие как платина или золото, стойки к окислению и образуют защитные пленки, которые предотвращают реакцию с кислородом. Это делает их устойчивыми к окислению и дает им высокую коррозионную стойкость.
Вопрос-ответ

Что такое рабочий лист по химии металлов?
Рабочий лист по химии металлов – это сборник основных свойств и реакций металлов, который используется для изучения и систематизации знаний о химических свойствах металлов.
Какие свойства металлов можно найти на рабочем листе?
На рабочем листе по химии металлов можно найти информацию о таких свойствах металлов, как плотность, температура плавления и кипения, цвет, проводимость тепла и электричества, а также их химические свойства и реакции с другими веществами.
Что такое окисление металлов?
Окисление металлов – это процесс, в результате которого металлы соединяются с кислородом, образуя оксиды. Во время окисления металлы теряют электроны и превращаются в положительно заряженные ионы.
Какие реакции металлов можно найти на рабочем листе?
На рабочем листе по химии металлов можно найти информацию о реакциях металлов с кислотами, щелочами и солями, их способности к образованию сплавов, реакциях с водой и воздухом, а также о реакциях металлов в электролитах.
