Химические свойства металлов имеют большое значение в химии и позволяют понять, какие реакции могут происходить между металлами и другими веществами. Это важная информация, которую необходимо изучить и запомнить учащимся 9-го класса.
Одно из главных химических свойств металлов - их способность образовывать ионы положительной заряды, или катионы. Это явление называется окислением, и происходит при реакции металла с кислотой или водой. Некоторые металлы обладают большей активностью и более легко образуют ионы, чем другие.
Металлы могут проявлять свои химические свойства через разные реакции. Например, реакция металлов с кислотами происходит с выделением водорода и образованием солей. Это полезное свойство металлов используется в практических целях, например, при производстве водорода для использования в различных отраслях промышленности.
Проверочная работа: химические свойства металлов

Химические свойства металлов – одна из основных тем, изучаемых в курсе химии в 9 классе. В данной проверочной работе вы сможете продемонстрировать свои знания об этой теме.
Металлы обладают рядом характеристических химических свойств, которые делают их особым классом веществ. Одно из таких свойств – способность образовывать соли. Металлы могут образовывать различные соли с кислородными и неокисленными кислотами. Это свойство определяет их важную роль в жизни организмов и промышленности.
Еще одно важное химическое свойство металлов – способность вступать в реакцию с кислородом. Многие металлы активно реагируют с кислородом воздуха, что приводит к образованию оксидов металлов. Некоторые оксиды металлов обладают ценными свойствами и применяются в производстве различных материалов.
Кроме того, металлы являются хорошими проводниками электричества и тепла. Это связано с их особенной структурой и наличием свободных электронов в зоне проводимости. Благодаря этому свойству металлы широко применяются в электротехнике, машиностроении и других отраслях промышленности.
И наконец, металлы обладают высокой пластичностью и прочностью. Это позволяет им быть основными строительными материалами и использоваться для создания различных конструкций. Благодаря своей структуре и химическим свойствам металлы можно легко превратить в нужную форму и удовлетворить различным производственным и потребительским потребностям.
Роль металлов в химии

Металлы играют важную роль в химии и имеют множество уникальных свойств, которые делают их неотъемлемой частью нашей повседневной жизни. Металлы являются отличными проводниками электричества и тепла, а также обладают высокой прочностью и пластичностью.
Один из наиболее известных химических свойств металлов - нейтральная реакция с кислородом воздуха. Большинство металлов образуют оксиды, которые защищают поверхность от дальнейшего окисления. Некоторые металлы, такие как алюминий и цинк, образуют инертную пленку оксида, которая предотвращает дальнейшую коррозию.
Металлы также могут реагировать с кислотами, образуя соли и выделяя водород. Эта реакция широко используется в химической промышленности и позволяет получать различные металлоорганические соединения.
Одно из самых интересных свойств металлов - способность образовывать сплавы. Сплавы представляют собой материалы, состоящие из двух и более металлов, которые обладают улучшенными свойствами, такими как повышенная прочность и стойкость к коррозии. Примером сплавов являются сталь (железо и углерод) и бронза (медь и олово).
Металлы также широко используются в электрохимии, особенно в процессе электролиза. В процессе электролиза металл может быть выделен на катоде, а кислород или другой неметалл – на аноде. Этот процесс используется для получения чистых металлов, ионов металлов, а также в электролизе воды для получения водорода.
Свойства металлов в химии
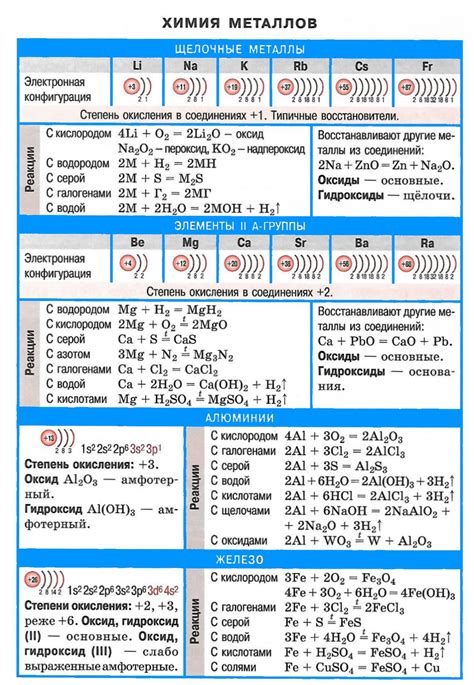
1. Проводимость электричества и тепла: Металлы обладают высокой проводимостью электричества и тепла. Это связано с наличием свободно движущихся электронов в металлической решетке, которые легко передают энергию и заряды.
2. Гибкость и пластичность: Металлы обладают способностью изменять форму без разрушения. Они могут быть вытянуты в проволоку, сплющены в листы или выплавлены для получения разных форм и изделий.
3. Прочность: Металлы характеризуются высокой прочностью и устойчивостью к механическим воздействиям. Они могут выдерживать большие нагрузки и сохранять свою форму.
4. Поверхностное действие: Металлы имеют способность реагировать с веществами на поверхности, образуя оксиды или соли. Некоторые металлы могут образовывать защитные оксидные пленки, которые предотвращают дальнейшую коррозию.
5. Коррозионная стойкость: Некоторые металлы обладают высокой устойчивостью к коррозии, особенно благодаря образованию пассивной оксидной пленки на поверхности. Однако большинство металлов подвержены коррозии под воздействием кислорода и влаги.
6. Ферромагнитные свойства: Некоторые металлы, такие как железо, никель и кобальт, обладают ферромагнитными свойствами и способностью притягивать магнит. Это связано с наличием упорядоченных магнитных моментов в атомах металлической решетки.
7. Восстановительные свойства: Некоторые металлы, такие как цинк и железо, обладают свойством восстанавливать окислители, при этом сами окисляясь. Это позволяет им использоваться в различных процессах восстановления и защиты от коррозии.
Химические реакции с металлами
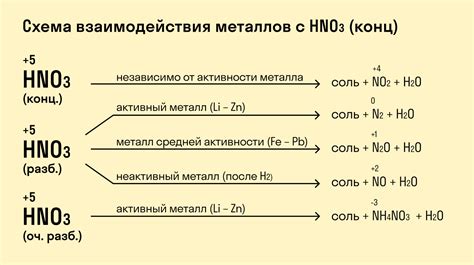
Взаимодействие металлов с другими веществами может приводить к различным химическим реакциям. Металлы, как правило, обладают высокой реакционной способностью, поэтому они могут вступать в реакцию с кислотами, щелочами и газами.
Одной из наиболее распространенных химических реакций с металлами является реакция с кислотами. При этом образуется соль и выделяется водород. Например, металл цинк при взаимодействии с соляной кислотой образует соль цинка и выделяется водородный газ:
- Zn + 2HCl = ZnCl2 + H2
Металлы также могут реагировать с щелочами, образуя соли и выделяяся водород. Например, реакция цинка с гидроксидом натрия приводит к образованию соли натрия и выделению водорода:
- Zn + 2NaOH = Na2ZnO2 + H2
Некоторые металлы способны взаимодействовать с кислородом воздуха, образуя оксиды металлов. Например, железо при взаимодействии с кислородом образует ржавчину:
- 4Fe + 3O2 = 2Fe2O3
Металлы могут вступать в реакцию и с различными газами. Например, реакция меди с кислородом приводит к образованию черной корки оксида меди:
- 2Cu + O2 = 2CuO
Таким образом, химические реакции с металлами широко используются в различных областях, таких как промышленность и наука. Знание этих реакций помогает понять и объяснить множество процессов, происходящих в химических системах, и применить их в практических целях.
Вопрос-ответ

Какие химические свойства металлов изучаются в 9 классе?
В 9 классе изучаются основные химические свойства металлов, такие как их реакция с водой и кислотами, окисление воздухом, образование солей и растворимость их солей.
Как происходит реакция металла с кислотой?
Реакция металла с кислотами происходит с образованием газа — водорода. При этом металл образует соль, растворимую в воде.
Какая реакция происходит при окислении металлов воздухом?
При окислении металлов воздухом образуется оксид металла. Например, железо окисляется до оксида железа.
Почему образуются соли при взаимодействии металлов с кислотами?
Соли образуются в результате реакции металла с кислотой. В данной реакции ионы металла смешиваются с ионами кислоты, образуя соль и воду.
