Простые металлы являются основными строительными блоками многих материалов, которые окружают нас ежедневно. Их структура и свойства отличаются от структуры и свойств других элементов, таких как неметаллы и полуметаллы. Однако, общая характеристика простых металлов - это их способность образовывать кристаллическую решетку из атомов.
Атомы элемента, являющегося простым металлом, имеют особую структуру, которая определяется их электронной конфигурацией. В отличие от полуметаллов и неметаллов, простые металлы имеют решетку из положительно заряженных ядер атомов и свободных электронов. Эти свободные электроны, называемые "электронами проводимости", обеспечивают металлам их основные физические свойства, такие как высокая теплопроводность и электропроводность.
Простые металлы могут быть разделены на две основные категории: переходные металлы и благородные металлы. Переходные металлы, такие как железо и медь, имеют сложную электронную структуру и могут образовывать соединения с другими элементами. Благородные металлы, такие как золото и платина, имеют более простую электронную структуру и обычно не образуют соединений.
Структура простого металла также влияет на поведение и свойства материалов, созданных из него. Например, если атомы металла имеют более хаотичное расположение в решетке, это может привести к ухудшению их свойств. Исследования структуры простого металла и его взаимодействия с другими элементами позволяют улучшить его свойства и создавать новые материалы с оптимальными характеристиками для различных применений.
Структура простого металла: атомы, элемент, вещество
Простые металлы - это химические элементы, обладающие особыми физическими и химическими свойствами. Структура простого металла основана на атомах данного элемента, которые образуют кристаллическую решетку.
Атомы простого металла взаимодействуют между собой через силы притяжения, что позволяет им образовывать твердое вещество - металл. Возможность образования твердого вещества обусловлена наличием свободных электронов в зоне проводимости.
Структура простых металлов основана на решетке кристаллической структуры, где каждый атом имеет регулярное расположение и окружен ближайшими соседями. Между атомами существуют слабые связи, что позволяет металлам обладать высокой проводимостью электричества и тепла.
Особенностью структуры простого металла является наличие дефектов в кристаллической решетке - вакансий и интерстиций. Эти дефекты создают возможность движения атомов, что обеспечивает подвижность электронов и пластичность металла.
Вещества, образованные из простых металлов, обладают высокой плотностью, прочностью и теплопроводностью. Благодаря структуре металла, они способны принимать и сохранять различные формы и иметь разнообразные физические свойства.
Атомы простых металлов и их особенности

Простые металлы представляют собой химические элементы, атомы которых обладают определенными особенностями.
Атомы простых металлов имеют металлическую структуру, что означает, что они образуют кристаллическую решетку. В этой решетке атомы расположены регулярно, с определенным промежутком между собой.
Одной из особенностей атомов простых металлов является их способность образовывать положительно заряженные ионы. Это связано с тем, что во внешней оболочке атома простого металла находятся несколько электронов, которые легко отдаются другим атомам или ионам.
Еще одной особенностью атомов простых металлов является их способность образовывать металлические связи. Когда атомы простого металла образуют решетку, их внешние электроны делятся между соседними атомами, что создает сильную связь между ними.
Важно отметить, что атомы простых металлов могут образовывать различные структуры решетки. Например, некоторые металлы образуют кубическую решетку, а другие - гексагональную или тетрагональную.
В целом, атомы простых металлов обладают уникальными свойствами, которые позволяют им образовывать прочные и проводящие электрический ток кристаллические решетки, что делает их неотъемлемой частью многих веществ и материалов, которые мы используем в повседневной жизни.
Роль атомов простых металлов в образовании вещества

Атомы простых металлов играют важную роль в образовании различных веществ и в основе структуры простых металлов. Атомы металлов обладают особыми свойствами, такими как подвижность электронов, что позволяет им создавать сильные металлические связи.
Свободные электроны, которые находятся в общих энергетических уровнях атомов простых металлов, могут свободно перемещаться, что обусловливает проводимость электричества в металлах. Они также отвечают за гибкость и деформируемость металлических материалов.
Металлическая связь между атомами простых металлов характеризуется тем, что каждый атом в металле все время окружен большим количеством свободных электронов. Это создает эффект тяжести, привлекающей электроны обратно к положительно заряженным ядрам атомов. Таким образом, в результате металлической связи образуется сетка атомов, в которой свободные электроны движутся между ядрами атомов и формируют систему положительно заряженных ионов и свободных электронов.
Другим свойством атомов простых металлов является их способность образовывать кристаллические структуры. Атомы простых металлов в кристаллической решетке занимают упорядоченное положение и организованы в определенные плоскости и направления.
Также следует отметить, что атомы простых металлов могут образовывать сплавы, вступая во взаимодействие с атомами других металлов. Это позволяет улучшить характеристики металлических материалов и придать им новые свойства, такие как повышенная прочность, устойчивость к коррозии или специфическая текучесть.
Влияние структуры атомов на свойства металлов
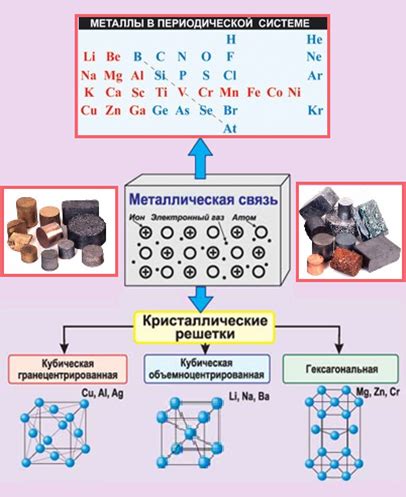
Металлы – это вещества, обладающие хорошей электропроводностью и теплопроводностью благодаря своей специфической структуре. Влияние структуры атомов на свойства металлов неоспоримо.
Структура атомов металлов предполагает наличие свободных, подвижно расположенных электронов во внешней оболочке атома. Это позволяет металлам проявлять механическую прочность и идеальную форму, поскольку их атомы могут перемещаться относительно друг друга без изменения физических связей.
Одна из самых характерных особенностей металлов – возможность образовывать атомные решетки. Атомы металла составляют трехмерную решетку, образуя идеальные структуры. Благодаря этому, у металлов высокая кристаллическая упорядоченность и отсутствие пустот в решетке, что дает им высокие физические свойства.
Структура атомов металлов также формирует их специфические свойства. Например, благодаря наличию свободных электронов металлы обладают хорошей электропроводностью и теплопроводностью. Кроме того, эти свободные электроны ответственны за хорошую деформируемость металлов и способность поглощать механическую энергию при нагружении, что обуславливает их высокую пластичность и металлический блеск.
Одной из важных характеристик металлов, определяемых структурой атомов, является их температура плавления и кипения. Свободные электроны в структуре металлов создают слабые связи между атомами, поэтому для смещения атомов из их положений требуется повышенная энергия, что обуславливает высокую температуру плавления и кипения у металлов.
Таким образом, структура атомов металлов играет существенную роль в формировании их свойств и определяет многочисленные характеристики металлов, делая их неотъемлемой частью нашей повседневной жизни.
Связь между атомами простого металла в пространстве
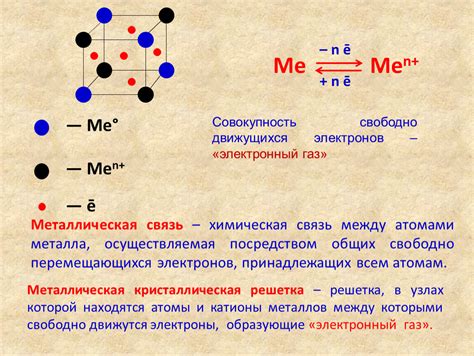
Структура простого металла определяется связью между его атомами в пространстве. Атомы простого металла образуют кристаллическую решетку, в которой они упорядочены и расположены на определенном расстоянии друг от друга.
Связь между атомами простого металла является металлической, что означает, что атомы обмениваются своими электронами и образуют общую электронную оболочку, называемую электронным морем. Эти общие электроны свободно двигаются между атомами, что придает металлу его уникальные свойства, такие как хорошая электропроводность и отличная теплопроводность.
Атомы простого металла в кристаллической решетке располагаются на определенных позициях, называемых узлами кристаллической решетки. Они могут быть расположены в виде кубов, граней куба или граней тетраэдра в зависимости от типа кристаллической решетки.
Структура простого металла существует благодаря силам притяжения и отталкивания между атомами. Силы притяжения обусловлены наличием положительных ядер в атомах и общим электронным морем. Силы отталкивания возникают за счет электростатического отталкивания между электронами на общей электронной оболочке.
Таким образом, связь между атомами простого металла в пространстве представляет собой сложную взаимосвязь между электронами и ядрами этих атомов, обеспечивающую существование и устойчивость структуры металла.
Вопрос-ответ

Что такое простой металл?
Простой металл - это химический элемент, который обладает электропроводностью и металлическим блеском.
Какова структура простого металла?
Структура простого металла состоит из регулярного решетчатого массива атомов этого металла. Атомы металла располагаются близко друг к другу и образуют кристаллическую структуру.
Что происходит с атомами простого металла при образовании вещества?
При образовании вещества атомы простого металла приобретают определенное положение в кристаллической решетке. Они располагаются регулярно и формируют кристаллическую структуру металла.
Какова роль атомов простого металла в обладании веществом электропроводностью?
Атомы простого металла играют важную роль в обладании веществом электропроводностью. Благодаря свободным электронам, которые находятся между атомами, металлы обладают высокой электропроводностью и теплопроводностью.
