Окисление металла – процесс, при котором поверхность металла взаимодействует с окружающей средой, образуя окисные соединения. В результате окисления металла происходит образование окиси, которая может иметь различные свойства и применения.
Каждая окись обладает определенными химическими свойствами, что влияет на ее применение в разных отраслях промышленности. Например, некоторые окиси металла используются в процессе производства светопрочного стекла, керамических изделий, электроники и других материалов.
Окиси металла также широко применяются в медицине, косметологии и пищевой промышленности. Некоторые окиси металла обладают антибактериальными свойствами и используются в производстве антисептических препаратов, косметики и пищевых добавок.
Окиси металла имеют различные цвета, что позволяет им находить применение в производстве красителей и красок. Кроме того, некоторые окиси металла обладают специфическими свойствами, такими как проводимость электричества или термическая устойчивость, что делает их полезными в производстве электроники и огнезащитных материалов.
Окисление металла – это не всегда негативный процесс. Продукты окисления металла могут иметь множество полезных свойств, используемых в различных отраслях промышленности и науки.
Первый продукт окисления металла: ржавчина
Ржавчина — это первый продукт окисления металла, возникающий при взаимодействии металла с кислородом и влагой воздуха. Основной причиной образования ржавчины является процесс коррозии, который приводит к повреждению поверхности металла и изменению его свойств.
Коррозия металла начинается с образования окиси металла (оксид), которая в дальнейшем превращается в гидроксид и далее – в ржавчину. Ржавчина обладает характерным красно-коричневым цветом и является несущим элементом конструкции металлических изделий.
Процесс образования ржавчины активизируется в условиях повышенной влажности и наличии солей в воздухе. Например, металлические изделия, находящиеся вблизи морского побережья или применяемые в условиях высокой влажности, более подвержены образованию ржавчины.
Ржавчина негативно влияет на качество и прочность металлических изделий. Она может вызывать разрушение материала и снижение его функциональных характеристик. Также ржавчина может привести к ухудшению внешнего вида изделия.
Для предотвращения образования ржавчины и защиты металлических изделий используют различные методы, включая нанесение защитного покрытия, применение специальных антикоррозийных составов и регулярное техническое обслуживание.
Второй продукт окисления металла: коррозия

Коррозия – это процесс, при котором металлы подвергаются разрушению под воздействием окружающей среды. В основе коррозии лежит окислительно-восстановительный процесс, при котором металл переходит в окисленное состояние. В результате этого процесса образуются оксиды металла, которые обычно имеют низкую прочность и способствуют дальнейшему разрушению металлической конструкции.
Коррозия является одной из основных причин повреждения металлических изделий и инфраструктуры. Она влияет на долговечность и надежность металлических конструкций, что приводит к экономическим потерям и необходимости замены или ремонта поврежденных объектов.
Существует несколько видов коррозии, включая поверхностную коррозию, например, образование ржавчины на поверхности железа, и скрытую внутреннюю коррозию, которая может разрушить металл изнутри, не оставляя видимых признаков на его поверхности.
Для предотвращения коррозии применяются различные методы и технологии защиты, включая нанесение антикоррозийных покрытий, гальваническое покрытие, а также использование антикоррозионных добавок и ингибиторов коррозии.
Однако, несмотря на применение различных методов защиты, коррозия по-прежнему остается серьезной проблемой, требующей постоянной внимательности и ухода.
Третий продукт окисления металла: оксид
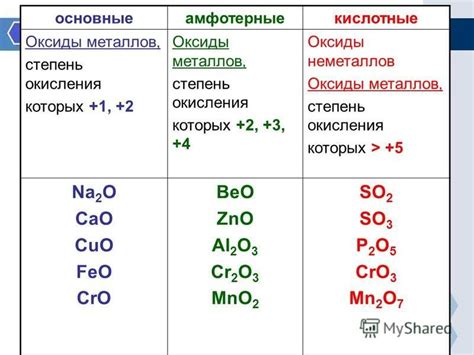
Оксид – это третий продукт окисления металла. Оксид образуется в результате взаимодействия металла с кислородом. Взаимодействие происходит при высоких температурах или при воздействии кислорода водой. Оксид обладает характерными физическими и химическими свойствами.
Оксиды могут быть кислотные, щелочные или амфотерными. Кислотные оксиды имеют кислотные свойства и взаимодействуют с водой, образуя кислоты. Щелочные оксиды обладают щелочными свойствами и реагируют с кислотами, образуя соли. Амфотерные оксиды могут взаимодействовать и с кислотами, и с щелочами.
Оксиды металлов имеют широкое применение в различных отраслях промышленности и научных исследованиях. Например, оксид алюминия (алюминиевая зола) используется в производстве стекла, керамики, различных типов катализаторов. Оксиды железа широко применяются в производстве красок, магнитных материалов, водородосмесительных систем. Оксид кремния (кварц) используют в производстве стекла, электронных компонентов, солнечных батарей.
Четвертый продукт окисления металла: гидроксид
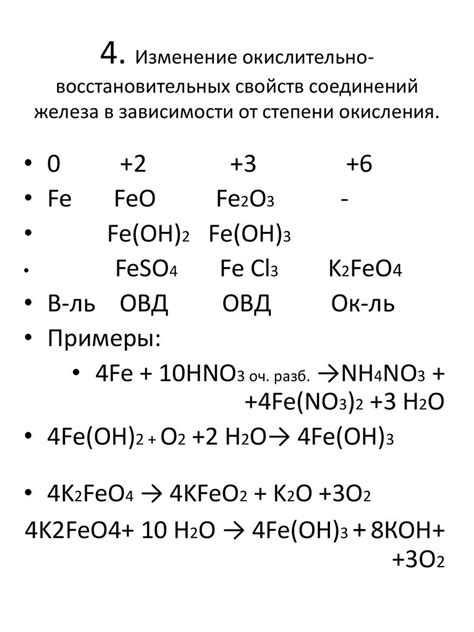
Гидроксид - один из основных и наиболее распространенных продуктов окисления металла. В результате реакции металла с водой образуется соединение, содержащее гидроксильную группу (-OH). Гидроксиды металлов обладают основными свойствами и могут реагировать с кислотами, образуя соль и воду.
Гидроксид обычно представляет собой твердое вещество, которое может иметь различные формы и цвета в зависимости от металла. Например, гидроксид железа имеет вид зеленоватой порошкообразной массы, а гидроксид алюминия может быть представлен как белый кристалл, так и в виде гельобразной субстанции.
Гидроксиды широко используются в различных отраслях промышленности. Например, гидроксид кальция (известный как «известь») используется для изготовления цемента, а гидроксид натрия («каустическая сода») - для производства стекла и чистки трубопроводов.
В медицине гидроксиды металлов могут использоваться как антисептические средства для дезинфекции ран, а также используются в качестве водородных ионовых обменников в процессе осмоларного дренирования.
Таким образом, гидроксид является важным продуктом окисления металла, который широко используется в различных областях жизни человека и промышленности.
Пятый продукт окисления металла: сульфид

Сульфид является одним из продуктов окисления металла, образующимся в результате реакции металла с кислородом. Процесс окисления металла может происходить при взаимодействии с водой, воздухом или другими химическими веществами.
Сульфид, химическая формула которого обычно записывается в виде МхСу, представляет собой соединение металла с серой. Он имеет темную или черную окраску и обладает характерным запахом. Также сульфиды обладают хорошей электропроводностью и часто используются в электротехнике и электронике.
Примерами сульфидов могут служить железный сульфид (FeS), медный сульфид (CuS), свинцовый сульфид (PbS) и другие. Они обладают различными свойствами и применяются в разных сферах, например, для производства красителей, катализаторов, аккумуляторов и даже фоточувствительных материалов.
Сульфиды могут иметь разную растворимость в воде. Некоторые из них растворяются хорошо, как, например, натриевый и калиевый сульфиды, а другие практически нерастворимы, как свинцовый и ртутиевый сульфиды. Это свойство используется в химическом анализе и технологических процессах.
В целом, сульфиды представляют собой важный класс химических соединений, которые обладают широким спектром свойств и применений. Изучение их свойств играет важную роль в развитии науки и технологий, а также способствует поиску новых материалов и решению различных проблем в разных областях.
Шестой продукт окисления металла: нитрид

Нитрид - это продукт окисления металла, получаемый путем соединения металла с азотом. Он обладает рядом уникальных свойств и широко используется в различных отраслях промышленности.
Нитриды являются одними из самых твердых и стойких к повреждениям веществ. Они обладают высокой теплостойкостью, химической инертностью и электропроводностью, что позволяет использовать их в производстве электроники и полупроводников. Например, нитрид кремния используется при создании интегральных схем.
В металлургии нитриды применяются для упрочнения металлических сплавов и инструментов. Они улучшают прочность, твердость и износостойкость материалов, что позволяет значительно продлить их срок службы. Например, нитрид титана применяется в производстве высокопрочного оборудования.
Нитриды также находят применение в производстве покрытий и пленок. Они образуют тонкий защитный слой, предотвращающий коррозию и износ металлической поверхности. Например, нитрид хрома используется для создания твердого и стойкого к истиранию покрытия на автомобильных деталях.
Седьмой продукт окисления металла: фосфат

Окисление металлов может привести к образованию различных продуктов, одним из которых является фосфат. Фосфаты – это соли или эфиры ортофосфорной кислоты, которые образуются при реакции металлического катализатора с оксидом фосфора в присутствии воды.
Фосфаты широко применяются в различных отраслях промышленности и науки. Они используются в производстве удобрений, стекла, керамики, электроники, металлургии и многих других областях. Кроме того, фосфаты являются важными компонентами в пищевой промышленности, где применяются в качестве пищевых добавок и консервантов.
Фосфаты обладают рядом полезных свойств, благодаря которым они нашли широкое применение. Они способны стимулировать рост растений в удобрениях, обеспечивать жаропрочность в стеклянных и керамических изделиях, а также повышать электропроводность в электронике. Кроме того, фосфаты способны снижать кислотность в пищевых продуктах и улучшать их консистенцию, что делает их более стабильными и безопасными для употребления.
Седьмым побочным продуктом окисления металла является фосфат, который широко применяется в различных областях промышленности и науки. Фосфаты способны стимулировать рост растений, обеспечивать жаропрочность в материалах и повышать электропроводность. Они также применяются в пищевой промышленности в качестве добавок и консервантов. В целом, фосфаты являются важными и универсальными соединениями, которые находят применение во многих сферах нашей жизни.
Вопрос-ответ

Какие вещества образуются при окислении металла?
При окислении металла образуются оксиды металла или соли металла, в зависимости от окислительной способности окислителя и свойств самого металла. Например, при окислении железа образуется оксид железа (III) Fe2O3, а при окислении меди образуется оксид меди (II) CuO.
Какие продукты образуются при окислении алюминия?
При окислении алюминия образуется оксид алюминия Al2O3. Данное вещество известно под названием криолит. Оксид алюминия является очень стойким и имеет высокую температуру плавления, поэтому используется в различных областях, таких как производство стекла, керамики, катализаторов и т.д.
