Металлы - одни из наиболее распространенных материалов, используемых в промышленности, строительстве и повседневной жизни. Однако, на протяжении времени, поверхности металлов подвержены различным процессам, которые могут приводить к их деградации и разрушению. Один из таких процессов - коррозия, которая происходит под воздействием влаги, кислот или других вредных веществ. Коррозия является химической реакцией, при которой металл растворяется и образуются оксиды или гидроксиды металла.
Коррозия является серьезной проблемой в различных сферах деятельности, таких как автомобильная промышленность, нефтегазовая отрасль и строительство. Она может привести к сокращению срока службы металлических конструкций, повышению издержек на их техническое обслуживание и восстановление. Однако, существуют различные методы предотвращения коррозии, такие как нанесение защитных покрытий, использование специальных сплавов или осуществление катодной защиты.
Кроме того, на поверхности металлов могут происходить и другие процессы, связанные с электрохимическими реакциями. Например, электролиз - это процесс, при котором электрический ток приводит к химическим превращениям в растворе. Подобные реакции применяются в различных областях, от производства металлов до аккумуляторов.
Таким образом, процессы на поверхности металлов оказывают значительное влияние на их эксплуатационные характеристики и применение. Понимание этих процессов позволяет разрабатывать эффективные методы защиты металлических конструкций от коррозии и использовать электрохимические реакции в различных промышленных процессах.
Процессы на поверхности металлов:

Поверхность металлов подвержена различным процессам, которые влияют на их структуру и свойства. Одним из наиболее известных процессов является коррозия. Коррозия представляет собой окислительно-восстановительную реакцию, при которой металл взаимодействует с окружающей средой, что приводит к его разрушению. Коррозия может происходить под воздействием воды, кислот, щелочей и других агрессивных веществ.
Еще одним важным процессом на поверхности металлов является адсорбция. Адсорбция представляет собой процесс присоединения молекул или ионов вещества к поверхности металла. Этот процесс может быть физическим или химическим. В результате адсорбции на поверхности металла формируется пленка, которая может защищать металл от дальнейшей коррозии или, наоборот, способствовать ее развитию.
Еще одним важным процессом на поверхности металлов является пассивация. Пассивация представляет собой образование на поверхности металла пассивной пленки, обладающей устойчивостью к разрушению. Пассивация может происходить самопроизвольно или под действием специальных химических или электрохимических процессов. Пассивирующая пленка защищает металл от коррозии, предотвращая контакт металла с окружающей средой.
Одним из интересных процессов на поверхности металлов является электрохимическая полировка. При этом процессе на поверхности металла происходит растворение неровностей и образование гладкой поверхности. Электрохимическая полировка используется в различных отраслях, например, в производстве электронной техники и ювелирных изделий, для придания поверхности металла эстетического вида.
Коррозия: сущность и причины

Коррозия - это процесс разрушения металлов под воздействием химических или электрохимических реакций с окружающей средой. Она приводит к утрате металлических свойств и может нанести значительный ущерб оборудованию, конструкциям и механизмам.
Основной причиной коррозии является окисление металлов при контакте с водой или влажными веществами. Вода содержит растворенные газы, такие как кислород и углекислый газ, которые реагируют с металлами, вызывая окисление и образование коррозионной среды.
Кроме того, окружающая среда может содержать агрессивные химические вещества, такие как соли, кислоты или щелочи, которые также могут вызывать коррозию. В промышленных условиях к основным причинам коррозии относятся еще и электрохимические процессы, такие как гальваническая коррозия или коррозия, связанная с разностью потенциалов между различными металлическими элементами системы.
Эффективные меры по защите от коррозии включают применение защитных покрытий, таких как краска или покрытие из другого металла, использование антикоррозионных добавок при производстве металлических изделий, а также контроль окружающей среды и условий эксплуатации.
Химические реакции на поверхности металлов
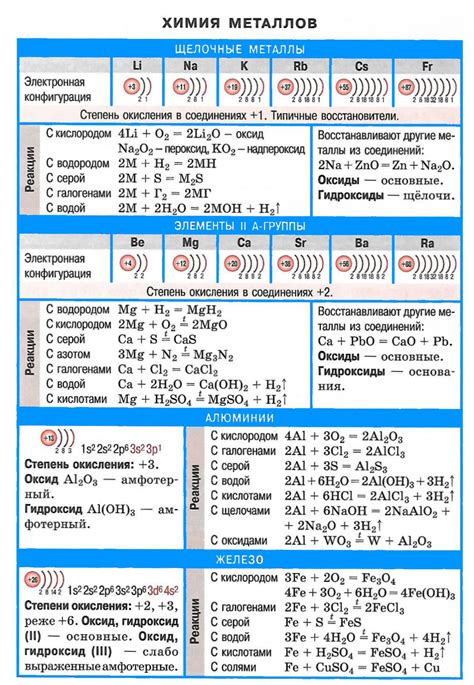
Поверхность металла подвержена различным химическим реакциям, которые могут приводить к изменению ее свойств и состояния. Эти реакции могут сопровождаться окислением или восстановлением атомов металла, образованием оксидных или гидроксидных пленок, коррозией и другими процессами.
Одной из основных химических реакций на поверхности металлов является коррозия — процесс, при котором металл взаимодействует с окружающей средой, что приводит к его разрушению. В результате коррозии на поверхности металла могут образовываться оксиды, гидроксиды или другие соединения, которые меняют его свойства и можно увидеть в виде пятен, ржавчины или потери блеска.
Кроме коррозии, на поверхности металлов могут происходить и другие химические реакции. Например, металл может вступать в электрохимические реакции, когда его поверхность взаимодействует с электролитом. В результате этих реакций могут образовываться различные осадки или соединения, которые могут быть использованы для различных целей, например, в процессе гальванического покрытия.
Важно отметить, что химические реакции на поверхности металлов могут быть управляемыми и контролируемыми. Использование специальных противокоррозионных покрытий, регулирование условий среды или осуществление электролиза позволяют уменьшить или предотвратить процессы коррозии и других химических реакций на поверхности металлов.
Электрохимические процессы на металлической поверхности
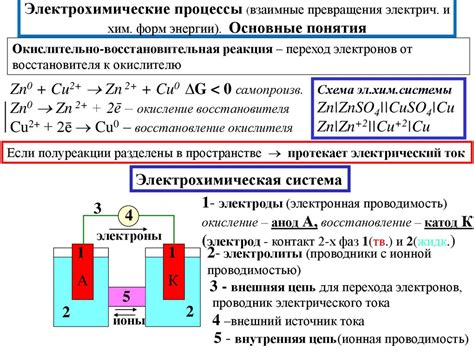
Металлы имеют способность вступать в электрохимические реакции при взаимодействии с окружающей средой. Электрохимические процессы на металлической поверхности обусловлены перемещение заряда через электролит и могут включать в себя такие явления, как анодная и катодная реакции, коррозия и электродепозиция. Эти процессы имеют огромное значение во многих отраслях промышленности, включая производство и обработку металлов, а также в сфере энергетики.
В электрохимических процессах на металлической поверхности ключевую роль играет разность потенциалов между анодом и катодом. При наличии электролита, который представляет собой среду, способную проводить электрический ток, между анодом и катодом возникает электролитическая ячейка. В этой ячейке протекают электрохимические реакции, в результате которых происходит переход электронов и ионов веществ от одного электрода к другому.
Анодная реакция представляет собой окислительно-восстановительную реакцию, в результате которой на аноде происходит процесс окисления. Катодная реакция, напротив, происходит на катоде и представляет собой процесс восстановления. Такие процессы обычно протекают одновременно и непосредственно влияют на поверхность металла.
Наиболее известным процессом, связанным с металлической поверхностью, является коррозия. Коррозия это процесс, при котором металл взаимодействует с окружающей средой, что приводит к его разрушению и образованию окислов. Это важный фактор, который необходимо учитывать при проектировании и эксплуатации металлических конструкций, так как коррозия может вызвать серьезные последствия, включая потерю прочности и непригодность к использованию.
Влияние окружающей среды на поверхность металлов

Поверхность металлов может изменяться под влиянием окружающей среды. Различные химические вещества, находящиеся в воздухе или взаимодействующие с металлом напрямую, могут приводить к коррозии, окислению или образованию защитной пленки.
Коррозия – это процесс разрушения поверхности металла под влиянием агрессивных химических веществ. Окисление – это реакция металла с кислородом воздуха, в результате которой образуется оксид металла. Образование защитной пленки может происходить при взаимодействии металла с окружающей средой, что способствует уменьшению скорости коррозии.
Например, атмосферный воздух, содержащий кислород и влагу, является одним из основных факторов коррозии металлов. Некоторые металлы, такие как железо, магний и алюминий, легко подвергаются окислению под воздействием кислорода. Однако, другие металлы, такие как алюминий и хром, образуют защитную оксидную пленку на поверхности, которая предотвращает дальнейшее корродирование.
Также, окружающая среда может содержать различные химические соединения, которые могут изменять поверхность металла. Например, соляная кислота может вызывать образование ржавчины на железе, а щелочное растворы могут привести к образованию зеленой патины на меди.
Таким образом, понимание влияния окружающей среды на поверхность металлов является важным для предотвращения коррозии и сохранения качества и долговечности металлических конструкций.
Вопрос-ответ

Какие процессы могут происходить на поверхности металлов?
На поверхности металлов могут происходить различные процессы, включая коррозию, окисление и электрохимические реакции.
Что такое коррозия?
Коррозия - это процесс разрушения металла под воздействием окружающей среды. Она обычно связана с химическими реакциями между металлом и окислителем, таким как кислород или вода. Коррозия может привести к образованию оксидной пленки на поверхности металла, что делает его менее прочным и может вызвать повреждения или потерю функциональности.
Какие факторы влияют на скорость коррозии металлов?
Скорость коррозии металлов зависит от нескольких факторов, включая тип металла, окружающую среду, температуру, влажность и наличие других химических веществ. Например, неблагоприятные условия, такие как высокая влажность и наличие кислоты в воздухе, могут ускорить процесс коррозии.
Каким образом электрохимические реакции связаны с поверхностью металлов?
Электрохимические реакции на поверхности металлов играют важную роль во многих процессах, включая коррозию и электролиз. В этих реакциях электроны переносятся между металлом и растворенными ионами. Например, в процессе коррозии металла, металлический ион может окисляться, покидая поверхность металла и образуя оксидную пленку.
