Коррозия металлов является одной из основных проблем, с которой сталкиваются инженеры и конструкторы при разработке различных металлических конструкций. Процессы коррозии происходят на аноде - металлическом элементе, который подвергается разрушению под воздействием окружающей среды. В данной статье рассмотрим механизмы разрушения на аноде и способы защиты от коррозии.
Один из основных механизмов разрушения на аноде - это электрохимические реакции между металлом и окружающими его средой. При взаимодействии электролитов с металлом происходит возникновение коррозионных явлений, которые приводят к постепенному разрушению структуры материала. Важное значение имеет величина электродной разности между анодом и катодом, которая определяет скорость коррозии и степень разрушения металла.
Для защиты от коррозии используются различные способы, включающие применение защитных покрытий, использование антикоррозионных материалов и методов электрохимической защиты. Защитные покрытия могут быть нанесены на поверхность металла с целью создания барьера между металлическим элементом и окружающей средой. Они могут быть органическими или неорганическими и должны обладать высокой стойкостью к коррозии и хорошей адгезией к металлической поверхности.
Также для защиты от коррозии используются антикоррозионные материалы, способствующие замедлению процессов коррозии на аноде. Эти материалы могут проникать в структуру металла и увеличивать его стойкость к разрушению. Электрохимическая защита - это метод, основанный на изменении условий окружающей среды для уменьшения разрушительных электрохимических реакций на аноде. Для этого могут использоваться анодные защитные системы, пассивационные покрытия и другие технологии.
В заключение, процессы на аноде при коррозии металлов являются сложными и многогранными. Понимание механизмов разрушения и применение эффективных способов защиты позволяют предотвратить нежелательное разрушение металлических конструкций и повысить их долговечность и надежность в условиях воздействия агрессивной окружающей среды.
Механизмы разрушения при коррозии металлов

Коррозия металлов – это процесс разрушения и утраты их свойств под воздействием окружающей среды. Механизмы разрушения при коррозии металлов могут быть различными и зависят от химического состава металла, температуры, влажности и других факторов окружающей среды.
Одним из основных механизмов разрушения при коррозии металлов является анодное растворение, когда атомы металла превращаются в ионы и уносятся с поверхности в виде растворенных соединений. Этот процесс приводит к уменьшению толщины металла и появлению язвенных дефектов на его поверхности. Как правило, анодное растворение происходит в кислой или щелочной среде, где высокая концентрация ионов обеспечивает интенсивность процесса.
Другим механизмом разрушения при коррозии металлов является питание, которое происходит, когда разные части металла находятся в контакте с различными средами. В этом случае происходит передача электронов и ионов между различными участками металла, что приводит к появлению ореолов коррозии. Этот процесс особенно активен при наличии электролитов, таких как вода или растворы солей.
Еще одним механизмом разрушения при коррозии металлов является межкристаллическая коррозия, когда разные зерна металла имеют разные электрохимические свойства и образуют гальванические элементы. В результате этого процесса происходит разрушение межкристаллических границ и появление трещин, что уменьшает прочность металла.
Для защиты от разрушения при коррозии металлов широко используются различные методы. Один из них – покрытие металла защитными покрытиями, такими как эмалями или пластиковыми пленками. Другой метод – использование антикоррозионных добавок при изготовлении металлических изделий. Также важным способом защиты от коррозии является контроль и регулирование условий окружающей среды, таких как влажность или концентрация агрессивных химических веществ.
Электрохимический процесс
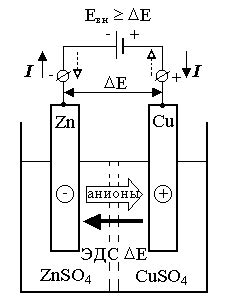
При коррозии металлов на анодной поверхности происходит электрохимическая реакция, что приводит к разрушению материала. Окисление металла на аноде и выделение электронов являются основными процессами в коррозии.
Электрохимическая реакция происходит в присутствии электролита, который является средой, проводящей электрический ток между анодом и катодом. В результате окисления металла на анодной поверхности образуются ионы металла, которые перемещаются через электролит к катоду. На катоде происходит восстановление ионов металла с выделением электронов.
Электрический ток в электрохимической реакции обеспечивается разностью потенциалов между анодом и катодом. Разность потенциалов определяется различием электрохимических свойств анодных и катодных областей металла, а также влиянием внешних факторов, таких как концентрация электролита и температура.
Для защиты от коррозии необходимо применять различные методы, такие как применение покрытий, использование анодной защиты, применение антикоррозионных добавок в электролиты и другие. При выборе метода защиты необходимо учитывать электрохимические свойства конкретного металла и условия эксплуатации.
Пассивация и активация
Пассивация и активация – важные процессы, связанные с коррозией металлов. Пассивация – это способность металла образовывать защитную покрытие на своей поверхности, которое препятствует его дальнейшей коррозии. В процессе пассивации на поверхности металла образуется пассивная пленка, состоящая из оксидов, гидроксидов или солей металла, которая обеспечивает защиту металла от агрессивной среды. Пассивация особенно характерна для таких металлов, как алюминий, хром, нержавеющая сталь и титан.
Активация, наоборот, является нарушением пассивного состояния металла и приводит к его коррозии. Активация может происходить из-за различных факторов, таких как нарушение защитной пленки, агрессивная среда или наличие других металлов с более отрицательным электродным потенциалом вблизи активируемого металла.
Процессы пассивации и активации можно регулировать и контролировать. Например, для устранения активации металла можно использовать методы катодной защиты, при которых на активируемый металл подается постоянное электрическое напряжение, препятствующее его коррозии. Также можно применять специальные защитные покрытия, которые предотвращают пассивацию или активацию металла.
Понимание процессов пассивации и активации металлов позволяет разработать эффективные методики защиты металлических конструкций от коррозии. Это особенно важно в промышленности, где коррозия металлов может привести к серьезным последствиям, таким как потеря прочности и долговечности конструкций, а также нанести значительный экономический ущерб.
Образование коррозионных продуктов
Коррозия – это процесс разрушения металлов под воздействием окружающей среды. При коррозии на аноде происходят электрохимические реакции, в результате которых образуются коррозионные продукты.
Образование коррозионных продуктов может происходить различными механизмами. Один из них – окисление металла при взаимодействии с кислородом воздуха или воды. Например, железо при коррозии окисляется, образуя ржавчину – гидроксид железа(III) и гидроксид железа(II).
Второй механизм образования коррозионных продуктов – растворение металла в окружающей среде. Например, при коррозии алюминия в воде образуются алюминиевые гидроксиды. Они растворяются и образуют ионы алюминия, которые мигрируют в воду.
Третий механизм – образование осадков на поверхности металла. Например, при коррозии меди в атмосфере с обильным содержанием сероводорода может образоваться черная непрозрачная пленка сульфида меди. Она защищает металл от дальнейшей коррозии.
Коррозионные продукты обычно обладают меньшей прочностью и устойчивостью к окружающим условиям, чем исходный металл. Поэтому коррозия может приводить к разрушению конструкций и повреждению материала.
Для защиты от коррозии применяют различные методы, такие как нанесение защитных покрытий (например, красок или эмалей), использование антикоррозионных материалов или проведение катодной защиты. Эти методы позволяют уменьшить воздействие окружающей среды на металл и предотвратить образование коррозионных продуктов.
Кавитация и эрозия

Кавитация — это процесс образования и роста пузырьков пара в жидкости под воздействием разряжения. При кавитации происходит разрушение поверхностей, так как пузырьки могут внезапно коллапсировать, создавая сильное давление. Кавитационная эрозия может возникать на поверхностях различных металлов при контакте с жидкостью, особенно если она содержит воздушные или газовые примеси.
Основной механизм разрушения при кавитации — ударные волны, которые возникают в результате коллапса пузырьков. Ударная волна создает сильное воздействие на поверхность металла, приводя к разрывам и образованию микротрещин. В результате поверхность металла становится неровной и пористой, что может привести к дальнейшему разрушению материала.
Для защиты от кавитационной эрозии используются различные методы. Один из них – применение специальных покрытий на поверхности металла. Эти покрытия могут быть изготовлены из различных материалов, таких как полимеры, керамика или металлы, и обладать устойчивостью к коллапсу пузырьков или ударным волнам. Также можно использовать специальные добавки к рабочей жидкости, которые помогают предотвратить образование пузырьков пара и предотвращают кавитационную эрозию.
Однако, помимо кавитации, эрозия также может возникать вследствие воздействия частиц или струй на поверхность металла. Например, при прохождении жидкости или газа через трубопроводы или детали оборудования может возникать эрозия абразивного характера. Твердые частицы или струи жидкости создают истирание и разрушение поверхности металла. Эрозия также может быть вызвана химическим воздействием жидкости.
Для защиты от эрозии применяются различные методы. Один из них – применение защитных покрытий на поверхности металла. Эти покрытия могут быть изготовлены из специальных материалов, которые устойчивы к истиранию и химическому воздействию. Также можно использовать специальные смазочные материалы или добавки к рабочей жидкости, которые снижают трение и истирание на поверхности металла.
Питание паразитными коррозионными токами

Коррозия металлов часто вызывается не только химическими реакциями, но и различными электрохимическими процессами. Одним из таких процессов является питание паразитными коррозионными токами.
Паразитные коррозионные токи возникают в результате гальванического контакта различных металлов, находящихся в окружающей среде или в конструкции. Этот электрический контакт создает батарею, в которой металлы играют роль электродов. При наличии электролита (например, влажного воздуха или влаги) между металлами возникают электрохимические реакции, сопровождающиеся появлением паразитных токов.
Паразитные коррозионные токи могут приводить к интенсивной коррозии металлов, особенно если сопротивление в электрическом контуре невелико. Данные токи особенно опасны в местах с повышенной влажностью или при наличии химически активных веществ. Результатом таких процессов является быстрое разрушение металлических конструкций.
Для предотвращения питания паразитными коррозионными токами используют различные защитные меры. Одной из таких мер является изоляция металлических конструкций от контакта с другими металлами или электролитами. Защиту от паразитных токов также осуществляют с помощью специальных защитных покрытий, которые не позволяют электрическому контакту между разными металлами.
Выводить металл с цепи коррозии тоже применяется как мера защиты от паразитных коррозионных токов. В таком случае один из металлов цепи коррозии удаляется, что приводит к разрыву электрической цепи и прекращению питания паразитными токами. Это достигается, например, путем замены одного из металлов на другой, менее активный металл или материал, который не подвержен коррозии.
Биологическая коррозия

Биологическая коррозия – это процесс разрушения металлических материалов под воздействием биологических организмов, таких как бактерии, водоросли, грибы и морские организмы. При этом, микроорганизмы оказывают влияние на процессы коррозии, ускоряя их или замедляя.
Процессы биологической коррозии наиболее активно протекают в местах с высокой влажностью и пониженным содержанием кислорода, таких как почвы, донные отложения, водоемы, а также в биофильмах, образующихся на поверхности металла. Биологическая коррозия может привести к значительному ухудшению свойств материалов, сокращению их срока службы и возможности возникновения аварийных ситуаций.
Существует несколько механизмов биологической коррозии. Бактерии, водоросли и грибы могут выделять различные химические вещества, такие как кислоты, энзимы или токсины, которые оказывают негативное воздействие на поверхность металла. Они также могут создавать коррозионные клетки, образуя питательные разности и увеличивая скорость коррозионных процессов.
Для защиты от биологической коррозии используются различные методы. Одним из них является нанесение защитных покрытий, которые препятствуют проникновению микроорганизмов на поверхность металла. Также можно использовать специальные добавки к материалам, которые обладают антимикробными свойствами и предотвращают развитие биологической коррозии. Важным моментом является также поддержание оптимальных условий эксплуатации, включая правильное хранение и поддержание чистоты материалов.
- Биологическая коррозия – это процесс разрушения металлических материалов под воздействием биологических организмов.
- Процессы биологической коррозии активно протекают в местах с высокой влажностью и пониженным содержанием кислорода.
- Бактерии, водоросли и грибы выделяют химические вещества, создают питательные разности и увеличивают скорость коррозионных процессов.
- Для защиты от биологической коррозии используются защитные покрытия, добавки с антимикробными свойствами и поддержание оптимальных условий эксплуатации.
Вопрос-ответ

Как происходит процесс коррозии металлов на аноде?
При коррозии металлов на аноде происходит окисление металла, то есть выделение электронов в окружающую среду. Электрохимически процесс коррозии может быть представлен следующей реакцией: Fe – 2e = Fe2+ + 2e-. Катодным образом является реакция восстановления электронов, проводимая другой материей или реагентом.
Какие механизмы разрушения металлов можно наблюдать при процессе коррозии на аноде?
При процессе коррозии на аноде металл может разрушаться различными способами. Один из основных механизмов разрушения - это образование оксидов и гидроксидов металла, которые легко отслаиваются и приводят к появлению трещин и заглублений на поверхности. Также может происходить растворение металла в коррозионной среде, что приводит к образованию пустот и дырок. В результате этих процессов поверхность металла становится неровной и уменьшается его прочность.
