Аммиак является одним из наиболее распространенных химических соединений, которое широко применяется в промышленности и научных исследованиях. Он получается путем синтеза из водорода и азота, и обладает множеством уникальных свойств, благодаря которым нашел свое применение в различных отраслях.
Одним из важных аспектов использования аммиака в промышленности является его реакция с щелочными металлами, такими как натрий и калий. При взаимодействии аммиака с этими металлами образуется амидный и гидридный комплексы. Амидные комплексы, в свою очередь, находят применение как промежуточные продукты в синтезе органических соединений, а гидридные комплексы используются в качестве катализаторов в различных реакциях.
Применение аммиака и его соединений с щелочными металлами широко распространено в промышленности производства удобрений. В результате взаимодействия аммиака с натрием и калием образуются удобрения, содержащие азот. Это является важным этапом в создании готовых комплексных удобрений, которые направлены на повышение плодородия почв и увеличение урожайности сельскохозяйственных культур.
В научных исследованиях аммиак и его реакции с щелочными металлами также играют важную роль. Изучение этих реакций позволяет углубить знания о свойствах аммиака и его взаимодействии с другими веществами. Такие исследования могут привести к созданию новых синтетических материалов, катализаторов, а также способствовать развитию новых технологий в промышленности и сельском хозяйстве.
Применение химических реакций аммиака с щелочными металлами

Химические реакции аммиака с щелочными металлами имеют широкое применение в промышленности и научных исследованиях. Аммиак (NH3) является сильным основанием и реагирует с щелочными металлами (например, натрием и калием) для образования аммиаката металла.
Процесс реакции аммиака с щелочными металлами обычно проводят в атмосфере аргона или другого инертного газа, чтобы предотвратить окисление металла или воспламенение аммиака. Реакция может происходить при комнатной температуре или при повышенных температурах и давлениях, в зависимости от конкретных условий эксперимента.
Применение химических реакций аммиака с щелочными металлами включает производство аммиаката, который широко используется в производстве удобрений. Аммиакат металла, такой как натрий аммиакат или калий аммиакат, обладает высокой растворимостью в воде и содержит аммиачную форму азота, необходимого для роста растений. Это делает аммиакаты металлов удобными и эффективными удобрениями для сельского хозяйства.
Химические реакции аммиака с щелочными металлами также находят применение в научных исследованиях, например, при синтезе новых соединений или исследовании их химических свойств. Реакция аммиака с щелочными металлами может быть использована для создания специфических структур и соединений, которые могут быть дальше изучены и применены в различных областях науки и технологий.
В промышленности и научных исследованиях
Химические реакции аммиака с щелочными металлами нашли широкое применение как в промышленности, так и в научных исследованиях.
В промышленности аммиак используется в процессах синтеза азотных удобрений. Реакция аммиака с щелочными металлами, такими как натрий, калий и литий, позволяет получить аммиакаты – соединения аммиака с этими металлами, которые затем могут быть использованы в качестве удобрений. Синтез аммиаката является одной из основных химических реакций в производстве азотных удобрений и позволяет значительно повысить эффективность процесса.
В научных исследованиях реакции аммиака с щелочными металлами широко применяются в исследовании различных свойств и характеристик аммиака и его соединений. Эти реакции позволяют получить чистые образцы аммиаката и изучать их структуру, свойства и потенциальные применения. Исследования в этой области могут быть полезными для разработки новых методов синтеза аммиака и улучшения существующих процессов производства удобрений.
Также, реакции аммиака с щелочными металлами имеют большое значение в каталитической химии. Данные реакции часто используются в катализаторах для различных процессов, таких как гидрирование, деаммиакация и синтез аммиака. Катализаторы на основе аммиаката помогают ускорить эти процессы и повысить их эффективность.
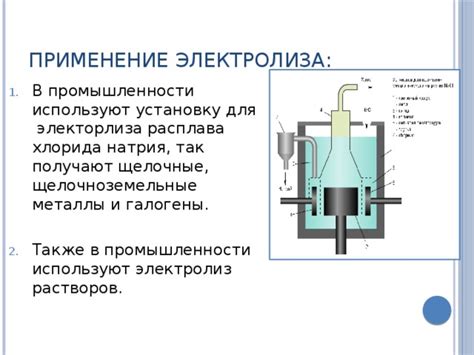
Электролиз: процесс разложения аммиака

Электролиз аммиака - это химический процесс разложения аммиака на атомы азота и водорода с помощью электрического тока. Для проведения электролиза аммиака используют специальную электролитическую ячейку, в которой находится разделительная мембрана. При прохождении электрического тока через аммиак, он разлагается на азот и водород.
Процесс электролиза аммиака имеет широкое применение в промышленности и научных исследованиях. Он используется для получения высокочистого водорода, который затем может быть использован в производстве азотной кислоты, аммиака, метанола и других химических соединений. Электролиз аммиака также позволяет получать атомарный азот, который используется в процессах синтеза аммиака и других химических реакций.
В процессе электролиза аммиака играет важную роль катодная реакция, в результате которой образуется водород. В то же время, на аноде происходит окисление аммиака, в результате чего образуется азот и водород. Электролиз аммиака можно проводить как при нормальных условиях (температура и давление), так и при повышенных температурах и давлениях.
В заключение, электролиз аммиака представляет собой важный процесс, который используется в различных областях промышленности и научных исследований. Он позволяет получать высокочистый водород и атомарный азот, активно применяемые в химической промышленности. Таким образом, разложение аммиака при помощи электролиза является важной химической реакцией, способствующей развитию и улучшению технологий и процессов в различных областях науки и промышленности.
Получение металлического калия из аммиака
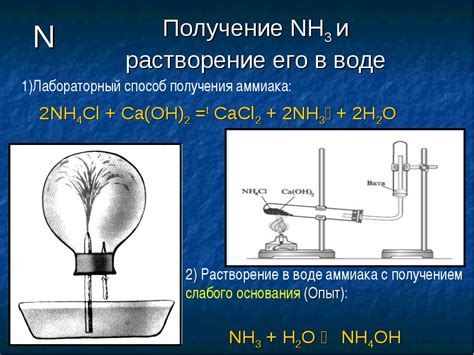
Металлический калий может быть получен из аммиака путем реакции калия с аммиаком. Этот процесс описывается следующим химическим уравнением:
2K + 2NH3 → 2KNH2 + H2
Первоначально, для проведения реакции, необходимо обеспечить условия, при которых аммиак жидкий. Для этого используется холодильник, в котором аммиак охлаждается до температуры, ниже его точки кипения.
После охлаждения аммиака, к нему добавляется кусок металлического калия. В результате реакции происходит образование соли, которую можно выделить путем испарения избыточного аммиака. После этого можно получить металлический калий в виде твердого вещества.
Получение металлического калия из аммиака имеет применение в промышленности для получения высокочистого калий-аммиака, который используется в процессе получения пластмасс, удобрений и других химических соединений. В научных исследованиях этот процесс часто используется в качестве метода получения металлических элементов для последующих экспериментов и исследований.
Аммиак и натрий: создание взрывоопасного соединения

Аммиак (NH3) – химическое вещество, обладающее рядом уникальных свойств. Оно является газообразным, имеет характерный резкий запах и обладает щелочными свойствами. Аммиак широко используется в промышленности и научных исследованиях благодаря своей возможности реагировать с другими веществами, в том числе с щелочными металлами.
Натрий (Na) – щелочной металл, который также обладает определенными особенностями. Он является мягким и реактивным элементом, который может успешно взаимодействовать с аммиаком, образуя взрывоопасное соединение.
В процессе реакции аммиака с натрием образуется особое соединение – аммиакат натрия (NH3•Na). Это гигроскопичное вещество, которое реагирует с влагой воздуха и образует раствор сильной щелочи. Аммиакат натрия имеет высокое давление насыщенного пара и может быть использован в промышленных процессах, требующих наличия аммиака, но исключающих его жидкую форму.
Однако стоит отметить, что аммиакат натрия – взрывоопасное соединение. При повышении температуры или взаимодействии с окислителями, вещество может проявить пирофорные свойства и воспламениться. Поэтому при работе с аммиакатом натрия необходимо соблюдать особые меры предосторожности и следить за условиями хранения и транспортировки.
Применение аммиака и щелочных металлов в производстве удобрений

Аммиак и щелочные металлы являются важными компонентами при производстве удобрений, которые играют существенную роль в сельском хозяйстве и повышении урожайности.
Аммиак (NH3) используется в реакции с щелочными металлами, такими как натрий (Na) или калий (K), для создания щелочных аммиакатов – основных компонентов удобрений. Реакция аммиака с щелочными металлами приводит к образованию аммиаката металла (NH3-М), который характеризуется высокой концентрацией азота, необходимого растениям для нормального развития и роста.
Удобрения на основе аммиака и щелочных металлов обеспечивают растения не только азотом, но и необходимыми микроэлементами, такими как калий, фосфор и магний. Они способствуют образованию белка и хлорофилла, усиливают процессы фотосинтеза, укрепляют растительные ткани, повышают экологическую устойчивость культурных растений и улучшают их качество.
Применение удобрений на основе аммиака и щелочных металлов позволяет фермерам повышать урожайность, снижать затраты на использование пестицидов, контролировать состояние почвы и улучшать плодородие. Кроме того, такие удобрения имеют хорошую стабильность и долгий срок хранения, что делает их популярными и востребованными на рынке сельскохозяйственных продуктов.
Исследование реакции аммиака с щелочными металлами в качестве альтернативного источника энергии

В настоящее время проблема поиска альтернативных источников энергии становится все более актуальной. В этом контексте значительное внимание уделяется исследованию химических реакций, которые могут служить источником энергии. Одной из таких реакций является реакция аммиака с щелочными металлами.
Аммиак (NH3) - это химическое соединение из азота и водорода. Щелочные металлы, такие как натрий и калий, обладают высокой реакционной активностью и могут взаимодействовать с аммиаком, образуя амиды (например, натриевый амид - NaNH2). Эта реакция сопровождается выделением большого количества тепла и генерацией аммония (NH4), который может использоваться в качестве источника энергии.
Исследования показывают, что реакция аммиака с щелочными металлами имеет высокий термический КПД, что делает ее привлекательной для использования в качестве альтернативного источника энергии. Кроме того, аммиак - дешевое и широко доступное соединение, что также способствует его потенциальному применению в промышленности.
Научные исследования в этой области направлены на обнаружение новых катализаторов и оптимизацию условий реакции, чтобы повысить эффективность и экономическую целесообразность процесса. Одной из основных задач таких исследований является увеличение скорости реакции и уменьшение затрат на производство аммония.
Таким образом, исследование реакции аммиака с щелочными металлами представляет собой перспективное направление, которое может принести значительные результаты в области альтернативной энергетики. Развитие этой области не только способствует решению проблемы энергетической независимости, но и имеет потенциал для сокращения выбросов углерода и смягчения климатических изменений.
Химический синтез амины: использование аммиака и щелочных металлов
Химический синтез амины представляет собой процесс, при котором из аммиака и щелочных металлов получаются различные классы органических соединений. Амины включают в себя разнообразные азотсодержащие молекулы, которые являются важным классом химических соединений и находят широкое применение в промышленности и научных исследованиях.
Использование аммиака и щелочных металлов в химическом синтезе аминов основано на реакции аммиака с металлическими ионофорами, такими как натрий или калий. При взаимодействии аммиака с щелочными металлами происходит образование амидов, которые могут быть превращены в амины при последующем обработке соответствующими реагентами. Этот процесс широко используется для получения аминов различного строения и функциональности.
Химический синтез амина с использованием аммиака и щелочных металлов имеет большое применение в промышленности. Амины используются в производстве пластмасс, лекарственных препаратов, пестицидов, красителей, и многих других продуктов. Благодаря разнообразию возможных реакций и модификаций, данный метод синтеза обеспечивает высокую степень контроля над структурой и свойствами аминов.
Кроме промышленного применения, химический синтез амина с использованием аммиака и щелочных металлов является важным инструментом в научных исследованиях. Изучение реакций амина с различными соединениями позволяет углубить понимание химических свойств этих веществ и разработать новые методы и технологии синтеза аминов с заданными свойствами.
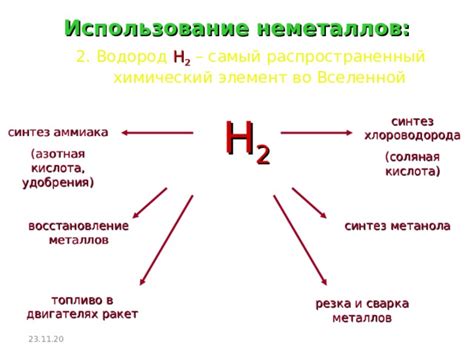
Применение аммиака и щелочных металлов в качестве катализаторов

Аммиак (NH3) и щелочные металлы, такие как натрий (Na), калий (K) и литий (Li), имеют широкое применение в качестве катализаторов в различных химических процессах.
Аммиак широко используется в аммиачной синтезе, процессе, при котором аммиак получают из азота (N2) и водорода (H2). В этом процессе аммиак выступает в качестве катализатора, ускоряя реакцию между азотом и водородом и образуя аммиачную смесь, которая затем может быть использована в производстве многих продуктов, включая удобрения и химические соединения.
Щелочные металлы, такие как натрий, калий и литий, также активно применяются в химической промышленности в качестве катализаторов. Они могут использоваться в реакциях полимеризации, превращая мономерные соединения в большие молекулы полимера. Кроме того, щелочные металлы могут быть вовлечены в реакции горения, такие как в батареях, где они служат катализаторами для химической реакции между кислородом и веществами, содержащими энергию, например, металлическими гидридами.
Применение аммиака и щелочных металлов в качестве катализаторов также занимает значительное место в научных исследованиях. Ученые и инженеры исследуют новые способы использования этих веществ в процессах синтеза и конверсии, а также пытаются улучшить их эффективность и стабильность. Такие исследования имеют большое значение для развития новых технологий и промышленных процессов.
Вопрос-ответ

Какая роль имеют реакции аммиака с щелочными металлами в промышленности?
Реакции аммиака с щелочными металлами имеют важное применение в промышленности, особенно в производстве различных типов амидов и аминов. Например, аммиак может использоваться для получения солей аммония, которые впоследствии используются в производстве удобрений. Кроме того, аммиак взаимодействует с натрием и калием для образования амидов, которые широко применяются в производстве пластмасс, лекарств и многих других химических соединений.
Как исследования в области реакций аммиака с щелочными металлами помогают развитию науки?
Научные исследования в области реакции аммиака с щелочными металлами играют важную роль в различных областях науки. Эти исследования помогают улучшить понимание основных принципов химических реакций и механизмов, которые ими регулируются. Кроме того, такие исследования позволяют разрабатывать новые катализаторы и методы синтеза, что может привести к разработке новых материалов и процессов, полезных в научных и промышленных целях.
