Окисление металлов является важным процессом в химии и материаловедении, который в значительной мере определяет их свойства и степень коррозии. Этот процесс происходит в присутствии кислорода и часто сопровождается образованием окиси металла или ржавчины. Окисление металлов происходит по сложной схеме реакций, включающей в себя несколько основных этапов.
Первым этапом является адсорбция кислорода на поверхности металла. Кислород взаимодействует с активными местами металлической поверхности, образуя водородные и оксидные группы, которые могут оставаться на поверхности или уходить из нее. Поверхность металла может быть покрыта слоем оксидных соединений или молекул кислорода, что предотвращает взаимодействие смежных металлических атомов с кислородом.
Далее следует этап окисления металлических атомов, который происходит путем передачи электронов от металлических атомов кислороду. В результате этого образуются ионы металла с положительным зарядом и ионы кислорода с отрицательным зарядом. Образовавшиеся ионы постепенно перемещаются в раствор или удаляются из поверхности металла.
Последним этапом процесса окисления металлов является образование окиси металла или ржавчины на поверхности металла. Это происходит в результате взаимодействия ионов металла с водой или другими химическими веществами. Ржавчина обладает низкой прочностью и структурной стабильностью, что часто приводит к разрушению и деградации металлических материалов.
Лучшей защитой от окисления металлов является использование защитных покрытий, антикоррозионных материалов и правильного обслуживания материалов. Это позволяет уменьшить воздействие окисления и продлить срок службы металлических изделий.
Процесс окисления металлов: от реакции до ржавчины

Окисление металлов является природным процессом, который приводит к образованию оксидов металлов, таких как ржавчина, когда металл взаимодействует с кислородом в атмосфере. Этот процесс может происходить самостоятельно или быть ускоренным влиянием различных факторов, таких как вода, соль или кислоты.
Сам процесс окисления металлов начинается с реакции металла с кислородом, которая приводит к образованию оксида металла. Например, железо реагирует с кислородом из воздуха, образуя оксид железа, известный как ржавчина. Эта реакция может быть представлена следующим образом:
- 2Fe (металл) + O2 (кислород) → 2FeO (оксид железа)
Оксиды металлов, такие как ржавчина, могут иметь различные цвета и свойства в зависимости от металла и условий реакции. Например, ржавчина на поверхности железа имеет темно-коричневый цвет и обладает хрупкостью. Кроме того, оксиды металлов могут образовывать защитную пленку на поверхности металла, которая может предотвращать дальнейшее окисление.
Окисление металлов может иметь как положительные, так и отрицательные последствия. С одной стороны, окисление металлов может использоваться для создания различных материалов, таких как оксиды металлов, которые могут обладать определенными свойствами, такими как устойчивость к коррозии или проводимость электричества. С другой стороны, окисление металлов может приводить к разрушению или понижению качества металлических изделий, особенно в условиях повышенной влажности или агрессивной среды.
В заключение, процесс окисления металлов, который начинается с реакции металла с кислородом, может привести к образованию оксидов металлов, включая ржавчину. Окисление металлов может иметь как положительные, так и отрицательные последствия, поэтому важно принимать меры предосторожности, чтобы предотвратить нежелательное окисление металлов и сохранить их качество и долговечность.
Реакция окисления металлов: что это такое?
Реакция окисления металлов – это процесс, при котором металлические элементы взаимодействуют с воздухом или другими окислительными веществами, образуя оксиды или другие соединения. Это естественный процесс, который имеет большое значение как с точки зрения химии, так и промышленности.
Окисление металлов происходит благодаря реакции с кислородом, который содержится в воздухе. Как правило, при окислении металлов образуется пленка оксида на их поверхности. Например, железо окисляется при взаимодействии с воздухом, образуя ржавчину – оксид железа. Реакция окисления может проходить быстро или медленно в зависимости от условий окружающей среды.
Оксиды, образующиеся при окислении металлов, имеют разные свойства и могут быть как полезными, так и вредными. Некоторые металлические оксиды применяются в производстве красок, стекла и керамики, а другие могут быть токсичными. Например, оксид свинца, образующийся при окислении свинца, является опасным для здоровья человека. Поэтому контроль за процессом окисления металлов имеет большое значение.
Основные факторы, влияющие на скорость окисления

Скорость окисления металлов может зависеть от различных факторов, которые оказывают влияние на характер и скорость протекания реакции. Рассмотрим основные из них:
- Температура - повышение температуры влечет за собой увеличение скорости окисления металлов. Это объясняется тем, что при повышенной температуре молекулы газов или жидкостей, участвующие в реакции, обладают большей энергией, что способствует более интенсивному взаимодействию между ними.
- Концентрация окислителя - увеличение концентрации окислителя также увеличивает скорость окисления металлов. Это связано с тем, что большее количество окислителя означает больший потенциал по переносу электронов, что ускоряет реакцию окисления.
- Площадь поверхности металла - чем больше площадь поверхности металла, тем больше молекул окислителя может соприкасаться с ним и участвовать в реакции окисления. Поэтому, мелко распределенный металл или порошок металла окисляются быстрее, чем массивное изделие.
- Присутствие каталитических веществ - некоторые вещества могут выступать в роли катализаторов и ускорять ход окислительной реакции. К таким веществам относятся, например, соль, кислоты или дисперсные катализаторы.
Эти факторы могут работать как независимо, так и взаимодействовать друг с другом, определяя скорость окисления металлов. Понимание этих факторов позволяет контролировать окислительные процессы и предотвращать или замедлять ржавление металлических поверхностей.
Роль влаги в процессе окисления металлов
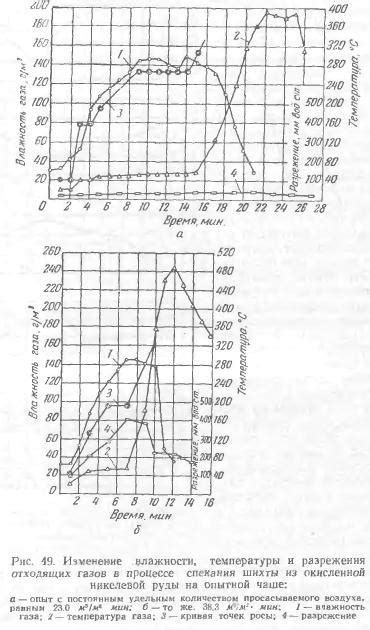
Влага играет важную роль в процессе окисления металлов. Контакт с водой или влажной средой способствует началу окислительной реакции металлов, которая приводит к образованию ржавчины. Вода является необходимым компонентом для образования и поддержания ржавчины на поверхности металла.
Вода действует как проводник электричества, обеспечивая процесс окисления металла. При наличии влаги на поверхности металла происходит электрохимическая реакция, в результате которой электроны переносятся с поверхности металла на окружающую среду. Это приводит к растворению металла и образованию ионов металла в воде.
Вода также обеспечивает доступ кислорода к поверхности металла. Когда металл соединяется с кислородом, образуются оксиды металла, которые составляют основу ржавчины. Влага помогает активизировать реакцию окисления металла, ускоряя процесс образования ржавчины.
Использование воды или растворов солей металлов может значительно ускорить процесс окисления. Альтернативой влаге могут быть другие реагенты, такие как кислоты или щелочи, которые накапливаются на поверхности металла и предоставляют дополнительные ионы для реакции окисления.
В целом, влага является неотъемлемой частью процесса окисления металлов. Взаимодействие металла с водой обеспечивает электрохимическую реакцию и активирует образование ржавчины. Знание роли влаги поможет понять, почему ржавчина образуется на металлических поверхностях при длительном контакте с влажной средой.
Что такое ржавчина и как она возникает

Ржавчина представляет собой процесс окисления металла, который возникает при взаимодействии металлической поверхности с влажностью и кислородом. Часто ржавчиной называют окись железа, которая образуется при окислении железа или стали.
Ржавчина обычно имеет коричнево-красный оттенок и может быть представлена в виде пятен, пластинок или слоев на металлической поверхности. Она не только портит внешний вид металла, но и может привести к его разрушению.
Процесс образования ржавчины начинается с образования оксида железа Fe2O3, который затем превращается в гематит Fe2O3·nH2O. При продолжении окисления металла образуется гидроокись железа Fe(OH)3, которая преобразуется в оксид железа Fe2O3, который и образует характерные коричнево-красные отложения - ржавчину.
Ржавчина образуется в результате существенного окисления металла, что происходит при наличии влаги и кислорода. Влага позволяет развиваться окислительно-восстановительным процессам, а кислород действует как окислитель, проникая в металл и разрушая его структуру. Этот процесс может быть ускорен в условиях повышенной влажности или при наличии солей в воздухе, например, вблизи океана.
Влияние окружающей среды на процесс окисления

Окисление металлов – это процесс, в результате которого металлы взаимодействуют с кислородом в окружающей среде и образуют оксиды. Окружающая среда играет важную роль в этом процессе, так как ее свойства и состав могут существенно влиять на скорость и интенсивность окисления.
Влажная среда способствует ускорению окисления металлов. Вода взаимодействует с металлом, образуя коррозионные продукты, такие как ржавчина. В результате образования ржавчины металл может потерять свои свойства, стать менее прочным и стабильным.
Кислотная среда также может ускорять процесс окисления металлов, так как кислоты содержат в себе ионы водорода, которые могут реагировать с металлом. Результатом такой реакции может быть образование солей металла, которые являются окислами.
Окисление металлов может происходить и в атмосфере, так как она содержит кислород и влагу. Результатом такого окисления может быть образование оксидных пленок на поверхности металла. Однако, не все металлы одинаково подвержены окислению в атмосфере. Некоторые металлы, такие как алюминий и цинк, образуют защитные пленки, которые предотвращают дальнейшее окисление.
Таким образом, окружающая среда имеет существенное влияние на процесс окисления металлов. Влажная среда и кислоты могут ускорять окисление, в то время как атмосфера может вызывать формирование оксидных пленок на поверхности металла. Для защиты металлов от окисления необходимо принимать соответствующие меры, такие как покрытие поверхности защитными пленками или использование антикоррозионных покрытий.
Способы защиты металлов от окисления

Окисление металлов – это процесс, при котором металлы взаимодействуют с кислородом воздуха, образуя оксиды. Окисление может привести к появлению ржавчины, коррозии и ухудшению внешнего вида металлических поверхностей.
- Покрытие металлов. Это один из самых распространенных способов защиты от окисления. Металл может быть покрыт пленкой из инертного материала, такого как оксид алюминия или оксид циркония. Это помогает препятствовать контакту металла с оксигеном и влагой в воздухе, тем самым предотвращая его окисление.
- Гальваническая защита. Этот метод заключается в создании гальванической пары между защищаемым металлом и другим металлом, которому окисление не столь вредно. Защищаемый металл выступает как анод и сознательно окисляется, а второй металл, играя роль катода, не окисляется. Примером гальванической защиты является цинковое покрытие стали.
- Использование антиоксидантов. Некоторые вещества, такие как фосфаты, нитраты и сульфиды, могут быть добавлены к окислительной среде, чтобы предотвратить или замедлить окисление металлов. Антиоксиданты действуют как комплексообразователи, образуя стабильные соединения с металлами и препятствуя их окислению.
Способ защиты металлов от окисления выбирается в зависимости от условий эксплуатации, типа металла и вида окисления, важно знать, что каждый из методов имеет свои преимущества и недостатки. Правильно выбранный способ защиты поможет сохранить металлические изделия в хорошем состоянии и продлить их срок службы.
Практические примеры окисления металлов в быту и промышленности
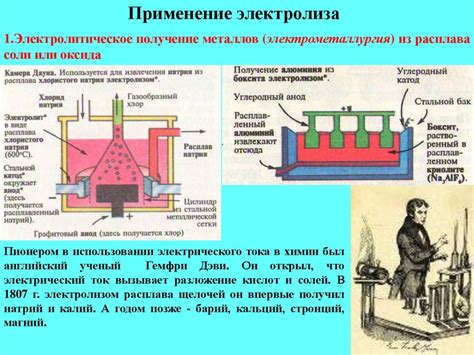
Окисление металлов является всеобщим процессом, который происходит в различных сферах нашей жизни. В быту мы наблюдаем окислительные процессы на металлических предметах, которые оставлены на открытом воздухе или находятся во влажной среде.
Один из ярких примеров окисления металлов в быту - это образование ржавчины на поверхности железных предметов, таких как кухонные ножи, трубы или автомобильные детали. Ржавчина образуется в результате реакции металла с кислородом воздуха и влагой. При взаимодействии этих компонентов на поверхности металла образуется слой оксида, который придаёт ему характерный коричневый цвет.
В промышленности окисление металлов играет также важную роль. Например, окисление алюминия на поверхности алюминиевой фольги или алюминиевых конструкций приводит к образованию защитного слоя оксида, который предотвращает дальнейшее повреждение металла. Такой слой оксида делает алюминий устойчивым к коррозии и позволяет использовать его в различных областях промышленности, включая производство упаковочных материалов и строительные конструкции.
Вопрос-ответ

Что такое окисление металлов?
Окисление металлов - это процесс химической реакции, при которой металлы соединяются с кислородом воздуха или других веществах, образуя оксиды.
Как происходит процесс окисления металлов?
Процесс окисления металлов начинается с реакции между металлом и кислородом. Когда металл контактирует с кислородом, происходит окислительно-восстановительная реакция, в результате которой металл претерпевает окисление, а кислород восстанавливается.
Какие факторы влияют на скорость окисления металлов?
Скорость окисления металлов зависит от ряда факторов, включая наличие влаги, особенности окружающей среды, температуру, наличие кислорода и других химических веществ. Также влияет электрический потенциал металла, его реактивность и поверхностные свойства.
Что происходит с металлом при окислении?
При окислении металла происходит образование оксида, который обычно является твердым веществом. Этот оксид образует поверхностную пленку на металлической поверхности, которая защищает металл от дальнейшего окисления.
Что такое ржавчина?
Ржавчина - это оксидное соединение железа, образующееся при окислении металла. Ржавчина имеет красно-коричневый цвет и обычно образует хрупкий слой на поверхности металла.
