Металлы играют важную роль в нашей жизни, и одним из наиболее фундаментальных свойств металлов является их способность взаимодействовать с водой. Это взаимодействие основано на химической реакции между металлом и водой, известной как металлическая коррозия. Металлическая коррозия происходит из-за окисления металла и редокс-реакции, которая включает передачу электронов между металлом и молекулами воды.
Вода, в свою очередь, имеет уникальные физические и химические свойства. Молекулы воды состоят из атомов водорода и кислорода, а также обладают полярной структурой. Это означает, что молекулы воды имеют отрицательно заряженную сторону (кислородный атом) и положительно заряженную сторону (водородные атомы). Это свойство делает воду эффективным растворителем для многих веществ, включая ионы металлов.
Взаимодействие металлов с водой может происходить различными способами в зависимости от вида металла и условий реакции. Некоторые металлы, такие как натрий и калий, очень реактивны и взаимодействуют с водой с большой энергией, при этом выделяется водородный газ и образуется гидроксид металла. Другие металлы, такие как железо и алюминий, могут реагировать с водой, но гораздо медленнее.
Металлическая коррозия имеет важные практические последствия, так как приводит к появлению ржавчины и разрушению металлических конструкций. Понимание принципов взаимодействия металла с водой и процессов коррозии позволяет разрабатывать методы защиты от коррозии, такие как покрытия и антикоррозионные покрытия. Также изучение металлической коррозии имеет большое значение для разработки новых материалов и улучшения существующих технологий в различных областях науки и промышленности.
Роль металла в водообразовании

Металлы играют важную роль в процессе образования воды, так как они способны взаимодействовать с водными молекулами и претерпевать химические реакции.
Одним из проявлений взаимодействия металла и воды является коррозия. Металлы могут реагировать с водой, приводя к образованию оксидов или гидрооксидов металлов. Например, реакция железа с водой приводит к образованию гидроксида железа, который является одним из компонентов ржавчины.
Наиболее активными металлами в реакции с водой являются щелочные и щелочноземельные металлы. Они способны образовывать гидроксиды металлов и водород. Например, натрий реагирует с водой, образуя гидроксид натрия и выделяя водородный газ.
Металлы также могут быть использованы в качестве катализаторов при процессе электролиза воды. Например, платина и родий обладают высокой активностью и стабильностью в электролитической реакции, что позволяет увеличить эффективность процесса разложения воды на водород и кислород.
Взаимодействие металла и воды может иметь и другие проявления, которые зависят от химических свойств и структуры конкретного металла. Исследование этих взаимодействий позволяет расширить наши знания о химических реакциях и разработать новые технологии в области производства воды и энергии.
Принципы взаимодействия
Процесс образования воды при взаимодействии металлов основан на принципах электрохимии. Когда металл вступает в реакцию с водной средой, происходит окисление его атомов. Окисление металла сопровождается выделением электронов, которые поступают на электродный материал. В то же время, вода восстанавливается, т.е. принимает электроны и происходит образование молекулы воды.
Окислительные свойства металла играют важную роль в этом процессе. Металлы с более высокими окислительными свойствами (например, натрий, калий, литий) способны активно реагировать с водой, образуя гидроксиды и высвобождая большое количество энергии. Металлы с более низкими окислительными свойствами (например, железо, цинк) взаимодействуют с водой более медленно и менее активно.
На скорость реакции взаимодействия металла с водой также влияют условия проведения эксперимента: концентрация металла в растворе, температура среды, физическое состояние металла (порошок, фольга). Также важно отметить, что реакция с водой может происходить с образованием различных соединений, например, при взаимодействии железа с кислородом из воды образуется ржавчина.
Химическая реакция металла и воды
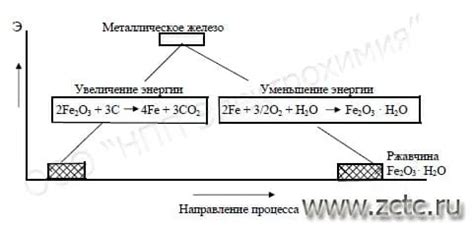
Химическая реакция между металлами и водой является основой для многих процессов в природе и промышленности. Когда металл контактирует с водой, происходит серия химических изменений, результатом которых является образование водорода и гидроксида металла.
Взаимодействие металла с водой связано с окислительно-восстановительными реакциями, где металл служит восстановителем, а вода - окислителем. Металл отдает электроны воде, образуя положительно заряженные ионы, а вода принимает электроны, превращаясь в отрицательно заряженные ионы гидроксида.
Реакции между металлами и водой могут проходить различными способами в зависимости от свойств металла и условий реакции. Некоторые металлы, такие как натрий и калий, очень активны и реагируют с водой достаточно быстро, выбрасывая пузырьки водорода и разлагаясь. Другие металлы, такие как железо и алюминий, могут требовать специальных условий, чтобы реакция прошла с нужной скоростью.
Понимание принципов химической реакции металла с водой позволяет улучшать процессы производства, разрабатывать новые материалы и технологии, а также прогнозировать поведение металлов в природных условиях. Благодаря этому знанию, можно избегать нежелательных последствий взаимодействия металла и воды, таких как коррозия и разрушение материалов.
Влияние металла на процесс образования воды

Металлы играют важную роль в процессе образования воды, так как они способны участвовать в химических реакциях, которые приводят к образованию этого вещества. Один из ключевых процессов, при котором металл влияет на образование воды, - это реакция металла с водой.
В результате реакции металла с водой образуется гидроксид металла и выделяется водород. Эта реакция особенно хорошо проявляется, если металл активный, например, натрий или калий. При реакции с водой активные металлы выделяются большое количество водорода, что делает процесс образования воды заметным и способствует его эффективности.
Также металлы могут использоваться в качестве катализаторов в реакциях образования воды. Катализатор - это вещество, которое ускоряет химическую реакцию, но само не участвует в ней. Например, платина может использоваться в катализаторах, которые способствуют реакции образования воды из водорода и кислорода.
Кроме того, некоторые металлы могут взаимодействовать с водой за счет своих электрохимических свойств. Например, в процессе электролиза, медь может выделяться на аноде, а вода превращаться в водород и кислород под воздействием электрического тока. Этот процесс можно использовать для получения воды из водных растворов металлов.
Таким образом, металлы оказывают значительное влияние на процесс образования воды благодаря своим химическим и электрохимическим свойствам. Они могут участвовать в реакциях с водой, выделяться в процессе образования гидроксида и водорода, а также использоваться в качестве катализаторов для ускорения образования воды.
Виды металлов, образующих воду

Металлы - это элементы, которые образуют ионы положительного заряда в растворах. Большинство металлов, взаимодействуя с водой, могут образовывать различные соединения, включая оксиды, гидроксиды и соли.
Один из наиболее распространенных металлов, образующих воду, - это натрий. При взаимодействии натрия с водой образуется гидроксид натрия (NaOH) и выделяется водородный газ. Эта реакция является очень активной и протекает с выделением большого количества тепла.
Еще одним металлом, способным образовывать воду, является калий. Когда калий взаимодействует с водой, образуется гидроксид калия (KOH) и выделяется водород. Реакция между калием и водой также является интенсивной и происходит с выделением тепла.
Алюминий - еще один металл, способный образовывать воду. При контакте алюминия с водой происходит окисление металла, образуется гидроксид алюминия (Al(OH)3) и выделяется водород. Эта реакция обычно протекает медленно, так как на поверхности алюминия образуется защитная оксидная пленка.
Также следует упомянуть металлы, которые взаимодействуют с водой, образуя щелочные растворы. Например, магний образует гидроксид магния (Mg(OH)2), а кальций - гидроксид кальция (Ca(OH)2). Эти металлы являются щелочными и обладают антикислотными свойствами.
В целом, существует множество металлов, способных образовывать воду. Каждый из них имеет свои характеристики и свойства при контакте с водой. Изучение этих реакций позволяет лучше понять взаимодействие металлов и воды, а также применить эти знания в различных областях науки и техники.
Металлы, не образующие воду

Вода образуется в результате химической реакции между металлами и кислородом. Однако не все металлы способны образовывать воду при взаимодействии с воздухом или водой.
Некоторые металлы, такие как золото и платина, не проявляют химической активности и не реагируют с кислородом или водой. Их поверхность остается стабильной и не окисляется в контакте с водой, что делает их хорошими материалами для производства украшений и электроники.
Другие металлы, такие как свинец и медь, могут образовывать оксиды при взаимодействии с кислородом, но не образуют воду. Например, свинец образует оксид свинца (PbO), а медь образует оксид меди (CuO). Эти оксиды могут быть использованы в различных промышленных процессах и производствах.
Некоторые металлы, такие как железо и алюминий, образуют воду при взаимодействии с кислородом или водой. Это происходит благодаря присутствию в их структуре активных атомов, способных образовывать химические связи с кислородом. Железо образует оксид железа (Fe2O3), алюминий образует оксид алюминия (Al2O3). При контакте с водой эти оксиды реагируют, образуя воду и освобождая энергию в процессе.
Способы ускорения реакции образования воды с металлом
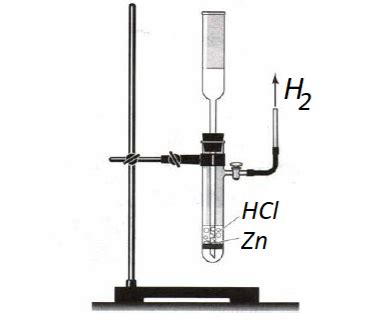
Образование воды с металлом может быть ускорено различными способами, которые изменяют скорость химической реакции или облегчают протекание процесса. Некоторые из этих способов включают:
- Использование катализаторов: Катализаторы - это вещества, которые ускоряют химическую реакцию, не изменяя своей структуры и не участвуя в конечном продукте. Добавление катализатора может значительно повысить скорость образования воды с металлом.
- Увеличение поверхности реагирующих веществ: Увеличение поверхности металла и воды может привести к ускорению реакции, так как большая площадь контакта с реагентами увеличивает вероятность их взаимодействия.
- Изменение концентрации реагентов: Изменение концентрации металла или воды в реакционной среде может повлиять на скорость образования воды. Повышенная концентрация одного из реагентов может способствовать быстрой реакции.
- Изменение температуры: Температура - важный фактор, влияющий на скорость химической реакции. Повышение или понижение температуры может ускорить или замедлить образование воды с металлом, в зависимости от конкретной реакции.
- Использование агентов активации: Некоторые вещества, называемые агентами активации, могут использоваться для стимулирования реакции образования воды с металлом. Они помогают разрушить химические связи и позволяют реагентам взаимодействовать более эффективно.
Для ускорения реакции образования воды с металлом можно применять как отдельные способы, так и комбинировать несколько из них. Эксперименты с определением оптимальных условий для данной реакции могут проводиться, чтобы достичь наибольшей эффективности процесса образования воды.
Применение химической реакции водообразования в промышленности

Химическая реакция водообразования, также известная как реакция металла с водой, имеет широкое применение в промышленных процессах. Эта реакция основана на химических свойствах различных металлов, которые образуют водород и гидроксиды при контакте с водой.
В промышленности химическая реакция водообразования используется для получения водорода, который затем может быть использован в ряде процессов, включая производство аммиака, реформирование пара и другие процессы, требующие высокоэффективного источника водорода.
Кроме того, реакция металла с водой может быть использована для очистки воды. Металлы, такие как железо, алюминий и магний, реагируют с загрязнениями воды и удаляют их из раствора. Этот процесс, известный как коагуляция, используется в промышленности для очистки сточных вод и обработки питьевой воды.
Кроме того, химическая реакция водообразования может быть использована для создания сильных щелочных сред. Гидроксиды некоторых металлов, таких как калий и натрий, являются базами и используются в производстве мыла, стекла, щелочей и других продуктов.
В заключение, химическая реакция водообразования имеет широкое применение в промышленности. Она используется для получения водорода, очистки воды и создания щелочных сред. Эта реакция является одной из основных и важных химических реакций, которая играет значительную роль в различных промышленных процессах.
Вопрос-ответ

Как металл образует воду?
Металл образует воду путем химической реакции с водой. Водород, который находится в металле, выделяется и соединяется с кислородом из воды, образуя молекулы воды.
Какие принципы взаимодействия действуют при образовании воды металлом?
Взаимодействие металла с водой происходит благодаря электрохимическим принципам. Металлы, такие как натрий, калий, литий и другие, имеют высокую химическую активность. При погружении металла в воду их атомы отдают электроны, образуя положительно заряженные ионы. Процесс образования воды возникает, когда водородные ионы вступают в реакцию с кислородом из воды, образуя молекулы воды.
Какая химическая реакция происходит при образовании воды металлом?
Химическая реакция, происходящая при образовании воды металлом, называется реакцией металла с водой. В этой реакции металл отдаёт электроны и образует положительно заряженные ионы. В то же время вода разлагается на водородные и оксидные ионы. Водородные ионы соединяются с электронами, отданными металлом, и образуют молекулы воды.
