Металлы активно реагируют с кислотами, проявляя различные признаки и явления. Основными проявлениями такой реакции являются образование солей, выделение газа и эволюция тепла. Эти процессы обусловлены специфическими механизмами, в результате которых происходит переход электронов и ионов
В процессе взаимодействия металла с кислотой образуется соль металла и вода. Образование соли связано с тем, что металлический ион (катион) замещает ион водорода, который является основной составляющей кислоты. Это приводит к образованию ионного соединения – соли. Например, взаимодействие цинка с соляной кислотой приводит к образованию хлорида цинка и выделению водорода:
Zn + 2HCl → ZnCl2 + H2 ↑
Помимо образования соли, в процессе реакции металла с кислотой происходит выделение газа. В большинстве случаев этот газ является водородом. Возникновение газа связано с разложением воды, образующейся в результате реакции металла с кислотой. Газ выделяется в виде пузырьков и может быть уловлен специальными приспособлениями. Например, при реакции магния с соляной кислотой выделяется водородный газ:
Mg + 2HCl → MgCl2 + H2 ↑
Кроме того, в процессе реакции металла с кислотой происходит эволюция тепла. Образование соли и выделение газа являются экзотермическими процессами, то есть сопровождаются выделением тепла. Интенсивность выделения тепла может различаться в зависимости от характера реакционных компонентов. Например, реакция железа с серной кислотой сопровождается сильным выделением тепла:
Fe + H2SO4 → FeSO4 + H2 ↑ + тепло
Таким образом, проявления реакции металлов с кислотами включают образование соли, выделение газа и эволюцию тепла. Эти процессы являются результатом специфических механизмов, включающих переход электронов и ионов. Понимание данных проявлений и механизмов реакции металлов с кислотами имеет важное значение в различных областях науки и техники.
Основные проявления реакции металлов с кислотами
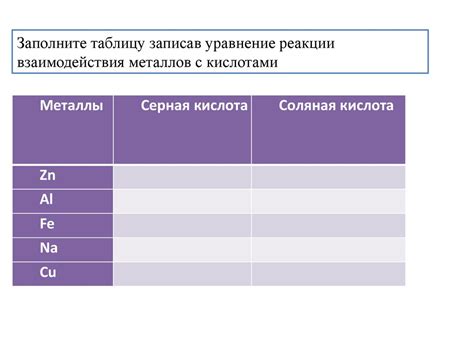
1. Образование солей металлов
Реакция металлов с кислотами приводит к образованию солей, которые являются основными продуктами этой химической реакции. Соли металлов обычно обладают кристаллической структурой и имеют характерные физические и химические свойства.
2. Выделение водорода
Реакция металлов с кислотами часто сопровождается выделением водорода. В результате этой реакции происходит разложение кислоты на ионы водорода и соответствующие анионы. При этом ионы металла вступают в соединение с анионами кислоты, образуя соответствующий соль металла.
3. Изменение окраски раствора
Реакция металлов с кислотами может привести к изменению окраски раствора. Например, при реакции железа с серной кислотой образуется раствор с железным катионом, который имеет характерный ярко-желтый цвет. Изменение окраски раствора может быть использовано для определения или идентификации металлов.
4. Выделение тепла
Реакция металлов с кислотами обычно является экзоэнергической, то есть сопровождается выделением тепла. Это связано с энергетическими изменениями, происходящими в результате образования связей между атомами и молекулами продуктов реакции. Выделение тепла может быть замечено в виде повышения температуры смеси во время реакции.
Проявление реакции в виде образования солей

Реакция металлов с кислотами проявляется в образовании солей. Соли являются реакционными продуктами в данном типе химических реакций.
Соли, образующиеся при реакции металлов с кислотами, имеют общее строение, а именно ионное. В ионной решетке содержатся положительные ионы металла и отрицательные ионы кислотного остатка.
Признаком образования солей при реакции металлов с кислотами является выпадение осадка или появление нового вещества в растворе. Соли обладают характерными физическими свойствами, такими как твёрдость, растворимость в воде и точка плавления.
Реакция металлов с кислотами, в результате которой образуются соли, может протекать с различным интенсивностью и скоростью. Она может сопровождаться выделением газа, образованием пены или изменением цвета раствора.
Механизмы реакции металлов с кислотами
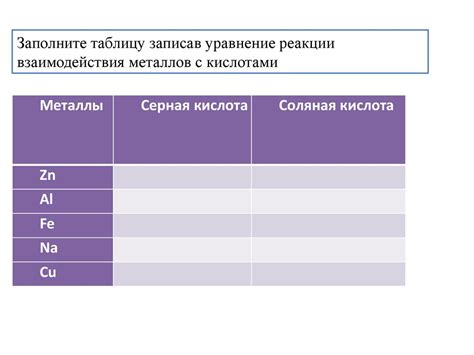
Взаимодействие металлов с кислотами является одной из основных реакций, которые могут происходить между химическими веществами. При этом происходят различные механизмы, которые определяют характер проявления реакции и образование соответствующих соединений.
Одним из основных механизмов реакции металлов с кислотами является образование водорода. В этом случае молекулы кислоты разлагаются на ионы водорода и анионы кислоты. Металл вступает в реакцию с ионами водорода, образуя соответствующие металлические ионы и молекулы воды.
Ещё одним механизмом реакции металлов с кислотами является образование солей. В этом случае ионы металла и ионы кислоты образуют соединение, которое называется солью. При этом металл вытесняет водород из кислоты, а само металлическое соединение образует нагромождение частиц, которые могут быть различной структуры, формы и цвета.
Некоторые металлы также проявляют реакцию с кислотами через образование окислов. В этом случае металл окисляется, а кислород входит в реакцию с металлическим ионом, образуя соответствующий оксид металла. Окислы металлов приобретают различные свойства и используются в различных областях промышленности и научных исследований.
Вопрос-ответ

Какие металлы реагируют с кислотами?
Многие металлы реагируют с кислотами, включая активные металлы, такие как натрий, калий, магний, алюминий, цинк, железо, а также менее активные металлы, такие как медь, серебро и золото.
Какие признаки реакции металлов с кислотами можно наблюдать?
Во время реакции металлов с кислотами можно наблюдать следующие признаки: выделение пузырьков газа, изменение цвета раствора, образование осадка или изменение внешнего вида металла.
Какой механизм протекает при реакции металлов с кислотами?
Реакция металлов с кислотами протекает по схеме: металл + кислота → соль + гидроген. Металл отдает электроны и образует положительные ионы, которые соединяются с отрицательными ионами кислоты, образуя соль. При этом в процессе реакции выделяется газ - водород.
Какие кислоты могут реагировать с металлами?
Многие кислоты могут реагировать с металлами, но наиболее распространенными являются соляная кислота (HCl) и серная кислота (H2SO4). Также реакцию можно наблюдать с азотной кислотой (HNO3) и уксусной кислотой (CH3COOH).
