Металлы - это химические элементы, которые обладают отличными проводящими свойствами, высокой пластичностью и металлическим блеском. Они играют важную роль во многих сферах нашей жизни, от строительства до производства электроники. Металлы обычно хорошо взаимодействуют с кислотами, образуя соли и выделяя водородный газ.
Рассмотрим несколько примеров металлов и их реакции с водной кислотой. Одним из самых известных металлов является железо. Оно активно реагирует с сильными кислотами, такими как соляная кислота (HCl) или серная кислота (H2SO4), образуя соответствующие соли и выделяя водород. Реакция железа с соляной кислотой можно записать следующим образом:
Fe + 2HCl → FeCl2 + H2
Еще одним примером металла, который реагирует с водной кислотой, является алюминий. При взаимодействии алюминия с кислородной кислотой, например, соляным раствором серной кислоты, образуется алюминийсульфат и водородный газ:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Таким образом, реакция металлов с водными кислотами является важной и широко распространенной в химических процессах. Она позволяет получить различные соединения металлов и использовать их в различных сферах промышленности и науки.
Примеры металлов и их реакция с водной кислотой
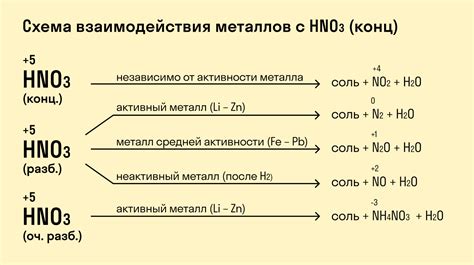
Металлы являются хорошими проводниками электричества и тепла и могут иметь различные свойства при взаимодействии с водной кислотой. Некоторые металлы, такие как железо и цинк, реагируют с водной кислотой, образуя соответствующие соли и выделяя водородный газ:
- Железо (Fe): Взаимодействие железа с водной кислотой, например с соляной кислотой (HCl), приводит к образованию хлорида железа (FeCl2) и выделению водородного газа (H2).
- Цинк (Zn): При реакции цинка с водной кислотой образуется сульфат цинка (ZnSO4) и выделяется водородный газ.
Однако, не все металлы реагируют одинаково с водной кислотой. Например, никель и платина не реагируют с обычной водной кислотой. Кроме того, некоторые металлы, такие как алюминий и медь, могут реагировать с водной кислотой, но при этом образовывают защитную пленку на своей поверхности, которая предотвращает дальнейшую реакцию металла с кислотой.
Реакции металлов с водной кислотой широко используются в химической промышленности и лабораториях для получения различных продуктов и солей. Кроме того, изучение этих реакций является важной частью обучения по химии, так как позволяет понять свойства и реактивность различных металлов.
Металл железо и его реакция с водной кислотой
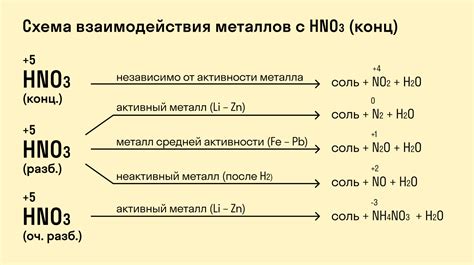
Железо (Fe) является одним из наиболее распространенных металлов на Земле. Оно обладает высокой прочностью и стойкостью к коррозии, что делает его очень популярным материалом в различных отраслях промышленности.
Едкость и коррозионную устойчивость железа можно проверить, используя водную кислоту (серную кислоту H2SO4, разбавленную в воде). При контакте железа с водной кислотой происходит реакция, выделяющая водородный газ и образующая сульфат железа (FeSO4).
Реакция металла железа с водной кислотой проходит по следующей схеме:
- Fe + H2SO4 → FeSO4 + H2↑
В результате этой реакции металлическая поверхность железа покрывается слоем сульфата железа, который может быть очень плотным и защитным, предотвращая дальнейшую коррозию металла. Однако, при продолжительном воздействии водной кислоты, железо может раствориться и образовать растворимые соли.
Поэтому важно следить за состоянием поверхности металла и обеспечивать ее защиту от коррозии, например, путем нанесения защитных покрытий или использования антикоррозийных средств.
Металл алюминий и его реакция с водной кислотой

Алюминий – легкий металл серого цвета, который активно реагирует с водной кислотой.
При контакте алюминия с водной кислотой, образуется гидроген. Реакция происходит следующим образом: алюминий окисляется при взаимодействии с водородом из кислоты, при этом образуется соль и выделяется взрывоопасный газ - водород. Реакция сопровождается эволюцией пузырьков газа.
В результате реакции алюминий уничтожается, образуя гидроксид соли, растворимый в воде. При этом водород, отделяющийся во время реакции, образует взрывоопасные смеси с воздухом.
Необходимо отметить, что реакция алюминия и водной кислоты протекает достаточно быстро, и эволюция газа происходит интенсивно.
Алюминий широко используется в промышленности и в быту. Он представляет собой весьма полезный материал благодаря своим свойствам, особенно легкости и прочности. Однако, при работе с алюминием необходимо обращать внимание на его реакцию с водной кислотой и предпринимать соответствующие меры безопасности.
Металл медь и ее реакция с водной кислотой

Медь – один из самых распространенных металлов на Земле. Она обладает высокой электропроводимостью, химической стабильностью и привлекательным внешним видом. Медь широко используется в промышленности, строительстве, электронике и других отраслях.
Вода и кислота не вызывают существенных изменений в структуре и свойствах меди при обычных условиях. Однако при взаимодействии меди с водной кислотой происходит химическая реакция.
Медь реагирует с различными видами водных кислот, включая серную, соляную и азотную. В результате реакции образуется соответствующий соль меди, а избыток водорода выделяется в виде газа.
Процесс реакции меди с водной кислотой можно описать следующей химической формулой: Cu + 2H+ → Cu2+ + H2↑.
Таким образом, реакция меди с водной кислотой приводит к образованию соли меди и выделению водорода в газообразном состоянии. Эта реакция имеет практическое значение и используется, например, при получении солей меди и в процессе очистки и омеднения поверхностей металла.
Металл цинк и его реакция с водной кислотой

Цинк – это металл из группы переходных элементов, обладающий серебристо-серым цветом. Он отличается высокой прочностью и устойчивостью к коррозии. Цинк широко используется в промышленности, особенно в производстве листового металла и гальванических покрытий.
Когда цинк вступает в реакцию с водной кислотой, например, с соляной или серной кислотой, происходит химическое взаимодействие с образованием газа водорода и соответствующих солей. Реакция может быть представлена химическим уравнением:
Zn + 2HCl → ZnCl2 + H2
В результате реакции образуется хлорид цинка (ZnCl2) и молекулы водорода (H2). Водород выделяется в виде пузырьков газа, который можно увидеть в процессе проведения эксперимента.
Интересно отметить, что цинк реагирует с кислотами, образуя соли, входящие в состав гальванического элемента. Благодаря этому свойству, цинк находит применение в производстве батареек и аккумуляторов.
Металл свинец и его реакция с водной кислотой

Свинец (Pb) – тяжелый металл серого цвета, который обладает высокой пластичностью и коррозионной стойкостью. Свинец используется в различных отраслях, включая строительство, электронику и автомобильную промышленность.
Реакция металла свинца с водной кислотой является химической реакцией, которая протекает по следующей схеме:
- Свинец реагирует с водной кислотой (H2O) и образует соль свинца и водородный газ:
2Pb + 2H2O -> Pb(OH)2 + H2
Образующийся водородный газ при этой реакции обладает высокой воспламеняемостью, поэтому реакцию следует проводить с осторожностью и в хорошо проветриваемом помещении.
Металл свинец довольно реактивен с кислотами, поэтому его использование в контакте с кислотными средами может привести к образованию токсичных соединений. В связи с этим, необходимо соблюдать меры предосторожности при обращении с свинцом и водной кислотой.
Вопрос-ответ

Какие металлы реагируют с водной кислотой?
Реакция металлов с водной кислотой имеет сложное химическое уравнение, но в целом многие металлы могут реагировать с ними. Например, активные металлы, такие как натрий, калий и литий, реагируют с водной кислотой, образуя гидроксид металла и выделяя водородный газ. Некоторые более реактивные металлы, такие как алюминий и цинк, могут реагировать с разбавленной кислотой, такой как соляная кислота.
Какие продукты образуют металлы при реакции с водной кислотой?
Реакция металлов с водной кислотой приводит к образованию продуктов, которые зависят от типа металла и кислоты. Обычно, металл реагирует с кислотой, образуя гидроксид металла и выделяя водородный газ. Например, реакция натрия с соляной кислотой приводит к образованию хлорида натрия, воды и выделению водорода.
Какие факторы влияют на скорость реакции металлов с водной кислотой?
Скорость реакции металлов с водной кислотой зависит от нескольких факторов. Одним из них является активность металла. Более активные металлы, такие как натрий и калий, реагируют быстрее с водной кислотой. Также важно обратить внимание на концентрацию кислоты и температуру. Более концентрированная кислота и повышенная температура могут ускорить реакцию.
Какие металлы не реагируют с водной кислотой?
Не все металлы реагируют с водной кислотой. Например, металлы, такие как серебро и золото, являются неактивными и не реагируют с водной кислотой. Это связано с их низкой реактивностью и стабильностью.
