Серная кислота – это один из самых распространенных и важных химических соединений. Она широко используется в промышленности и лабораториях, являясь основным промышленным источником серы и других связанных с ней продуктов.
Однако при взаимодействии металлов с серной кислотой происходят химические реакции, которые могут привести к различным результатам. Большинство металлов могут реагировать с серной кислотой, образуя соли металлов и выделяя сероводород. Однако, есть и такие металлы, которые не реагируют с серной кислотой или реагируют медленно и с большими трудностями.
Основная причина невозможности получения металлов при взаимодействии с серной кислотой заключается в ее агрессивности и окислительных свойствах. Серная кислота обладает высокой кислотностью и способна окислять вещества. Поэтому, когда металлы взаимодействуют с серной кислотой, происходит окисление металла и выделение сероводорода.
Таким образом, невозможность получения металлов при взаимодействии с серной кислотой обусловлена их химическими свойствами и способностью к окислению. Это необходимо учитывать при проведении химических экспериментов и выборе реагентов для получения металлов.
Почему металлы не получаются при взаимодействии с серной кислотой?
Когда металлы взаимодействуют с серной кислотой, обычно не происходит получение металлов. Это связано с химическими свойствами серной кислоты и ее влиянием на металлы.
Серная кислота, или H2SO4, является одним из самых сильных кислотных веществ. Она обладает способностью окислять металлы, т.е. принимать электроны от металла и превращать его в ион. Однако, взаимодействуя с некоторыми металлами, серная кислота не способна получить металлическое состояние.
При взаимодействии с серной кислотой некоторые металлы проявляют пассивность или инертность кислоте. Это значит, что кислота не может расщепить металл на ионы и вступить с ними в реакцию, чтобы получить металлическое состояние. Такие металлы являются химически стойкими и не выделяются из серной кислоты в виде ионов металла.
Некоторые из таких пассивных металлов, которые не получаются при взаимодействии с серной кислотой, включают алюминий, хром, железо, цинк и свинец. Эти металлы обладают защитными слоями оксида, сульфида или других соединений на своей поверхности, которые предотвращают дальнейшее реагирование с серной кислотой.
Химический процесс

Интеракция металлов с серной кислотой осуществляется на основе химического процесса, который приводит к образованию сульфатов металлов и выделению диоксида серы. Данный процесс представляет собой типичную реакцию окисления-восстановления, где металл окисляется, а сера восстанавливается.
При контакте металла с серной кислотой происходит ионный обмен, когда ионы металла замещают ионы водорода в составе серной кислоты. В результате образуются сульфаты металлов и освобождаются молекулы диоксида серы. Такой процесс наблюдается, например, при растворении цинка в серной кислоте
Металлы, такие как железо, алюминий или магний, не растворяются в серной кислоте из-за образования защитной пленки оксида на поверхности металла. Эта оксидная пленка не позволяет кислоте проникать внутрь и взаимодействовать с металлом, что делает невозможным очередное окисление металла и дальнейшую реакцию. Таким образом, металлический образец остается неприкосновенным при воздействии серной кислоты.
Реакционные свойства серной кислоты
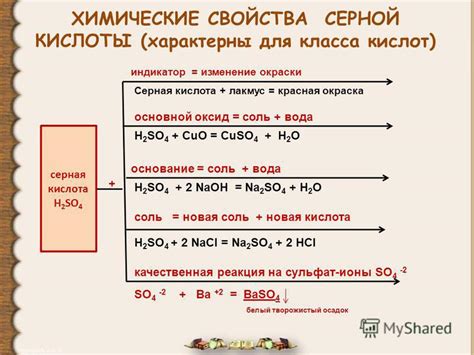
Серная кислота - одна из наиболее распространенных и важных химических соединений. Она обладает широким спектром реакционной активности, что делает ее ценным источником для множества промышленных процессов. Рассмотрим основные реакционные свойства серной кислоты.
1. Окислительные свойства: серная кислота является сильным окислителем. При взаимодействии с некоторыми веществами она способна передавать кислородные атомы, окисляя их. Так, она способна окислять металлы, освобождая молекулярный кислород. Однако, не все металлы реагируют с серной кислотой.
2. Взаимодействие с основаниями: серная кислота является сильной кислотой и реагирует с основаниями, образуя соль и воду. Примером может служить реакция серной кислоты с гидроксидом натрия:
H2SO4 + 2NaOH → Na2SO4 + 2H2O
3. Образование сульфатов: серная кислота реагирует с многими металлами, образуя сульфаты – соли серной кислоты. Образование сульфатов можно использовать для определения наличия или отсутствия определенного металла в растворе.
4. Действие на органические соединения: серная кислота является сильным дегидратирующим агентом и может образовывать эфиры с органическими соединениями. Также она может реагировать с алкенами, образуя сульфаты (эфиры серной кислоты).
5. Реакция с нитратами: серная кислота образует нитросоединения при взаимодействии с нитратами. Например, при взаимодействии с нитратом серебра образуется серебряная серная кислота (AgNO3 + H2SO4 → AgHSO4 + HNO3).
Таким образом, серная кислота проявляет широкий спектр реакционной активности, что позволяет использовать ее в различных химических процессах и промышленных производствах.
Агрессивность серной кислоты

Серная кислота (H2SO4) является одним из самых распространенных и агрессивных химических веществ. Ее агрессивность обусловлена ее способностью реагировать с различными веществами и оказывать разрушительное влияние на многие материалы.
Взаимодействие серной кислоты с металлами является одним из примеров проявления ее агрессивности. При взаимодействии с серной кислотой большинство металлов производят водород, который образует газовую смесь с кислотой. Это приводит к образованию пузырьков, активного выделения тепла и возможности разбрызгивания кислоты.
Серная кислота также способна реагировать с окислами, при этом образуется сильно окрашенный и коррозийно-активный газ - диоксид серы (SO2). Это обусловлено высокой оксидирующей способностью серной кислоты, что является еще одним примером ее агрессивности.
Из-за своей агрессивности серная кислота обладает высоким риском для здоровья и безопасности. При работе с ней необходимо соблюдать особые меры предосторожности, такие как ношение защитной экипировки и проведение работ в специально оборудованных помещениях.
Коррозия металлов

Коррозия металлов - это процесс взаимодействия металла с окружающей средой, который приводит к его разрушению и образованию окисленных продуктов. Отсюда следует, что контакт металла с агрессивными субстанциями, такими как кислоты, может вызвать коррозию.
Кислоты, такие как серная кислота (H2SO4), могут быть крайне опасными для различных металлов. Взаимодействие металла с серной кислотой приводит к образованию сульфатов металлов и выделению водорода. В результате этого процесса металл разрушается и теряет свои характеристики.
Например, железо (Fe), которое является одним из самых распространенных металлов, может подвергнуться коррозии при взаимодействии с серной кислотой. При этом образуется сульфат железа (FeSO4), который может быть виден в виде отложений или ржавчины на поверхности металла.
Важно отметить, что не все металлы подвержены коррозии при контакте с серной кислотой. Например, алюминий (Al) обладает защитной пленкой оксида, которая образуется на его поверхности и предотвращает дальнейшую коррозию. Однако другие металлы, такие как цинк (Zn) или медь (Cu), могут быть более подвержены коррозии при взаимодействии с серной кислотой.
В целом, коррозия металлов является важной проблемой, которая требует внимания и предпринимаемых мер для предотвращения. Это может включать в себя использование защитных покрытий или специальных материалов, которые могут устойчиво сопротивляться агрессивным средам, таким как серная кислота.
Образование соединений

Взаимодействие металлов с серной кислотой приводит к образованию различных соединений и реакционных продуктов. Серная кислота (H2SO4) является сильной кислотой и обладает способностью окислять металлы. При взаимодействии с металлами серная кислота образует соли, сульфаты металлов, и выделяет молекулярный водород.
При взаимодействии активных металлов, таких как натрий, калий, магний, серная кислота выделяет водородный газ и образует сульфаты этих металлов. Например, взаимодействие натрия с серной кислотой приводит к образованию натрия гидрогенсульфата (NaHSO4):
- 2 Na + H2SO4 → Na2SO4 + 2 H2
Активные металлы, такие как железо, алюминий, медь и цинк, также могут реагировать с серной кислотой, но образуются соединения другого типа - сульфаты металлов. Например, при взаимодействии железа и серной кислоты образуется железный сульфат (FeSO4):
- Fe + H2SO4 → FeSO4 + H2
Таким образом, взаимодействие металлов с серной кислотой приводит к образованию различных соединений, в зависимости от химической активности металла и условий реакции. Эти реакции являются химическими иллюстрациями принципа окислительно-восстановительных реакций.
Практическое применение

Невозможность получения металлов при взаимодействии с серной кислотой имеет прямое практическое значение в различных отраслях промышленности и научных исследованиях.
В процессе производства и обработки металлов использование серной кислоты может привести к непредсказуемым результатам и значительным материальным потерям. Например, при попытке обработки металлов серной кислотой она может растворить их, образуя соединения, которые не являются ценными или применимыми в дальнейшей обработке.
В лабораторных исследованиях невозможность получения металлов при взаимодействии с серной кислотой может быть полезной особенностью. Она позволяет исследователям устанавливать границы действия и взаимодействия различных веществ с металлами, а также создавать методы и приборы, которые основаны на этой невозможности.
Также данное явление может использоваться в качестве препятствия для предотвращения коррозии металлических конструкций. В частности, при использовании серной кислоты в производстве и транспортировке нефти и газа, невозможность взаимодействия металлов с серной кислотой позволяет снизить риск разрушения трубопроводов и оборудования, что является важным фактором для обеспечения безопасности и надежности процесса транспортировки и хранения нефтепродуктов.
Вопрос-ответ

Почему нельзя получить металлы при взаимодействии с серной кислотой?
Взаимодействие металлов с серной кислотой приводит к образованию сульфатов металлов, которые не являются металлическими элементами. Это происходит из-за того, что серная кислота обладает окислительными свойствами и способна окислять металлы, превращая их в ионы металла соответствующего металлического сульфата.
Что происходит при реакции металлов с серной кислотой?
При реакции металлов с серной кислотой происходит окисление металлов и образование ионов металла соответствующего сульфата. Например, при взаимодействии железа (Fe) с серной кислотой (H2SO4) образуется сульфат железа (FeSO4) и выделяется водород (H2).
Почему взаимодействие металлов с серной кислотой приводит к образованию сульфатов?
Сульфаты образуются, потому что кислота является окислителем и способна окислить металлы, превращая их в ионы металла, который соединяется с ионами серы (SO4^2-) и образует сульфаты. Такое взаимодействие металла и кислоты ведет к образованию сульфатов металлов.
Какие металлы не реагируют с серной кислотой?
Некоторые металлы, такие как золото (Au), серебро (Ag) и платина (Pt), не реагируют с серной кислотой. Эти металлы обладают очень низкой реакционной способностью и устойчивы к окислению, поэтому не образуют сульфатов при контакте с серной кислотой.
Есть ли способ получить металлы из сульфатов?
Да, сульфаты металлов могут быть восстановлены обратно в металлы с помощью различных методов. Например, электролиз может использоваться для восстановления металлических ионов из раствора сульфатов металлов. Также возможен использование химических реакций восстановления, где вещества с высокой реакционной способностью передают электроны металлическим ионам, восстанавливая их обратно в металлы.
