Электрохимическое полирование является одним из методов обработки металлических поверхностей, при котором происходит удаление неровностей и поверхностных слоев металла под воздействием электрического тока. Этот процесс основан на электролизе, который происходит в электролите при наличии постоянного тока.
В ходе электрохимического полирования металла на поверхности изделия происходит окислительно-восстановительная реакция. При этом, на катоде металлической поверхности происходит растворение металла, а на аноде, обычно изготовленном из инертного материала, такого как платина, происходит электролиз воды, что приводит к образованию водорода и кислорода. Таким образом, процесс электрохимического полирования металла подразумевает связку электрохимических реакций, происходящих в определенной среде.
Одним из основных преимуществ электрохимического полирования поверхности металла является возможность получения идеально ровной поверхности без механической обработки. При этом, качество и эффективность полирования зависят от многих факторов, включая состав электролита, протекающих электрохимических реакций, параметры электрического тока и время обработки. Использование электрохимического полирования позволяет добиться высокой точности и чистоты поверхности металла, использование данного метода особенно актуально в производстве высокоточных приборов, электроники и медицинского оборудования.
Процесс электрохимического полирования
Электрохимическое полирование является эффективным способом обработки поверхностей металлических изделий с целью улучшения их внешнего вида и функциональных характеристик. Данный метод основывается на использовании электролитической реакции, происходящей между поверхностью металла и электролитом под воздействием электрического тока.
Процесс электрохимического полирования осуществляется в специальных емкостях, называемых электролитическими ваннами. В этих ваннах металлическое изделие, которое требуется полировать, погружается в электролит, состоящий из раствора кислоты или щелочи. Подводится электрический ток, который инициирует реакцию на поверхности металла.
Во время электрохимического полирования происходит процесс окисления и редукции на поверхности металла. Как результат, происходит удаление неровностей, отложений и загрязнений с поверхности, и она становится более гладкой и блестящей. Важным фактором в данном процессе является правильное подбор напряжения, тока и прочих параметров, которые определяют интенсивность и качество полировки.
Электрохимическое полирование находит применение в различных отраслях промышленности и научных исследованиях. Оно используется для полировки металлических поверхностей разных материалов, включая сталь, алюминий, медь и другие. Этот процесс широко применяется при производстве автомобилей, техники, электроники, медицинских приборов и других изделий.
Химический состав реакционной среды

Химический состав реакционной среды при электрохимическом полировании поверхности металла имеет решающее значение для процесса полирования и получения желаемого результата.
Основным компонентом реакционной среды является электролит, состоящий из раствора кислоты, щелочи или соли. Кислотные электролиты, такие как серная кислота или соляная кислота, обеспечивают кислую среду, которая обладает растворяющими свойствами и способствует удалению окисленных слоев и примесей с поверхности металла. Щелочные электролиты, такие как гидроксид натрия или гидроксид калия, создают щелочную среду, которая обладает структурирующими и смягчающими свойствами, способствуя выравниванию поверхности металла.
В состав реакционной среды могут также входить добавки, такие как ингибиторы коррозии, комплексообразующие вещества и поверхностно-активные вещества. Ингибиторы коррозии предназначены для защиты металла от нежелательной коррозии во время процесса полирования. Комплексообразующие вещества используются для образования комплексных соединений с примесями, что способствует их удалению с поверхности металла. Поверхностно-активные вещества обладают поверхностно-активными свойствами, улучшают мокрость реагентов на поверхности и обеспечивают более равномерное распределение электрического тока.
Важно подобрать оптимальный химический состав реакционной среды, учитывая тип металла, его поверхностные свойства и требуемый результат. Контроль химического состава и концентрации реагентов позволяет достичь высокой эффективности процесса полирования и улучшить качество и внешний вид обрабатываемой поверхности металла.
Электролит и растворитель

Электрохимическое полирование поверхности металла – это процесс, осуществляемый в растворе, который называется электролитом. Такой раствор представляет собой ионное вещество, которое может проводить электрический ток. В качестве электролитов часто используются кислоты, щелочи или их соли.
Растворитель – это вещество, в котором растворяется электролит. Он должен обладать несколькими важными свойствами. Во-первых, он должен обеспечить равномерное распределение электролита по поверхности металла. Во-вторых, растворитель должен быть достаточно стабильным и не разрушаться в процессе полирования. Кроме того, он должен обладать определенной вязкостью, чтобы обеспечивать эффективное распределение электролита по всей поверхности металла.
В зависимости от типа металла, который подвергается электрохимическому полированию, выбираются определенный электролит и растворитель. Например, для полирования алюминиевых деталей часто используют растворы на основе сульфатов или гидроксидов щелочных металлов. Для полирования нержавеющей стали выбирают растворы на основе кислот, таких как серная или фосфорная. Таким образом, правильный подбор электролита и растворителя играет важную роль в процессе электрохимического полирования металла.
Влияние параметров на реакцию полирования
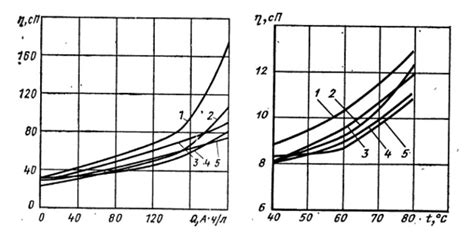
Эффективность электрохимического полирования поверхности металла зависит от ряда параметров, которые могут быть изменены для достижения желаемого результата. Одним из ключевых параметров является концентрация электролита. Чем выше концентрация раствора, тем выше скорость полирования, однако при слишком высокой концентрации может возникнуть побочная реакция, приводящая к образованию пятен или неровностей на поверхности металла.
Также важным параметром является плотность электрического тока. Оптимальная плотность тока обеспечивает равномерное полирование поверхности без образования изъянов. Если плотность тока слишком низкая, процесс полирования может быть слишком медленным, а при слишком высокой плотности тока поверхность может быть разрушена или повреждена.
Температура раствора также влияет на реакцию полирования. Повышение температуры увеличивает скорость реакции, однако при слишком высокой температуре возможно образование окислов, которые могут повредить поверхность металла или вызвать нежелательные химические реакции.
Влияние времени процесса на реакцию полирования также важно. Длительность процесса должна быть достаточной для удаления несовершенств поверхности, но при этом не должна превышать определенного значения, чтобы избежать переполнения или повреждения материала.
Таким образом, оптимальные значения параметров, таких как концентрация электролита, плотность тока, температура раствора и время процесса, позволяют достичь желаемого результата при электрохимическом полировании поверхности металла.
Вопрос-ответ

Как происходит электрохимическое полирование поверхности металла?
Электрохимическое полирование поверхности металла происходит путем погружения металлического изделия в электролит и подключения его к источнику постоянного тока. При этом на поверхности металла происходит окислительно-восстановительная реакция, в результате которой происходит удаление микронеровностей и придание поверхности более гладкого и блестящего вида.
Какова роль электролита при электрохимическом полировании поверхности металла?
Электролит играет важную роль в процессе электрохимического полирования поверхности металла. Он служит не только для проведения электрического тока, но и содержит вещества, которые участвуют в реакции окисления и восстановления металла. Электролит также может содержать добавки, которые улучшают процесс полирования и защищают поверхность от повреждений.
Какие металлы подвержены электрохимическому полированию?
Электрохимическое полирование может быть применено к большинству металлов, включая сталь, нержавеющую сталь, алюминий, медь и т.д. Однако каждый металл требует особого подхода и подбора электролита, чтобы достичь оптимального результата. Некоторые металлы могут быть более подвержены коррозии или требуют специальных условий обработки.
Какие преимущества имеет электрохимическое полирование поверхности металла по сравнению с другими методами?
Электрохимическое полирование поверхности металла имеет несколько преимуществ по сравнению с другими методами. Во-первых, оно позволяет добиться очень высокой степени гладкости поверхности, что особенно важно при производстве оптических и электронных компонентов. Во-вторых, этот метод позволяет удалять микронеровности с поверхности, что улучшает ее антикоррозийные свойства. Наконец, электрохимическое полирование более экологически чистый и эффективный процесс, чем механическое полирование, так как не требует применения абразивных материалов и снижает нагрузку на оборудование.
