Диссоциация солей - процесс, в ходе которого электролитические соединения разбиваются на ионы. Но вопрос заключается в том, какие катионы образуются в результате данного процесса. Одна из возможностей - образование катионов металла, другая - образование катионов аммония.
Катионы металла образуются при диссоциации солей, состоящих из металла и аниона. Примером может служить хлорид натрия (NaCl), который при диссоциации в водном растворе разлагается на катион натрия (Na+) и анион хлорида (Cl-). Поэтому можно сделать вывод, что при диссоциации солей образуются катионы металла.
Однако, не всегда при диссоциации солей образуются катионы металла. В некоторых случаях, соли могут содержать аммиачные группы (NH4+), которые образуют катион аммония при диссоциации. Примером такой соли может служить гидрохлорид аммония (NH4Cl), который при диссоциации разлагается на катион аммония (NH4+) и анион хлорида (Cl-).
Итак, при диссоциации солей могут образовываться как катионы металла, так и катионы аммония.
Таким образом, при диссоциации солей возможно образование как катионов металла, так и катионов аммония. Все зависит от того, из каких элементов состоит соль и какие группы присутствуют в ее составе. Этот факт имеет большое значение при изучении химии и образовании соединений, а также при проведении различных химических реакций.
Сущность диссоциации солей
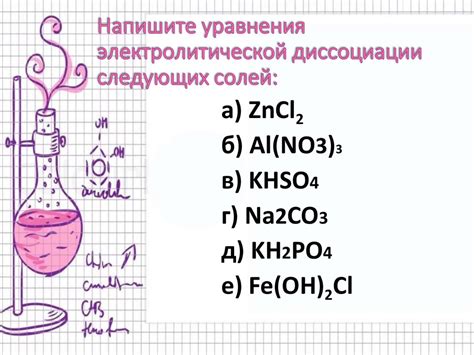
Диссоциация солей - это процесс, при котором ионная решетка соли разрушается под воздействием растворителя, и образуются отдельные ионы. В результате диссоциации соли образуются катионы и анионы, которые может быть могут образовывать новые соединения или участвовать в химических реакциях.
В процессе диссоциации солей обычно образуются катионы металла, так как металлы обладают способностью отдавать электроны. Однако, в некоторых случаях, соли могут диссоциировать, образуя катионы аммония. Катионы аммония (NH4+) формируются в результате замещения катиона металла на катион аммония.
Диссоциация солей играет важную роль в химических реакциях и процессах, так как образование ионов позволяет им участвовать во взаимодействиях с другими веществами. Катионы и анионы, образовавшиеся в результате диссоциации солей, могут осуществлять обмен ионами, образовывать новые соединения или участвовать в реакциях с веществами, содержащими соответствующие анионы или катионы.
Диссоциация солей также является фундаментальным процессом в химии растворов и химического равновесия. Понимание сущности и механизмов диссоциации солей позволяет предсказывать поведение солей в растворе и оптимизировать условия химических реакций.
Что такое диссоциация солей

Диссоциация солей – это процесс, в котором ионные соединения растворяются в воде и разделяются на ионы. Когда соль попадает в воду, межмолекулярные силы притяжения между ионами и молекулами воды превышают силы притяжения внутри молекулы соли, и происходит разрушение сети ионов.
Диссоциация солей происходит при контакте с водой, поэтому соли, такие как хлорид натрия (NaCl) или сульфат магния (MgSO4), обычно доступны в виде аморфного порошка или кристаллических гранул. В процессе диссоциации солей образуются катионы и анионы, которые находятся в растворе внутри частиц воды.
Катионы – это положительно заряженные ионы, а анионы – отрицательно заряженные ионы. Например, при диссоциации хлорида натрия образуются катион натрия (Na+) и анион хлорида (Cl-). Таким образом, при диссоциации солей образуются как катионы металла (например, натрия, калия, магния), так и катионы аммония (NH4+).
Как происходит диссоциация солей
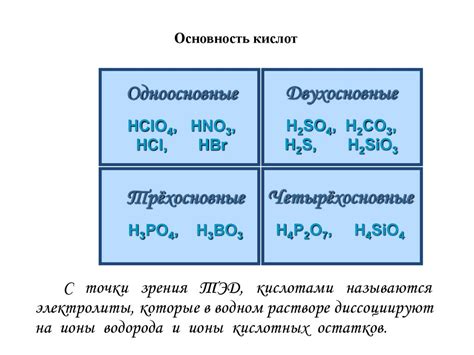
Диссоциация солей - это процесс, при котором ионная решетка соли разбивается на ионы. Обычно это происходит в растворе, когда соль погружается в воду или другую подходящую среду. Диссоциация может происходить как с катионами металла, так и с катионами аммония.
При диссоциации солей катионы металла и катионы аммония могут образовывать разные ионы. Например, при диссоциации хлорида натрия (NaCl) образуются натриевые ионы (Na+) и хлоридные ионы (Cl-). В то же время, при диссоциации хлорида аммония (NH4Cl) образуются аммониевые ионы (NH4+) и хлоридные ионы (Cl-).
Диссоциация солей происходит благодаря влиянию растворителя, который облагораживает ионы, разрывая их связи в ионной решетке соли. Вода является наиболее распространенным растворителем, так как обладает положительным и отрицательным зарядами, которые могут притягивать ионы соли и разделять их. Этот процесс происходит благодаря электростатическим взаимодействиям между ионами и водными молекулами.
Диссоциация солей может быть полной или неполной, в зависимости от концентрации соли и других факторов. При полной диссоциации все ионные связи в решетке соли разрушаются, и все ионы становятся отдельно свободными в растворе. В случае неполной диссоциации только часть ионных связей разрушается, и только некоторые ионы освобождаются.
Диссоциация солей является важным процессом не только в химии, но и в биологии и медицине. Ионы, образующиеся при диссоциации солей, участвуют в реакциях в организме, обеспечивая нормальное функционирование клеток и органов.
Катионы металла в соли

Соли являются одним из основных классов химических соединений, которые состоят из катионов и анионов. Катионы металла играют важную роль в образовании солей.
Катион металла представляет собой положительно заряженный ион, который образуется при потере одного или нескольких электронов атомом металла. Катионы металла в соли играют ключевую роль в определении физических и химических свойств соединения.
Во время диссоциации соли, молекула соли разбивается на катион металла и анион. Катионы металла различаются по своим свойствам и играют важную роль в различных химических процессах. Некоторые катионы металла имеют катализаторные свойства, что означает, что они ускоряют химические реакции, в то время как другие катионы металла могут участвовать в образовании соединений с определенными свойствами.
Примером катионов металла в соли может служить катион железа (Fe2+ или Fe3+), катион меди (Cu2+), катион кальция (Ca2+) и многие другие. Эти катионы металла имеют различные заряды и свойства, которые играют роль в определении поведения и свойств солей.
Что такое катионы металла?
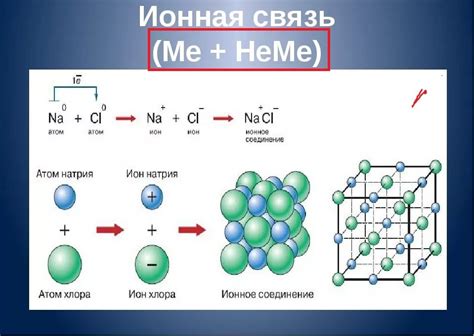
Катионы металла - это положительно заряженные ионы, состоящие из атомов металлов. Катионы металла образуются при диссоциации соответствующих солей и являются основными компонентами многих химических соединений.
Катионы металла обладают особыми свойствами, такими как высокая электропроводность и металлический блеск. Они играют важную роль в различных областях, таких как промышленность, электроника, катализ и многие другие.
Катионы металла могут иметь различные заряды, которые определяются их электронной конфигурацией и числом потерянных или приобретенных электронов. Некоторые катионы металла имеют фиксированный заряд, например, Fe3+ (железо(III)), в то время как другие катионы могут иметь переменный заряд, например, Cu+ (медь(I)) или Cu2+ (медь(II)).
Катионы металла могут образовывать различные ионы и сочетания с анионами, такими как хлориды (Cl-), сульфаты (SO42-) или карбонаты (CO32-). Эти соединения являются основой для формирования различных солей и растворов, которые широко применяются в химической промышленности и научных исследованиях.
Образование катионов металла при диссоциации солей

Диссоциация солей — это процесс, при котором ионная решетка соли разрушается под воздействием воды. При этом ионы, образующие эту решетку, становятся свободными и перемешиваются с молекулами воды.
При диссоциации солей образуются катионы и анионы. В случае с солями металлов, образуются катионы металла. Катион металла представляет собой заряженную частицу, имеющую положительный заряд. Количество ионов металла, образующихся при диссоциации соли, зависит от состава и структуры соли.
Катионы металла имеют большое значение в различных областях науки и техники. Они служат для создания различных материалов, катализаторов, электродов и других веществ, необходимых в процессе производства и эксплуатации различных устройств.
Диссоциация солей и образование катионов металла являются основой для многих реакций и процессов, происходящих в природе и в лабораторных условиях. Понимание этого процесса позволяет улучшить синтез и получение различных веществ, а также способствует развитию новых технологий и материалов.
Катионы аммония в соли

Катионы аммония (NH4+) активно участвуют в образовании солей, образуя соединения с различными анионами. Аммоний является одним из наиболее распространенных ионов в неорганической химии.
При диссоциации солей, в которых присутствует катион аммония, он разлагается на ион аммония и противоион, который может быть анионом или молекулой. В результате образуются растворимые соли аммония, которые хорошо растворяются в воде.
Катионы аммония играют важную роль в различных химических процессах. Например, аммонийные соли широко используются как удобрения в сельском хозяйстве. Они являются доступным источником азота для растений и способствуют их росту и развитию.
Также катионы аммония применяются в промышленности и экологии. Они могут быть использованы в качестве катализаторов в химических реакциях, аммонийные растворы используются для очистки воды от ионов тяжелых металлов.
В заключение, катионы аммония имеют широкий спектр применения в химии и промышленности. Они образуют соли со многими анионами, что позволяет использовать их в различных химических процессах.
Вопрос-ответ

Образуются ли катионы металла при диссоциации солей?
Да, при диссоциации солей образуются катионы металла. Диссоциация - это процесс, при котором ионы растворенной соли разделяются на положительные и отрицательные частицы. Катионы металла представляют положительные ионы, которые образуются при этом процессе.
Какие катионы образуются при диссоциации солей?
При диссоциации солей могут образовываться различные катионы, в зависимости от состава и химической формулы соли. Например, в нитрате натрия (NaNO3) образуются катионы натрия (Na+), а в сульфате меди (II) (CuSO4) образуются катионы меди (Cu2+).
Могут ли при диссоциации солей образовываться катионы аммония?
Да, при диссоциации некоторых солей могут образовываться катионы аммония (NH4+). Например, в нитрате аммония (NH4NO3) образуются катионы аммония и анионы нитрата (NO3-). Однако, не все соли образуют катионы аммония при диссоциации, так как это зависит от состава и химической формулы соли.
Какие соли образуют катионы аммония при диссоциации?
Катионы аммония (NH4+) могут образовываться при диссоциации различных солей, в которых присутствует аммоний. Некоторые примеры таких солей: хлорид аммония (NH4Cl), фосфат аммония (NH43PO4), сульфат аммония (NH4)2SO4. При диссоциации этих солей, ионы аммония отделяются от соответствующих анионов.
