Металлы 2 группы главной подгруппы являются одной из главных тем для изучения в 9 классе. В этой группе находятся элементы, которые имеют многочисленные применения и являются неотъемлемой частью нашей повседневной жизни. Эти металлы обладают особыми свойствами и широко используются в различных отраслях, от промышленности до науки и техники.
Одним из примеров металлов 2 группы главной подгруппы является медь. Этот металл обладает высокой электропроводностью и теплопроводностью, что делает его незаменимым в производстве электронных устройств и проводов. Медь также используется в строительстве, а также в производстве различных изделий, включая монеты и украшения.
Вторым примером металлов 2 группы главной подгруппы является цинк. Этот металл широко используется в промышленности благодаря своей коррозионной стойкости. Цинк покрывает стальные изделия, предотвращая их ржавение, и таким образом продлевает их срок службы. Кроме того, цинк используется в производстве пластиков и аккумуляторов, а также в качестве добавки в некоторых лекарствах и пищевых продуктах.
Изучение металлов 2 группы главной подгруппы позволяет учащимся познакомиться с интересными и практическими аспектами химии и технологии. Эти металлы являются важными материалами для различных сфер деятельности и их изучение поможет ученикам лучше понять их свойства и применение в жизни.
Основные свойства металлов 2 группы

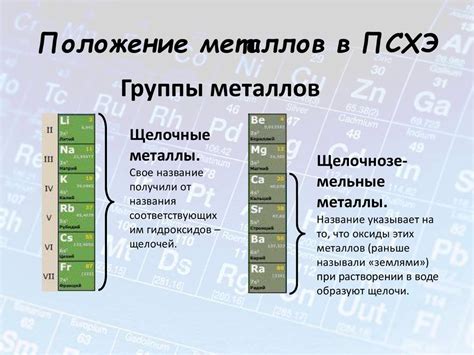
Металлы 2 группы главной подгруппы – это элементы, расположенные во второй группе таблицы химических элементов Д.И. Менделеева. Эта группа состоит из металлов щелочноземельных металлов, таких как магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Представители этой группы обладают рядом характеристических свойств. Во-первых, они являются химическими элементами с высокой электропроводностью. Таким образом, металлы 2 группы обладают способностью проводить электрический ток, что делает их важными материалами для электронных устройств и проводов.
Во-вторых, металлы 2 группы обладают высокой пластичностью и деформациией. Это означает, что они могут легко изменять свою форму без разрушения. Благодаря этому свойству особенностям, металлы 2 группы широко используются в промышленности для изготовления различных изделий и конструкций.
В-третьих, металлы 2 группы образуют стойкие оксиды. Это значит, что они обладают стойкостью к окислениям и способностью образовывать оксиды, которые защищают их поверхность от дальнейшей коррозии. Благодаря этому свойству металлы 2 группы применяются для создания материалов, устойчивых к разрушительному воздействию окружающей среды.
Таким образом, металлы 2 группы главной подгруппы обладают высокой электропроводностью, пластичностью и способностью образовывать стойкие оксиды. Эти свойства делают их ценными и полезными материалами в различных областях науки и промышленности.
Металлы 2 группы: общая характеристика
Металлы 2 группы главной подгруппы долгое время считались самыми распространенными и важными металлами. К ним относятся цинк (Zn), кадмий (Cd) и ртуть (Hg). Эти элементы обладают рядом общих характеристик.
В первую очередь, металлы 2 группы имеют блестящую поверхность и хорошую проводимость электричества и тепла. Они обладают высокой пластичностью, что позволяет легко формировать из них различные изделия и конструкции. Более того, многие из них обладают низкой плотностью, что делает их легкими и мобильными материалами.
Также металлы 2 группы достаточно реактивны. Они способны образовывать соединения с различными элементами, особенно с неметаллами. Например, цинк и кадмий образуют оксиды при взаимодействии с кислородом. Ртуть является единственным металлом, который находится в жидком состоянии при обычных условиях температуры и давления. Она обладает высокой плотностью и отличается от других металлов 2 группы.
Металлы 2 группы широко используются в различных отраслях промышленности. Например, цинк используется для производства гальванических покрытий, таких как оцинковка. Кадмий используется в батареях и аккумуляторах, а также в производстве специальных сплавов. Ртуть применяется в термометрах, барометрах, электронных приборах и в других отраслях науки и техники.
Физические свойства металлов 2 группы

Металлы из 2 группы главной подгруппы элементов - это химические элементы, которые обладают рядом характерных физических свойств. Вот некоторые из них:
Высокая тепло- и электропроводность. Металлы второй группы главной подгруппы обладают высокой способностью проводить тепло и электричество. Это связано с их специфической структурой, где электроны имеют свободу движения и могут легко передавать энергию.
Пластичность и деформируемость. Металлы этой группы являются пластичными материалами, то есть их можно легко превратить в пластичное состояние и формировать в различные изделия. Они также обладают высокой деформируемостью, то есть могут изменять свою форму без разрушения.
Металлический блеск. Металлы 2 группы главной подгруппы обладают характерным металлическим блеском, который обусловлен их способностью отражать свет. Это делает их привлекательными с точки зрения дизайна и удобными в использовании в различных отраслях промышленности.
Высокая плотность. Металлы 2 группы главной подгруппы обычно обладают высокой плотностью, что означает, что их масса на единицу объема велика. Это объясняется тем, что атомы металлов тесно упакованы в кристаллической решетке и взаимодействуют друг с другом сильными межатомными связями.
Высокая точка плавления и кипения. Металлы этой группы обладают высокой температурой плавления и кипения, что делает их полезными материалами для высокотемпературных процессов, таких как литье и пайка. Температуры плавления и кипения металлов этой группы могут достигать нескольких сотен, а иногда и тысяч градусов Цельсия.
Химические свойства металлов 2 группы

Металлы второй группы (алюминий - Al, галлий - Ga, индий - In, таллий - Tl) обладают своеобразными химическими свойствами. Они являются активными металлами и относятся к благородным металлам.
Алюминий является очень распространенным элементом в земной коре и имеет высокую химическую активность. Он реагирует со многими кислотами, образуя соли. Алюминий обладает высокой коррозионной устойчивостью и образует прочный оксидную пленку на поверхности, защищающую его от окисления. Также он может вступать в реакцию с щелочами, образуя алюминаты.
Галлий является малоактивным металлом. Он реагирует с кислородом и образует оксид Ga2O3, а также существует способность образовывать бориды, карбиды, сульфиды. Галлий растворяется в щелочах с образованием галлатов. Он обладает температурной чувствительностью, при t°C выше 29,8 °C подвергается плавкести, при t°C ниже 0 °C деперетированию.
Индий также является металлом с низкой активностью. Он не реагирует с водой и окисляется на воздухе только при нагревании. Индий также растворяется в кислотах и щелочах, образуя индийаты и индаты. Индий можно легко ковать, растягивать и прокатывать.
Таллий обладает высокой реакционной способностью. Он растворяется в концентрированных кислотах, образуя соответствующие соли. Таллий окисляется на воздухе, покрываясь оксидной пленкой. Таллиевый сплав с ртутью широко используется в термометрах и других приборах.
Применение металлов 2 группы в промышленности

Металлы 2 группы главной подгруппы – это химический элементы, которые имеют вторую электронную оболочку полностью заполненную. Эти металлы широко применяются в различных отраслях промышленности благодаря своим уникальным свойствам и высокой химической активности.
Одним из основных применений металлов 2 группы является использование их в производстве сплавов. Например, цинк (Zn), который является одним из представителей этой группы, широко используется в производстве оцинкованной стали. Этот материал обладает высокой стойкостью к коррозии и применяется в строительстве, машиностроении, автомобильной и энергетической промышленности.
Также металлы 2 группы активно применяются в производстве аккумуляторов. Например, никель (Ni) и кадмий (Cd) используются в никель-кадмиевых аккумуляторах, которые обладают высокой энергоемкостью и могут быть использованы в различных устройствах, от портативной электроники до электромобилей.
Еще одним важным применением металлов 2 группы является использование их в катализаторах. Например, медь (Cu) широко применяется в производстве катализаторов для различных химических реакций. Катализаторы на основе меди способствуют ускорению протекания химических процессов и повышению эффективности производства различных продуктов и материалов.
Вопрос-ответ

Какие металлы относятся к 2 группе главной подгруппы?
Ко второй группе главной подгруппы относятся металлы цинк (Zn), кадмий (Cd) и ртуть (Hg).
Чем отличаются металлы 2 группы главной подгруппы от других металлов?
Металлы второй группы главной подгруппы отличаются от других металлов тем, что они образуют нестойкие гидриды, т.е. соединения с водородом.
Для чего применяют металлы 2 группы главной подгруппы?
Металлы 2 группы главной подгруппы имеют различные применения. Например, цинк используется в производстве легких сплавов, кадмий применяется в изготовлении аккумуляторов, а ртуть используется в термометрах и барометрах.
Какие свойства имеют металлы 2 группы главной подгруппы?
Свойства металлов 2 группы главной подгруппы включают высокую электропроводность, хорошую термическую и электрическую проводимость, а также химическую активность и способность образовывать соединения с различными элементами.
