Кислоты – это важный класс химических соединений, обладающих разнообразными свойствами и широким спектром применения в научных и производственных целях. Изучение химических свойств кислот является одной из важных задач химии, природных наук и промышленности. В данной статье рассмотрим как практическую работу с кислотами, так и их взаимодействие с металлами.
Первое, с чего начинается изучение кислот, - это их химические свойства. Кислоты обладают способностью выделять ион водорода (H+), а также проявлять кислотность. Имея различную кислотность, кислоты обладают свойствами окрашивать индикаторы в различные цвета. Более сильные кислоты могут реагировать с металлами, образуя соли и выделяя водородный газ.
Практическая работа с кислотами включает в себя изучение их физических и химических свойств, методы получения, применение в синтезе органических соединений, лабораторные опыты и многое другое. Особое внимание уделяется безопасности работы с кислотами из-за их высокой кислотности, а также возможности их химического взаимодействия с другими веществами, включая различные металлы.
Взаимодействие кислот с металлами является практически важной частью их химических свойств. Как правило, металлы реагируют с кислотами, образуя соли и выделяя водородный газ. Реакция между кислотой и металлом происходит по следующей схеме: кислота + металл = соль + водород. Важно отметить, что силу кислотности и металлическую активность металла можно предсказать по результатам исследования их взаимодействия.
Основные химические свойства кислот

Кислоты – это класс химических соединений, которые обладают рядом особых свойств. Взаимодействуя с другими веществами, они способны проявлять кислотные реакции. Основные химические свойства кислот можно описать следующим образом:
- Кислотность: кислоты обладают кислотным вкусом и способны изменять цвет индикаторов, например, лакмуса. Вода, взаимодействуя с кислотами, может образовывать ионные растворы с положительно заряженными ионами водородного катиона H+.
- Реакция с металлами: кислоты могут реагировать с активными металлами, такими как цинк или железо, образуя соли и выделяя водородный газ. Такие реакции называются реакциями замещения. Например, при взаимодействии соляной кислоты (HCl) и цинка (Zn) образуется хлорид цинка (ZnCl2) и выделяется водородный газ (H2).
- Взаимодействие с основаниями: кислоты способны реагировать с основаниями, образуя соли и воду. При этом происходит образование ионов водорода (H+) и гидроксидных ионов (OH-). Такие реакции называются нейтрализационными.
- Окислительные свойства: некоторые кислоты обладают окислительными свойствами, то есть они способны окислять другие вещества. Например, соляная кислота (HCl) может окислять двухвалентное железо (Fe) до трехвалентного (Fe3+) посредством передачи электронов.
Изучение и понимание основных химических свойств кислот позволяет понять их роль в различных процессах, а также использовать их в практических целях, например, для производства солей, водорода или в качестве катализаторов в реакциях. Кислоты играют важную роль во многих отраслях науки и техники, а их свойства и реакции широко используются в химической промышленности и повседневной жизни.
Практическая работа с кислотами

Кислоты – важное класс химических веществ, широко используемых в различных отраслях науки и промышленности. Они имеют свойства изменять pH раствора, обладать ожогающим воздействием на кожу и вызывать коррозию металлов. Поэтому безопасная работа с кислотами требует соблюдения определенных правил и мер предосторожности.
Перед началом работы с кислотами необходимо надеть защитную экипировку, включающую в себя защитные очки, резиновые перчатки, фартук и надеть маску. Это позволит избежать попадания кислоты на кожу и снизить риск вдыхания ее паров.
Для работы с кислотами необходимо иметь специальные стеклянные или пластиковые емкости, такие как пробирки, колбы или бюксы. Не рекомендуется использовать металлическую посуду, так как она может реагировать с кислотой и вызывать нежелательные химические реакции.
При работе с кислотами следует соблюдать правила химической безопасности. Нельзя смешивать несовместимые кислоты, так как это может привести к опасным реакциям. Также необходимо быть осторожным при отливании кислоты и избегать брызг и разлива. В случае попадания кислоты на кожу или в глаза следует немедленно промыть большим количеством воды и обратиться за медицинской помощью.
Важно помнить, что кислоты необходимо хранить в специальных отдельных шкафах в закрытой таре. Это предотвратит случайные проливы и обеспечит безопасность работы с кислотами.
Взаимодействие кислот с металлами
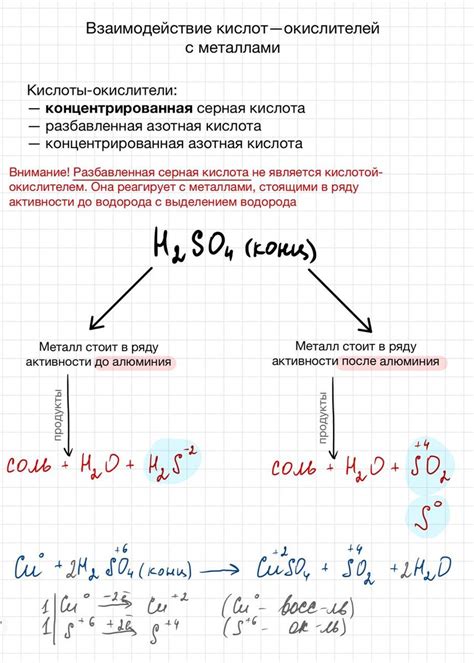
Кислоты - это вещества, обладающие кислотными свойствами и способные оттавливать водород при взаимодействии с металлами. Взаимодействие кислот с металлами является важным химическим процессом и имеет широкое применение в повседневной жизни и промышленности.
При взаимодействии кислот с металлами происходит образование солей и выделение водорода. Водород, образующийся при реакции, можно наблюдать в виде пузырьков газа, которые поднимаются вверх. Соли, образующиеся в результате реакции, имеют различные свойства и могут использоваться в разных областях.
Некоторые металлы реагируют с различными кислотами:
- Цинк, железо и алюминий реагируют с соляной кислотой, образуя соответствующие соли и выделяя водород;
- Металлы щелочных и щелочноземельных групп (например, натрий, калий, магний, кальций) реагируют с соляной кислотой, образуя хлориды и выделяя водород;
- Алюминий и железо реагируют с серной кислотой, образуя соответствующие сульфаты и выделяя водород;
- Медь и серебро реагируют с азотной кислотой, образуя соответствующие нитраты и выделяя водород.
Взаимодействие кислот с металлами широко используется в промышленности, например для получения солей различных металлов, которые являются важными сырьевыми материалами для других производственных процессов. Кроме того, это взаимодействие является основой для проведения химических анализов, так как возможность реакции между кислотой и металлом может использоваться для определения наличия определенного металла в пробе.
Таким образом, взаимодействие кислот с металлами представляет собой сложный и изучаемый процесс, имеющий практическое применение и вносящий значительный вклад в различные области науки и технологии.
Вопрос-ответ

Какие основные свойства кислот?
Основные свойства кислот включают следующие: кислоты имеют кислотный вкус, они способны взаимодействовать с основаниями, образуя соль и воду, кислоты могут реагировать с металлами, выделяя водородный газ, а также они могут реагировать с металлоксидами и металлуглекислотами, образуя соли.
Что такое кислотная реакция?
Кислотная реакция - это химическая реакция, которая происходит между кислотой и другим веществом, обычно основанием или металлом. В результате такой реакции образуется соль и вода. Кислоты и основания взаимодействуют таким образом, что их ионы сопрягаются и образуют нейтральное соединение.
Какие металлы реагируют с кислотами?
Многие металлы могут реагировать с кислотами, выделяя водородный газ и образуя соль. Некоторые примеры таких металлов включают цинк, железо, медь, свинец и алюминий. Реактивность металла с кислотой зависит от его электрохимического потенциала и свойств кислоты.
