Химия – один из основных предметов в школьной программе, который позволяет ученикам познакомиться с основными принципами и законами мироздания. Особое внимание в этом предмете уделяется изучению металлов и химических реакций, которые с ними происходят.
В рамках практической работы по химии в 9 классе ученикам предлагается провести серию экспериментов, связанных с химическими превращениями металлов. Целью данной работы является закрепление теоретических знаний о металлах и их реакциях, а также развитие практических навыков и умения их применять в реальных условиях.
Превращения металлов – это химические реакции, при которых происходит изменение состояния металлов под воздействием других химических веществ. Эти реакции могут протекать с выделением или поглощением энергии, с образованием новых веществ или изменением структуры самого металла.
В процессе практической работы ученикам предлагается провести ряд химических опытов, используя различные металлы и растворы соляной кислоты, серной кислоты, щелочи и других химических веществ. Ученики будут наблюдать за реакцией между металлом и раствором, изменением цвета, выделением газов и другими признаками химической реакции.
Химия 9 класс: цепочка химических реакций металлов

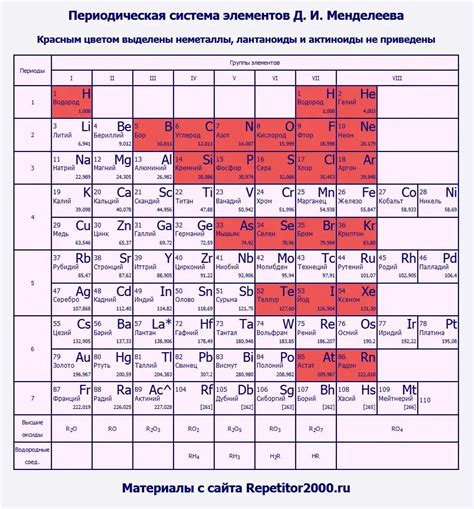
Учащиеся 9 класса изучают цепочку химических реакций металлов в предмете "Химия". Эта тема является важным звеном в обучении химии, так как позволяет ученикам понять особенности взаимодействия металлов с различными веществами и относить металлы к той или иной группе в периодической системе элементов.
Первый этап изучения цепочки химических реакций металлов начинается с рассмотрения реакций металлов с кислотами. Ученики изучают типы и свойства кислот, а также их реакцию с металлами. Здесь важно понять, что реакция металлов с кислотами протекает с образованием газа и соли, а также с выделением тепла.
На втором этапе изучаются реакции металлов с солями. В результате этих реакций происходит образование новых солей и осаждение нерастворимых соединений. Этот этап ученикам помогает разобраться в способах преобразования одной соли в другую и определить тип реакции, происходящей между металлами и солями.
Завершающий этап изучения цепочки химических реакций металлов - реакции металлов в растворах электролитов. На этом этапе учащиеся изучают качественные реакции с образованием ионообразного соединения.
Виды химических превращений металлов
Химические превращения металлов - это различные реакции и процессы, которые металлы могут претерпевать в контакте с другими веществами. В зависимости от условий и среды, в которой происходит реакция, металлы могут подвергаться разным видам химических превращений.
Окисление - один из наиболее распространенных видов химических превращений металлов. В результате окисления металл может образовывать соединение с кислородом, например, оксид, гидроксид или пероксид. Этот процесс может происходить при взаимодействии металла с водой, воздухом или другими веществами.
Реакция металла с кислотой - еще один вид химического превращения. Когда металл вступает в контакт с кислотой, образуется соединение, вода и выделяются газы. Реакция металла с кислотой часто сопровождается пузырьками, искрой или выделением тепла.
Другим видом химического превращения металлов является реакция солями. В результате этой реакции металл может вытеснить другой металл из соли или образовывать новое соединение с солью. Этот процесс называется замещением.
Кроме того, есть и другие виды химических превращений металлов, такие как реакция с аммиаком, сульфидами и другими веществами. Все эти реакции могут использоваться как в лабораторных условиях, так и в промышленности для получения различных продуктов или для анализа свойств металлов.
Значение практической работы по химии

Практическая работа по химии играет важную роль в учебном процессе в 9 классе. Она позволяет учащимся закрепить и применить полученные теоретические знания на практике.
Во время практической работы ученики активно взаимодействуют с химическими веществами, выполняют различные эксперименты и наблюдают за реакциями, что помогает им лучше понять и запомнить основные химические законы и принципы.
Практическая работа также развивает у учеников навыки наблюдения, описания и анализа результатов эксперимента. Они учатся формулировать гипотезы, планировать эксперименты, собирать и анализировать данные, делать выводы.
Практические занятия по химии также помогают развивать творческое мышление учащихся, поскольку они могут самостоятельно исследовать различные химические явления и предлагать свои собственные эксперименты и исследования.
В целом, практическая работа по химии позволяет учащимся углубить свои знания в этой области, развить творческое мышление, научиться работать с химическими веществами, а также развить умения наблюдения и анализа. Она является неотъемлемой частью учебного процесса и помогает ученикам лучше понять и применить химические знания в практической деятельности.
Опыты и эксперименты с металлами

Реакция с кислотой: Металлы активно взаимодействуют с кислотами, образуя соли и выделяя газы. Например, реакция меди с соляной кислотой приводит к образованию соли меди и обильному выделению газа хлора. Такие опыты позволяют исследовать химические свойства металлов и их реакционную способность.
Окисление металлов: Многие металлы могут окисляться при контакте с воздухом, в результате образуя оксиды. Например, железо образует ржавчину, а алюминий покрывается тонкой пленкой оксида, защищающей его от дальнейшего окисления. Опыты с окислением металлов позволяют наблюдать изменение их цвета и текстуры, а также изучать их стойкость к коррозии.
Выделение металлов: Некоторые металлы могут быть выделены из своих соединений с помощью химических реакций. Например, сплав меди с цинком может быть разложен при реакции с соляной кислотой, в результате чего медь выделяется в виде неразъемного осадка. Такие эксперименты позволяют изучать методы выделения и очистки металлов из руд и исследовать их химические свойства.
Гальванические элементы: Опыты с гальваническими элементами позволяют изучать преобразование химической энергии в электрическую. Для проведения таких экспериментов используют два различных металла, погруженных в электролит. Металлы в растворе взаимодействуют между собой, выделяя электроны и создавая разность потенциалов. Это может приводить к появлению электрического тока, который можно использовать для питания электрических устройств.
Получение сплавов: Опыты с получением сплавов металлов позволяют исследовать их физические и химические свойства. Например, сплав бронзы – меди и олова – обладает повышенной прочностью и износостойкостью, поэтому он широко используется в производстве монет, скульптур и музыкальных инструментов. Эксперименты с получением сплавов металлов позволяют изучать влияние состава и структуры на их свойства и применение в разных областях промышленности.
Вопрос-ответ

Какие металлы могут претерпевать химические превращения?
Металлы, такие как железо, медь, алюминий, свинец и цинк, могут претерпевать химические превращения.
Какие химические превращения металлов происходят?
Металлы могут окисляться (также известно как коррозия), вступать в реакцию с кислотами, осаждаться (считаться веществом) или растворяться в воде и образовывать соли при реакции с кислотами.
Какие материалы используются для проведения практической работы по химии с металлами?
Для проведения такой практической работы обычно используются предметы изделия, содержащие различные металлы, такие как гвозди, монеты и проволока, а также различные реактивы и химические растворы.
Зачем нужно изучать химические превращения металлов в практической работе?
Изучение химических превращений металлов в практической работе помогает учащимся лучше понять химические свойства и реакции металлов. Это также помогает развивать навыки наблюдения, проведения экспериментов и анализа результатов.
