Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, являются группой химических элементов, характеризующихся своими металлическими свойствами. Они обладают низкой плотностью, малой твердостью и высокой теплопроводностью, что делает их ценными материалами в различных отраслях промышленности и научных исследованиях.
Металлические свойства щелочных металлов в значительной мере определяются их электронной структурой. В атомах щелочных металлов внешний электронный слой содержит всего один электрон. Это делает эти элементы очень реактивными, так как они стремятся потерять этот электрон и образовать катионы с положительным зарядом. Благодаря этому, щелочные металлы проявляют сильную амфотерность и образуют стабильные соединения с другими элементами.
Однако, несмотря на их металлические свойства, щелочные металлы могут быть ослаблены определенными факторами. Во-первых, они могут реагировать с кислородом и образовывать оксиды, нитриды и другие соединения, которые ослабляют их металлические свойства. Во-вторых, щелочные металлы могут быть ослаблены взаимодействием с другими реактивными веществами, такими как галогены или сероводород. Эти реакции могут привести к образованию нерастворимых соединений или образованию солей, которые уже не обладают теми же металлическими свойствами, что и исходные металлы.
Понятие ослабления металлических свойств
Ослабление металлических свойств является явлением, при котором химический элемент, обладающий характеристиками металла, становится менее металлическим и приобретает некоторые свойства неметаллов.
Данный процесс часто наблюдается у щелочных металлов, таких как литий, натрий, калий и другие. Щелочные металлы обычно обладают высокой электропроводностью, воспламеняемостью, мягкостью и металлическим блеском. Ослабление их металлических свойств означает снижение электропроводности, огнестойкости, увеличение твердости и потерю блеска.
Причиной ослабления металлических свойств щелочных металлов является влияние окружающей среды, в которой они находятся. Например, щелочные металлы могут реагировать с кислородом, водой или другими химическими соединениями, что приводит к образованию оксидов, гидроксидов или солей. Эти соединения уже обладают неметаллическими свойствами и могут не проявлять металлических характеристик.
Также ослабление металлических свойств щелочных металлов связано с электронной структурой. Элементы группы щелочных металлов имеют одну внешнюю электронную оболочку, состоящую из единственного электрона. Этот электрон обладает высокой подвижностью и легко участвует в химических реакциях. При вступлении элементов группы щелочных металлов в химическую реакцию, этот электрон может переходить на другие атомы, что влияет на структуру и свойства вещества.
Раздел 1: Ослабление металлических свойств лития

Литий – первый элемент в группе щелочных металлов и обладает характерными металлическими свойствами. Однако существуют способы ослабления данных свойств, которые могут быть полезными в различных областях науки и технологий.
Первым способом ослабления металлических свойств лития является использование легирующих добавок. Добавление других элементов к литию может изменить его структуру и свойства. Например, добавление алюминия или галлия позволяет создать сплавы с улучшенной прочностью и стабильностью. Предполагается, что эти легированные сплавы будут иметь повышенную стойкость к коррозии и более широкий диапазон применения.
Вторым способом ослабления металлических свойств лития является создание композитных материалов. Путем внедрения неметаллических материалов, таких как керамика или полимеры, в структуру лития можно изменить его физические и химические свойства. Например, создание литий-керамических композитов может улучшить его механическую прочность и термическую стабильность.
Третьим способом ослабления металлических свойств лития является использование различных техник обработки. Например, литий можно подвергнуть оловянированию, что позволит уменьшить его металлическую проводимость и повысить электролитическую активность. Также можно использовать спекание или горение порошков для создания пористых структур лития, что снизит его плотность и механическую прочность.
Химические свойства лития

Литий – химический элемент из группы щелочных металлов, обладающий уникальными свойствами. Литий является самым легким металлом и обладает наименьшей плотностью среди всех элементов. Он имеет атомный номер 3 и химический символ Li.
Одним из основных свойств лития является его активность. Литий очень реактивен и быстро реагирует с водой, выделяя горючий газ. Это делает его идеальным материалом для использования в батареях и аккумуляторах, так как он может обеспечить большое количество энергии.
Еще одно важное химическое свойство лития – его способность образовывать сплавы с другими металлами. Литий является одним из ключевых компонентов в различных сплавах, которые используются в авиакосмической и автомобильной промышленности. Эти сплавы обладают высокой прочностью и легкостью, что делает литий незаменимым материалом для создания легких и прочных конструкций.
Также следует отметить, что литий обладает высокой химической стабильностью. Он не реагирует с кислородом или азотом при нормальных условиях, что делает его устойчивым к окислению и коррозии. Это позволяет литию использоваться в производстве различных химических соединений и компонентов, таких как лубриканты, катализаторы и смазки.
Механические свойства лития

Литий является самым легким металлом в таблице химических элементов. Он обладает низкой плотностью и высокой эластичностью, что делает его идеальным материалом для использования в аэронавтике и автомобильной промышленности.
В чистом виде литий очень мягкий и может быть легко срезан ножом. Он обладает низкой твердостью и прочностью, что делает его уязвимым для царапин и деформаций. Однако, литий может быть легко обрабатываться и принимать различные формы благодаря своей пластичности.
Кроме того, литий обладает высокой проводимостью электричества и тепла. Из-за этих свойств, его широко используют в производстве аккумуляторов. Литиевые ионные батареи обладают высокой энергетической плотностью и долгим сроком службы, что делает их идеальным выбором для современных электронных устройств и электромобилей.
Несмотря на свою пластичность и высокую эластичность, механические свойства лития ухудшаются при низких температурах. Он становится хрупким и может легко треснуть или сломаться. Поэтому, при использовании лития в качестве конструкционного материала, необходимо учитывать температурные условия и предусмотреть меры по защите от низких температур.
Термические свойства лития

Литий - это первый элемент в группе щелочных металлов, который обладает особыми термическими свойствами. При нагревании литий достигает высокой температуры плавления и кипения.
Температура плавления лития составляет около 180 градусов Цельсия, что делает его одним из наиболее низкотемпературных металлов. Это позволяет литию использоваться в различных технологических процессах, таких как производство аккумуляторов и легких сплавов.
Следующим важным термическим свойством лития является его высокая теплоемкость. Это означает, что литий может поглощать и отдавать большое количество тепла без существенного изменения своей температуры. Именно благодаря этому свойству литий используется в производстве теплообменных систем, в том числе в ядерных реакторах и ракетных двигателях.
Кроме того, литий обладает низким коэффициентом теплового расширения, что делает его идеальным материалом для использования в производстве прецизионных приборов и систем, где необходима стабильность размеров при разных температурах.
Раздел 2: Ослабление металлических свойств натрия

Натрий – это химический элемент, принадлежащий к группе щелочных металлов. Щелочные металлы характеризуются высокой электропроводностью, мягкостью и низкой температурой плавления. Однако существует несколько способов ослабления металлических свойств натрия.
В первую очередь, можно изменить условия окружающей среды. Натрий реагирует с влажным воздухом и водой, образуя гигроскопические соединения, такие как гидроксид натрия. Это приводит к образованию пленки оксида на поверхности металла, которая защищает его от коррозии и ослабляет его металлические свойства.
Другим способом ослабления металлических свойств натрия является сплавление с другими металлами. Например, сплав натрия с калием обладает более низкой температурой плавления и более высокой степенью мягкости, чем чистый натрий. Это позволяет использовать такой сплав в различных инженерных приложениях, например, в процессе легирования других металлов.
Также можно изменить структуру натрия с помощью механической обработки. Особенно эффективным методом является процесс холодной деформации, который значительно улучшает пластичность металла. Это делает натрий более податливым и меньше склонным к разрушению при деформации.
В результате этих манипуляций натрий может приобрести новые свойства, которые могут найти применение в различных областях науки и техники, например, в производстве батарей, стекла и сплавов.
Химические свойства натрия

Натрий является химическим элементом, относящимся к группе щелочных металлов. У него имеется один валентный электрон, что делает его очень реакционноспособным. Натрий обладает свойством легко вступать в химические реакции, особенно с водой и кислородом.
Одним из наиболее известных свойств натрия является его способность реагировать с водой. При взаимодействии натрия с водой образуется водород и гидроксид натрия. Эта реакция сопровождается выделением энергии и образованием пламени. Вода проникает в решетку металла, выбивая из нее электроны и образуя гидроксид натрия.
Натрий также способен реагировать с кислородом. При нагревании натрия на воздухе происходит окисление, при котором образуется оксид натрия. Образовавшийся оксид натрия растворяется в растворах, образуя гидроксид натрия.
Натрий обладает способностью растворяться в многих органических растворителях, таких как этиловый спирт или ацетон. При этом образуются растворы, которые могут быть использованы в различных химических процессах и реакциях.
Еще одним важным свойством натрия является его способность образовывать соединения с другими элементами. Натрий может образовывать соли с различными кислотами, такими как серная и хлорная кислоты. Эти соли имеют различные физические и химические свойства и могут использоваться в различных областях науки и промышленности.
Механические свойства натрия

Натрий - металлический элемент, относящийся к группе щелочных металлов с атомным номером 11. У натрия есть ряд важных механических свойств, которые делают его полезным в различных областях промышленности и науки.
Одним из основных механических свойств натрия является его пластичность. Натрий можно легко изменять форму под воздействием внешних сил. Это позволяет использовать его для производства различных видов изделий, таких как провода, трубы и листы. Благодаря пластичности натрия также можно получать тонкие покрытия на поверхности других материалов.
Еще одним важным механическим свойством натрия является его твердость. Натрий отличается высокой степенью твердости, что делает его устойчивым к истиранию и деформации. Это свойство делает его применимым в производстве различных видов прочных и долговечных изделий.
Также следует отметить, что натрий обладает низкой температурной пластичностью. Это означает, что при низких температурах натрий может стать хрупким и легко разрушаться под воздействием механической силы. Поэтому при работе с натрием важно учитывать его температурные свойства и предпринимать соответствующие меры для предотвращения его деформации и разрушения.
В целом, механические свойства натрия делают его важным и полезным материалом в различных отраслях промышленности, таких как металлургия, электроника и химическая промышленность. Знание и учет этих свойств позволяют эффективно использовать натрий для производства различных изделий и материалов.
Термические свойства натрия

Температура плавления: Натрий обладает низкой температурой плавления, равной 97,8 °C. Это делает его легко плавящимся металлом, который может быть переработан и использован в различных промышленных процессах.
Теплопроводность: Натрий обладает высокой теплопроводностью, со значением около 141 Вт/(м·К) при комнатной температуре. Это делает этот металл эффективным для использования в теплехладовых системах и процессах, требующих передачи тепла.
Температура кипения: Температура кипения натрия составляет около 883 °C. Это очень высокая температура, что означает, что натрий можно использовать в процессах, требующих высоких температур, таких как взрывчатые работы или термообработка стали.
Теплоемкость: Теплоемкость натрия составляет около 1,228 Дж/(г·К). Это означает, что этот металл способен поглощать и отдавать большое количество тепла, что делает его полезным для использования в качестве теплоаккумулирующего материала.
Термическое расширение: Натрий обладает высоким коэффициентом термического расширения, что означает, что он значительно расширяется при нагреве. Это является важным свойством, учитывая, что натрий используется в процессах, связанных с тепловым расширением, таких как при изготовлении стекла или керамики.
Термические свойства натрия делают его важным материалом в различных промышленных процессах и приложениях, связанных с передачей тепла, высокими температурами и тепловым расширением. Благодаря своим свойствам, натрий успешно применяется в различных отраслях, включая металлургию, энергетику и производство стекла.
Вопрос-ответ

Какой порядок ослабления металлических свойств щелочных металлов?
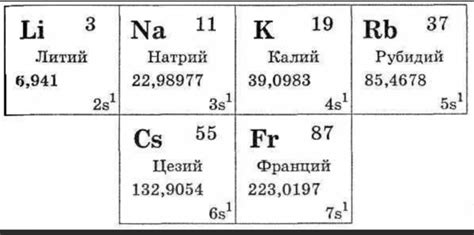
Металлические свойства щелочных металлов ослабляются в следующем порядке: литий (Li) > натрий (Na) > калий (K) > рубидий (Rb) > цезий (Cs).
Почему металлические свойства щелочных металлов ослабляются?
Металлические свойства щелочных металлов ослабляются из-за увеличения размера и сложности строения атомов при переходе к более тяжелым элементам в данной группе периодической таблицы.
Какие металлические свойства ослабляются у щелочных металлов?
У щелочных металлов ослабляются такие металлические свойства, как электропроводность, теплопроводность, металлический блеск, пластичность и образование катионов. Ослабление связи между атомами при переходе к более тяжелым элементам приводит к уменьшению этих свойств.
