Щелочные металлы - это группа элементов, включающая литий, натрий, калий, рубидий, цезий и франций. Они обладают рядом уникальных химических свойств, включая высокую реактивность и способность реагировать с водой. В этой статье мы рассмотрим процесс получения щелочных металлов с помощью воды и узнаем, почему эта реакция настолько удивительна.
Вода играет ключевую роль в процессе получения щелочных металлов. Когда щелочный металл реагирует с водой, происходит расщепление молекулы воды на водород и гидроксид иона. После этого гидроксид ион реагирует с щелочным металлом, образуя гидроксид щелочного металла и высвобождая водород.
Реакция щелочных металлов с водой является очень быстрой и энергичной. Во время реакции может наблюдаться выделение газа и образование пламени. Также следует отметить, что реакция реальностей разных металлов с водой может отличаться. Некоторые металлы могут реагировать медленно и без пламени, в то время как другие - с большой скоростью и с ярким пламенем.
Получение щелочных металлов с помощью воды имеет большое значение для промышленности. Они широко используются в различных областях, таких как производство батарей, стекла, лекарств и других химических соединений. Благодаря своим химическим свойствам, щелочные металлы стали незаменимыми материалами в нашей повседневной жизни.
Методы получения щелочных металлов
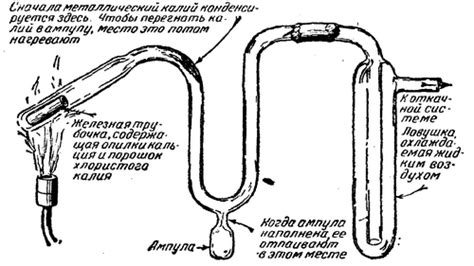
Щелочные металлы, такие как литий, натрий, калий и др., являются особыми элементами в таблице химических элементов. Они имеют малую плотность, мягкость и низкую температуру плавления. Поэтому для получения щелочных металлов используют различные методы, в основе которых лежат их физические и химические свойства.
Одним из методов получения щелочных металлов является электролиз плавящихся солей. В этом процессе используется растворение щелочной соли, например, хлорида или гидроксида, в подходящем растворителе, как правило, вода. Затем к электролиту подводят постоянный электрический ток, что приводит к разложению соли на ионы металла и ионы растворителя. Ионы металла осаждаются на отрицательно заряженном электроде, в результате чего получается металлический элемент.
Другим методом получения щелочных металлов является реакция металла с водой или паром воды. Например, натрий активно реагирует с водой, образуя гидроксид натрия и выделяя водород. Эта реакция происходит при комнатной температуре, но для ускорения процесса иногда применяют повышенную температуру и поверхность катализатора.
Еще одним методом получения щелочных металлов является пироксеновый метод, основанный на реализации химической реакции металлов с окисью углерода. В этом процессе металлы восстановлются угарным газом при высоких температурах, их оксиды превращаются в углекислые газы, а гонимая смесь проходит фазу десорбции и конверсии, которая способствует получению щелочных металлов в больших количествах.
Таким образом, получение щелочных металлов является сложным и трудоемким процессом, требующим использования специальных методов и реакций. Однако благодаря этим методам мы можем получать щелочные металлы, которые нашли широкое применение в различных отраслях промышленности и науки.
Электролиз воды
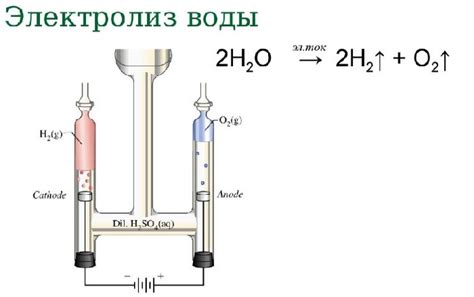
Электролиз воды – это химический процесс, при котором вода разлагается на составляющие ее элементы – водород и кислород – с помощью электрического тока. Для проведения электролиза воды необходимо использовать специальное оборудование – электролизер.
Принцип работы электролизера заключается в том, что внутри него устанавливаются специальные электроды из щелочных металлов, таких как натрий или калий. Электроды помещаются в воду, а затем через них пропускается постоянный электрический ток. Под воздействием электрического поля происходит разложение воды на ионы водорода и кислорода.
При электролизе воды на катоде (отрицательный электрод) образуются ионы водорода, которые вступают в реакцию с электроны катода, образуя молекулы водорода (H2). На аноде (положительный электрод) образуются ионы кислорода, которые соединяются с ионами водорода, образуя молекулы воды (H2O).
Электролиз воды является не только способом получения щелочных металлов, но и эффективным способом получения водорода, который широко используется в различных отраслях промышленности, включая производство химических веществ, производство энергии и даже в космической отрасли.
Химические реакции с водой

Химические реакции с водой являются одним из основных способов получения щелочных металлов. Щелочные металлы, такие как натрий (Na), калий (K) и литий (Li), имеют высокую реакционную способность с водой, что позволяет успешно провести реакцию при взаимодействии с ней.
Вода (H2O) представляет собой химическое соединение, состоящее из атомов водорода (Н) и атомов кислорода (О). При контакте с щелочными металлами происходит реакция, в результате которой образуются соответствующие гидроксиды и выделяется водородный газ (Н2).
Например, при взаимодействии натрия (Na) с водой (H2O) образуется натриевый гидроксид (NaOH) и выделяется водород (H2).
Химические реакции с водой проводятся с использованием специальных реакционных сосудов, обычно из стекла или нержавеющей стали, чтобы обеспечить безопасность процесса. Реакцию можно контролировать с помощью температуры, количества воды и объема щелочного металла.
Важно отметить, что реакция щелочных металлов с водой является сильно экзотермической, то есть сопровождается выделением большого количества тепла. Поэтому необходимо соблюдать осторожность и правила безопасности при проведении данных химических реакций.
Использование специальных растворов

Для получения щелочных металлов с помощью воды, используются специальные растворы, которые позволяют активизировать реакцию и получить желаемый результат. Эти растворы обычно содержат добавки, которые способствуют быстрому разложению воды и образованию гидроксидов щелочных металлов.
Одним из наиболее распространенных растворов, использованных в данном процессе, является раствор калия гидроксида (KOH). Этот раствор обладает высокой активностью и способностью разлагать воду, что позволяет получить калий непосредственно из гидроксида. Для активации процесса может использоваться дополнительная электролитическая ячейка.
Также для получения щелочных металлов может использоваться раствор натрия гидроксида (NaOH). Этот раствор обладает схожими свойствами с раствором калия гидроксида, поэтому его можно успешно применять в том же процессе. Однако стоит отметить, что NaOH является более доступным и дешевым вариантом.
Для ускорения процесса разложения воды и получения щелочных металлов также можно использовать растворы с добавкой органических кислот, таких как уксусная или лимонная кислота. Эти кислоты помогают активизировать реакцию и повышают эффективность получения щелочных металлов из воды. Для получения наиболее точного и стабильного результата рекомендуется проводить эксперименты и оптимизировать концентрацию и соотношение компонентов раствора.
Выделение из минералов

Выделение щелочных металлов из минералов является сложным и трудоемким процессом. Щелочные металлы, такие как натрий, калий и литий, в большинстве случаев присутствуют в минералах в составе соединений, которые не обладают щелочными свойствами. Для выделения этих металлов необходимо провести ряд химических реакций.
Одним из методов выделения щелочных металлов из минералов является их первичное обогащение, которое осуществляется путем измельчения и обогащения исходного материала. Затем происходит его обработка растворами кислот или щелочей, с целью выделения солей щелочных металлов.
Для получения натрия высушенная смесь минералов подвергается воздействию жидкой аммиачной соли. В результате происходит реакция растворения, при которой образуется аммиачная соль натрия. Такая соль затем обрабатывается раствором кислоты, после чего получают чистый натрий.
Также для выделения натрия может использоваться метод электролиза. При этом процессе раствор аммиачной соли натрия подвергается электролизу, при воздействии электрического тока происходит разложение соли на натриевые и аммиачные ионы. Натриевые ионы отрицательно заряжены и притягиваются к положительному электроду, где и выделяются в виде металлического натрия.
Выделение калия из минералов также осуществляется с помощью электролиза. Минералы, содержащие калиевые соли, подвергаются обработке серной кислотой, после чего получают раствор с солями калия. Затем этот раствор подвергается электролизу, при котором выделяется металлический калий.
Для получения лития применяют методы активного обогащения минералов, включающие измельчение и сортировку. Затем минералы обрабатывают аммиачным раствором, который приводит к растворению солей лития. Далее этот раствор подвергается процессу его охлаждения и фильтрования для отделения нерастворимых примесей. Затем полученный раствор с литием обрабатывается раствором серной кислоты, после чего происходит выделение и скопление лития.
Извлечение из пепла растений

Извлечение ключевых элементов из пепла растений является важным процессом для получения различных продуктов. Отработанный пепел, получаемый после сжигания растений, содержит множество полезных веществ, таких как калий, фосфор, натрий и магний. Путем прохождения через различные этапы переработки, эти элементы могут быть успешно извлечены.
Первоначально пепел подвергается процессу сушки, чтобы удалить излишнюю влагу. Затем следует этап гомогенизации, при котором пепел измельчается до достаточно мелкого состояния, чтобы обеспечить равномерный распределение веществ. После этого процесса, производится выщелачивание пепла с помощью воды или различных растворителей.
Выщелаченный раствор проходит через фильтры, чтобы улавливать нежелательные примеси. Затем он подвергается процессу концентрирования, в результате которого удаляется большая часть воды и получается концентрированный раствор содержащий нужные элементы. Этот раствор обычно проходит фазу обессоливания, чтобы удалить избыточные соли, что позволяет получить искомые щелочные металлы с максимальной чистотой и концентрацией.
Методы действия налегке

1. Электролиз: Один из наиболее распространенных способов получения щелочных металлов, таких как натрий и калий, - это электролиз. В этом методе вода разлагается на водород и кислород под воздействием электрического тока. В результате натрий или калий извлекаются из гидроксидов, образующихся при этом процессе.
2. Легкий металлургический способ: Другой метод получения щелочных металлов - это их извлечение из руд или минералов, содержащих их, с использованием легкометаллургического процесса. В этом случае руда сначала обрабатывается для выделения металлов, а затем их обрабатывают для получения чистой формы.
3. Гидроксидные способы: Щелочные металлы также могут быть получены путем взаимодействия гидроксидов с другими химическими веществами. Например, гидроксид натрия можно получить путем обработки поваренной соды (гидрокарбоната натрия) кальцинированием или взаимодействием с кислотой.
4. Взаимодействие с амальгамами: В качестве альтернативного способа получения щелочных металлов можно использовать их взаимодействие с амальгамами. Амальгамы - это сплавы металлов с ртутью. При взаимодействии амальгамы с натрием или калием происходит химическая реакция, в результате которой металлы извлекаются из амальгамы.
5. Фракционирование: Для получения очень чистых щелочных металлов может быть использован специальный метод - фракционирование. В этом методе применяется физическое разделение разных компонентов, принцип которого основан на разнице в физических свойствах металлов, таких как температура плавления или паровая напряженность, и используется специальная способность щелочных металлов образовывать сплавы с другими металлами.
Вопрос-ответ

Какие щелочные металлы можно получить с помощью воды?
С помощью воды можно получить такие щелочные металлы, как литий, натрий, калий, рубидий и цезий.
Почему вода может помочь в получении щелочных металлов?
Вода может помочь в получении щелочных металлов, так как они реагируют с водой и образуют щелочные растворы, которые можно использовать для получения их соединений.
Какой химической реакцией происходит в получении щелочных металлов с помощью воды?
Химическая реакция, происходящая при получении щелочных металлов с помощью воды, называется реакцией щелочной металл + вода. В результате этой реакции образуется щелочный раствор и выделяется водородный газ.
В каких условиях можно получить щелочные металлы с помощью воды?
Для получения щелочных металлов с помощью воды необходимо проводить реакцию в контролируемых условиях, например, в специальных реакторах или пробирках, чтобы избежать опасных реакций или взрывов.
