Натрий – это химический элемент с атомным номером 11 и обозначением Na в периодической системе. Он относится к активным щелочным металлам и имеет важное промышленное и химическое применение. Получение натрия может осуществляться различными методами в зависимости от его источника и условий.
Один из распространенных методов получения натрия – электролиз плавящихся солей. В данном процессе используются специальные электролизеры, в которых плавится соль, содержащая натрий. Под действием постоянного электрического тока натрийионы переносятся на отрицательный электрод (катод), где осаждается натрий в виде металла.
Еще одним методом получения натрия является реакция металла с водой. При этом реагенты взаимодействуют с образованием гидроксида натрия и выделением водорода. Уравнение реакции может быть представлено следующим образом: 2Na + 2H2O → 2NaOH + H2. Этот метод получения натрия широко используется в лабораторной практике и образовательных целях.
Также натрий может быть получен путем взаимодействия металла с галогеном (хлором) в инертной среде. На этапе реакции образуется галогенид натрия и выделяется хлор. Уравнение данной реакции можно представить следующим образом: 2Na + Cl2 → 2NaCl.
Методы получения натрия и их классификация

Натрий - щелочной металл с атомным номером 11 в периодической системе химических элементов. Он имеет множество применений, в том числе используется в производстве стекла, мыла, мышьяка и т.д. Для получения натрия применяются различные методы, которые можно разделить на несколько категорий.
Метод электролиза: при помощи этого метода натрий получают из расплава его солей. Натриевые соли, такие как хлорид натрия (NaCl), плавят и подвергают электролизу в специальных электролизерах. Под действием электрического тока происходят окисление и восстановление веществ, в результате чего на одном электроде (аноде) образуется хлор, а на другом электроде (катоде) - металлический натрий.
Метод термического восстановления: в этом методе натрий получают путем взаимодействия натриевых оксидов или нитридов с водородом. При этом происходит восстановление оксидов или нитридов, и натрий выделяется в виде металла. Этот метод является более дорогостоящим и менее распространенным, но также является эффективным способом получения натрия.
Метод обработки натриевых солей: этот метод включает в себя обработку натриевых солей различными химическими реактивами. Например, сульфид натрия (Na2S) может быть обработан оксидом кальция (CaO), при этом образуется натрий и карбонат кальция (CaCO3). Этот метод также может применяться для получения натрия.
Таким образом, методы получения натрия можно классифицировать по применяемым процессам: электролиз, термическое восстановление и обработка натриевых солей. Каждый из этих методов имеет свои преимущества и недостатки и может применяться в зависимости от конкретной ситуации и целей.
Электролиз хлорида натрия

Электролиз хлорида натрия - это процесс разложения хлорида натрия (NaCl) под воздействием электрического тока. Этот метод широко применяется для получения натрия.
Для проведения электролиза хлорида натрия необходимо иметь две электродные камеры: катодную и анодную. В катодной камере помещается раствор хлорида натрия, а в анодной - раствор воды с добавлением некоторого электролита, например, серной кислоты.
При электролизе хлорида натрия на катоде образуется металлический натрий (Na), который выделяется в виде металлического осадка. На аноде происходит окисление аниона хлорида (Cl-), при этом выделяется хлор (Cl2) в газообразной форме. Таким образом, проведение электролиза позволяет получить натрий и хлор.
Уравнения реакций, происходящих во время электролиза хлорида натрия, выглядят следующим образом:
- На катоде: 2Na+ + 2e- -> 2Na (натрий)
- На аноде: 2Cl- -> Cl2 + 2e- (хлор)
Таким образом, электролиз хлорида натрия является эффективным методом получения натрия и хлора, и широко используется в промышленности и научных исследованиях.
Термическое восстановление оксида натрия

Термическое восстановление оксида натрия — это процесс, при котором оксид натрия, также известный как пищевая или содовая сода, превращается в металлический натрий. Этот метод является одним из основных способов получения натрия и широко применяется в промышленности.
Процесс начинается с нагревания оксида натрия до высокой температуры, обычно около 900-1000 градусов Цельсия. При такой высокой температуре оксид натрия распадается на атомы натрия и кислород.
Для проведения термического восстановления оксида натрия используют специальные печи или реакторы, которые позволяют поддерживать необходимую температуру и контролировать процесс разложения оксида.
Полученный при разложении оксида натрия металлический натрий сразу реагирует с окружающим воздухом или влагой, поэтому его сразу помещают в защитную среду, например, под слой жидкости или в вакуум. Это позволяет избежать окисления натрия и его дальнейшей реакции с кислородом или водой.
Полученный металлический натрий после охлаждения можно использовать в различных промышленных процессах или для получения других химических соединений.
Метод электролиза водного раствора натрия
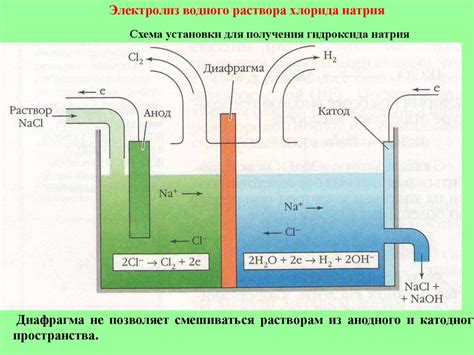
Электролиз водного раствора натрия является одним из методов получения натрия. Для проведения этой реакции необходимо наличие водного раствора натрия и проводов, через которые будет пропускаться электрический ток.
Реакция начинается с разложения воды на водород и кислород при помощи электролиза. При этом на катоде происходит процесс получения натрия, а на аноде образуется кислород.
При электролизе раствора натрия вода разлагается по следующей реакции: 2H₂O → 2H₂↑ + O₂↑. На катоде атомы водорода образуют молекулы водородного газа, а на аноде идет окисление ионов гидроксида, при котором образуется молекулярный кислород.
Кроме получения натрия, электролиз водного раствора натрия также может использоваться для получения других веществ. Например, при наличии специальных электродов, можно получить хлор. При этом на катоде образуется водород, а на аноде образуется хлор. Этот процесс называется электролизом соли.
Таким образом, метод электролиза водного раствора натрия позволяет получить натрий, а также может использоваться для получения других веществ, таких как хлор.
Уравнения реакций получения натрия
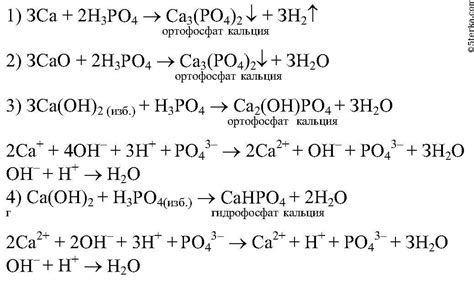
Натрий - химический элемент с атомным номером 11 и символом Na. Он является одним из основных металлов, широко используемых в промышленности и в повседневной жизни. Наиболее распространенным методом получения натрия является электролиз. Ниже приведены уравнения реакций этого процесса.
1. Электролиз хлорида натрия (NaCl). При этом реакции происходят на аноде и катоде.
- На аноде: 2Cl^- → Cl2 + 2e^-
- На катоде: 2H2O + 2e^- → H2 + 2OH^-
- Общая реакция: 2NaCl + 2H2O → Cl2 + H2 + 2NaOH
2. Электролиз расплава гидроксида натрия (NaOH).
- На аноде: 4OH^- → 2H2O + O2 + 4e^-
- На катоде: 2H2O + 2e^- → H2 + 2OH^-
- Общая реакция: 2NaOH + 2H2O → H2 + O2 + 2NaOH
3. Реакция многократного воздействия бутана на натрий (геттинговая реакция).
- 2C4H10 + 6Na → 6NaC + C8H18
Кроме этих методов, натрий также можно получить реакцией экзотермического окисления алюминия (Al) порошкообразным натрием хлорида (NaCl) при нагревании до 800°C.
Уравнение реакции электролиза хлорида натрия

Электролиз хлорида натрия — это процесс, при котором под действием постоянного электрического тока разлагается хлорид натрия на элементы — натрий и хлор. Уравнение реакции электролиза хлорида натрия позволяет описать химические изменения, происходящие при этом процессе.
Уравнение реакции электролиза хлорида натрия можно записать следующим образом:
2NaCl + 2H₂O → 2NaOH + H₂↑ + Cl₂↑
В этом уравнении хлорид натрия (NaCl) вступает в реакцию с водой (H₂O), при этом образуются гидроксид натрия (NaOH), водород (H₂) и хлор (Cl₂).
В процессе электролиза положительно заряженный ион натрия (Na+) перемещается к отрицательному электроду (катоду), где происходит его редукция с образованием натрия. Отрицательно заряженный ион хлора (Cl-) перемещается к положительному электроду (аноду) и окисляется, образуя хлор.
Электролиз хлорида натрия является важным процессом в промышленности, поскольку позволяет получать натрий и хлор — важные химические элементы, применяемые в различных отраслях промышленности.
Уравнение реакции термического восстановления оксида натрия
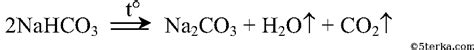
Одним из методов получения натрия является термическое восстановление оксида натрия. Эта реакция основана на использовании высокой температуры для восстановления связей между атомами натрия и кислорода.
Уравнение реакции термического восстановления оксида натрия можно записать следующим образом:
2Na2O → 4Na + O2
В результате нагревания оксида натрия (Na2O) до высокой температуры, происходит разложение на металлический натрий (Na) и кислород (O2). Полученный натрий обладает металлическим блеском и свойствами активного металла.
Уравнение такой реакции позволяет увидеть химические изменения, происходящие веществах в процессе восстановления оксида натрия. Эта реакция широко используется в промышленности для получения натрия, который затем применяется в различных отраслях, включая производство стекла, щелочи и др.
Термическое восстановление оксида натрия является эффективным методом получения натрия, так как позволяет получить высокую концентрацию этого металла при использовании относительно простого оборудования и доступных сырьевых материалов.
Уравнение реакции электролиза водного раствора натрия

Электролиз водного раствора натрия представляет собой процесс распада воды на кислород и водород под воздействием постоянного тока. Реакция электролиза происходит в специальной электролитической ячейке, в состав которой входят анод и катод из инертного материала, а также раствор натрия.
Уравнение реакции электролиза водного раствора натрия можно записать следующим образом:
На аноде происходит окисление воды и образуется кислород:
2H2O(l) → O2(g) + 4H+(aq) + 4e-
На катоде происходит восстановление водорода:
4H2O(l) + 4e- → 2H2(g) + 4OH-(aq)
Общее уравнение реакции электролиза водного раствора натрия выглядит следующим образом:
2H2O(l) → O2(g) + 2H2(g)
Таким образом, при электролизе водного раствора натрия образуются кислород и водород, которые выделяются в виде газов на соответствующих электродах.
Вопрос-ответ

Как можно получить натрий?
Натрий можно получить различными способами. Например, одним из методов является электролиз расплавленного хлорида натрия, в результате которого получается чистый натрий. Еще одним способом является взаимодействие металла с водой или кислотами.
Как происходит реакция получения натрия с водой?
Реакция получения натрия с водой происходит очень быстро и является очень активной. При контакте с водой, натрий реагирует с ней, выделяя водород и образуя гидроксид натрия.
Какие еще существуют методы получения натрия?
Помимо электролиза и реакции с водой, натрий можно получить методом термического разложения гидроксида натрия или взаимодействия натрия с азотной или серной кислотами. Также существует способ получения натрия из его оксида путем реакции с угарным газом.
Какие реакции происходят при взаимодействии натрия с кислотами?
При взаимодействии натрия с кислотами происходит реакция образования соли и выделения водорода. Например, при взаимодействии натрия с соляной кислотой образуется хлорид натрия и выделяется водород.
Какие еще металлы можно получить при электролизе аналогичных соединений?
Путем электролиза аналогичных соединений можно получить различные металлы. Например, литий, калий, магний, кальций и др. Все эти металлы также являются активными и могут реагировать с водой или кислотами.
