Электролиз является одним из наиболее эффективных методов получения металлов. При этом процессе происходит разложение раствора соли металла под воздействием электрического тока, что позволяет выделить металл на его электроде. Один из таких методов – электролиз нитрата серебра.
Нитрат серебра представляет собой химическое соединение, которое образуется при растворении серебра в азотной кислоте. Этот раствор обладает свойством проводить электрический ток и может использоваться для проведения электролиза. Электролитическая ячейка, включающая этот раствор, позволяет выделить чистое серебро на его электроде.
Принцип действия электролиза нитрата серебра основан на использовании двух электродов: катода, на который осуществляется осаждение металла, и анода, на котором происходит окисление серебра до ионов. Под влиянием электрического тока на катоде осаждаются и собираются атомы серебра с поверхности анода. Таким образом, возможно получение чистого металла с высокой степенью очистки от примесей.
Процесс электролиза нитрата серебра
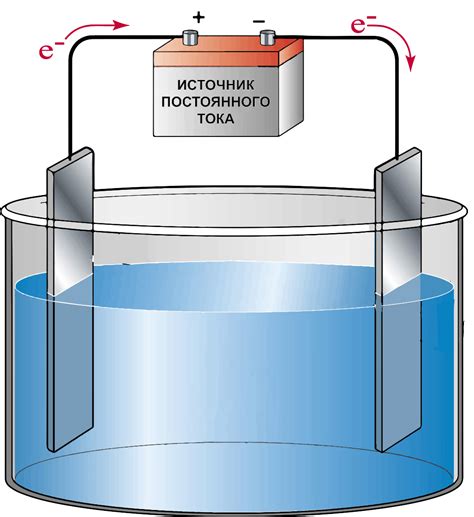
Электролиз нитрата серебра – это процесс, при котором осуществляется разложение нитрата серебра под воздействием электрического тока. Этот процесс позволяет выделить металлическое серебро из его соединения и получить чистую металлическую фольгу или другие формы серебра.
Для проведения электролиза нитрата серебра необходимы следующие компоненты: нитрат серебра в виде раствора, анод – обычно это серебряная пластина, и катод – это металлическая поверхность, на которой будет выделяться металл. Также необходим электролит и электрический источник, который будет обеспечивать поток электронов.
Во время электролиза на аноде происходит окисление металла – серебра, а на катоде – восстановление. Реакция окисления можно записать следующим образом: Ag → Ag+ + e-. Процесс восстановления будет выглядеть так: Ag+ + e- → Ag. Таким образом, ион серебра положительно заряженный и, благодаря электрическому полю, мигрирует к катоду, где и происходит его восстановление в виде металлического серебра.
В результате электролиза нитрата серебра на катоде образуется металлическое серебро, которое может быть легко отделено от раствора. Полученное серебро имеет очень высокую степень чистоты, так как электролиз позволяет избавиться от примесей и доминировать процессу выделения металла.
Механизм процесса и условия его проведения

Электролиз нитрата серебра – это процесс, в ходе которого осуществляется выделение серебра на катоде при помощи электрического тока.
Осуществление процесса электролиза нитрата серебра требует определенных условий. В первую очередь, необходимо выбрать подходящий электролит – нитрат серебра. Этот соединение хорошо проводит электрический ток и обеспечивает насыщение раствора серебром.
Далее, следует подобрать электроды, одним из которых будет катод, на котором происходит выделение серебра. Катодом может быть изготовленный из металла электрод или обычная монета из серебра. Важно, чтобы катод был непогружен в электролит полностью и находился вблизи анода.
Кроме того, важно правильно настроить параметры установки, в которой проводится электролиз. Необходимо подобрать подходящее напряжение и силу тока, чтобы обеспечить достаточную скорость выделения серебра, но не превысить предельные значения, которые могут привести к нежелательным побочным реакциям.
В процессе электролиза нитрата серебра в растворе происходит реакция окисления серебра и образования ионов Ag+. Под воздействием электрического тока ионы серебра перемещаются к катоду, где происходит их восстановление и образование металлического серебра.
Выделение металла на аноде
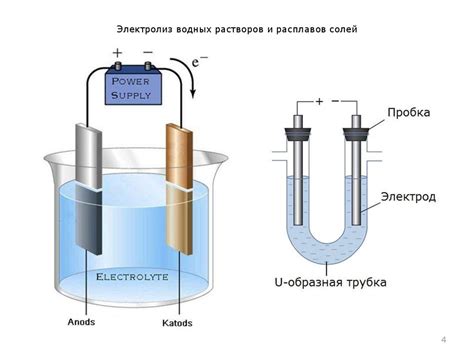
Выделение металла на аноде является одним из процессов электролиза и широко применяется в различных промышленных и лабораторных процессах. При электролизе нитрата серебра на аноде происходит окисление атомов серебра, что приводит к образованию ионов серебра Ag+.
На аноде, под воздействием положительного напряжения, ионы серебра переходят в атомарное состояние, а затем реагируют с водой, образуя ион гидроксида (OH-). Этот процесс называется окислительным процессом электролиза.
В результате окислительного процесса на аноде образуется сереброокись (Ag2O), которая может дальше реагировать с ионами серебра, образуя ионы серебра Ag+. Ионы серебра могут перемещаться в растворе и осаждаться на поверхности катода.
Выделение металла на аноде имеет большое значение для производства металлических изделий. Оно позволяет получать чистые и качественные образцы металла, обладающие необходимыми физическими и химическими свойствами.
Однако выделение металла на аноде может приводить к повышенному износу анодного материала и образованию нежелательных химических соединений. Поэтому важно контролировать процесс электролиза, поддерживая оптимальные условия для выделения металла на аноде.
Роль анода в электролизе и особенности реакции

Анод - это положительно заряженный электрод в электролитической ячейке, который играет важную роль при электролизе нитрата серебра. В данной реакции, анод является местом окисления, где происходит потеря электронов.
В процессе электролиза нитрата серебра на аноде происходит окисление и выделение анионов серебра в виде ионов Ag+. Это происходит в результате электрокатодной реакции, в которой серебро окисляется и переходит из нейтральной формы в ионную.
При неразрывной связи поступательной и крутильной подвижности ионов в растворах ser и ser + NaCl, элекциона — это раздел заряжённой смеси, где ионы диффундируют только насыщенные напряжением растворы. Но, с другой стороны, серебро – неединственный металл , который может быть активным анодом на катодном металле; как кальций или магний. Именно эта способность позволяет эффективно обратить внимание, что серебро является хорошим и катодом, и анодом.
Вопрос-ответ

Что такое электролиз нитрата серебра?
Электролиз нитрата серебра - это процесс разложения нитрата серебра на его ионы и осаждение металлического серебра на электрод. В результате электролиза, серебро достается в осажденном состоянии.
Для чего проводят электролиз нитрата серебра?
Электролиз нитрата серебра проводят для выделения металлического серебра в качестве продукта. Полученное серебро может быть использовано для производства ювелирных изделий, электроники, зеркал и других изделий.
