Металлы играют важную роль в нашей жизни и являются основой многих отраслей промышленности. Они обладают рядом уникальных свойств, которые делают их незаменимыми материалами для строительства, производства электроники, автомобилей и многих других товаров.
В периодической таблице элементов металлы занимают большую часть места и представлены различными группами и периодами. Они относятся к разным группам в зависимости от своей химической активности и способности образовывать ионы.
Важной характеристикой металлов является их электропроводность, которая объясняется наличием свободно движущихся электронов в их структуре. Большинство металлов являются отличными проводниками тепла и электричества.
Металлы также часто обладают высокой пластичностью и прочностью, что позволяет им быть использованными в качестве конструкционных материалов. Они также могут образовывать сплавы с другими металлами, что расширяет их применение и придает им дополнительные свойства.
Общие сведения о металлах в периодической таблице

Металлы представляют собой основную группу элементов периодической таблицы. Они обладают рядом уникальных свойств, которые делают их важными и необходимыми в различных сферах жизни. В периодической таблице металлы обычно располагаются слева от линии отделения, которая проходит между группами 2 и 13.
Металлы характеризуются высокой тепло- и электропроводностью, а также обладают гибкостью и пластичностью. Большинство металлов обладает блеском поверхности, который обуславливается способностью металлов отражать свет.
В периодической таблице металлы подразделяются на несколько групп и подгрупп в зависимости от химических и физических свойств. Одной из основных групп являются щелочные металлы, которые находятся в первой группе таблицы. Они характеризуются низкой плотностью и низкой температурой плавления.
Другой группой металлов являются щёлочноземельные металлы, которые располагаются во второй группе. Они обладают высокой реактивностью и встречаются в природе в виде соединений. Другие группы металлов включают переходные металлы, лантаноиды, актиноиды и др. Каждая из этих групп имеет свои особенности и применения в различных областях науки и техники.
Определение и классификация металлов
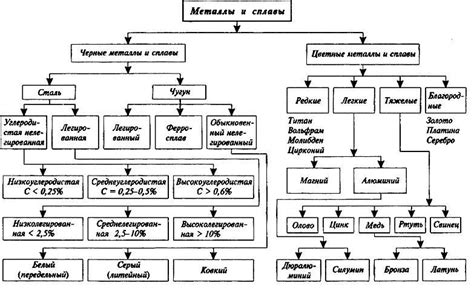
Металлы - это группа химических элементов, обладающих свойствами проводить электрический ток и тепло. В периодической таблице они располагаются слева от границы между металлами и неметаллами. Металлы обладают особым строением кристаллической решетки, характеризующейся наличием свободных электронов, что позволяет им хорошо проводить электрический ток.
Металлы можно классифицировать по различным признакам. Одним из таких признаков является металлическая проводимость. Так, выделяют две основные категории металлов: первоначальные и переходные. К первоначальным металлам относятся легкие металлы, такие как алюминий, магний и натрий. Они обладают высокой металлической проводимостью и хорошо растворимы в воде. Переходные металлы, например железо, медь и золото, обычно обладают большей плотностью, твердостью и стойкостью к окислению.
Другим важным признаком для классификации металлов является их реакционная способность. В зависимости от того, какие соединения они образуют с другими элементами, металлы могут быть активными, полимерными или инертными. Активные металлы, например натрий и калий, легко реагируют с кислородом и водой. Полимерные металлы, такие как железо и алюминий, могут образовывать различные оксиды и гидрооксиды. Инертные металлы, к которым относится золото, не реагируют с большинством веществ и обладают высокой устойчивостью к окислению и коррозии.
В заключение, металлы обладают уникальными свойствами и играют важную роль в различных сферах нашей жизни. Их классификация осуществляется на основе металлической проводимости и реакционной способности. Научиться определять и различать различные типы металлов очень полезно для понимания их влияния на окружающую среду и применения в различных технологиях.
Свойства металлов и их уникальные особенности
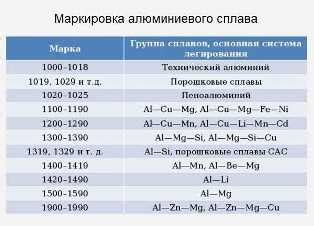
Металлы – это группа элементов, которые обладают рядом уникальных особенностей и свойств. Одним из главных свойств металлов является их способность проводить тепло и электричество. Благодаря этому свойству металлы широко используются в производстве электроники и проводов для передачи электрического тока.
Второе важное свойство металлов – их высокая пластичность и прочность. Металлы способны выдерживать большие нагрузки и деформации без разрушения. Это свойство позволяет использовать металлы в строительстве, машиностроении и других отраслях промышленности.
Еще одно характерное свойство металлов – их способность образовывать ионные связи с неметаллами. Благодаря этому свойству металлы образуют соли и минералы. Многие металлы также обладают блестящим металлическим блеском, который проявляется при наблюдении на свету.
Кроме того, металлы обладают высокой плотностью, тугоплавкостью и кондуктивностью. Эти свойства делают металлы важными компонентами в различных отраслях промышленности, включая авиацию, судостроение, а также при производстве различных металлических изделий.
В периодической таблице металлы расположены слева и по центру, при этом наиболее химически активные металлы находятся в левой части таблицы. Это связано с их способностью легко отдавать электроны и образовывать положительные ионы. Металлы также характеризуются своими химическими свойствами и возможностью образовывать разнообразные соединения с другими элементами таблицы.
Периодическая система химических элементов
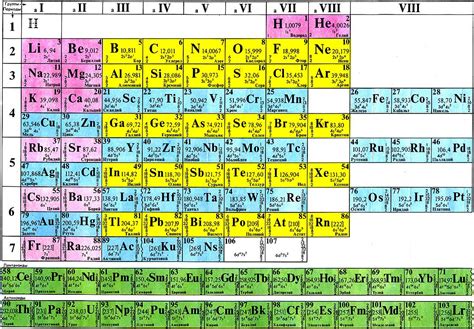
Периодическая система химических элементов – это систематизированная таблица, в которой химические элементы располагаются в порядке возрастания их атомных номеров. Созданная Дмитрием Ивановичем Менделеевым в 1869 году, она является основой для описания и классификации химических элементов.
Периодическая система состоит из нескольких основных частей. Первая часть – это периоды, представляющие собой строки, в которых элементы располагаются по возрастанию атомных номеров. Вторая часть – это группы, представляющие собой столбцы, в которых элементы имеют сходные свойства и одинаковое количество электронных оболочек.
По своим свойствам химические элементы в периодической системе классифицируются на металлы, неметаллы и полуметаллы. Металлы обладают хорошей электропроводностью, обычно твердые, блестящие и хорошо тянутся. Неметаллы, напротив, обладают плохой электропроводностью, чаще всего газообразные или хрупкие, и не обладают блеском. Полуметаллы обладают свойствами, характерными и для металлов, и для неметаллов.
Металлы занимают значительную часть периодической системы и находятся слева от ступенчатой линии, называемой "линией деления". Справа от этой линии находятся неметаллы, а по обе стороны – полуметаллы. Каждый элемент в периодической системе имеет свое уникальное положение и характеристики, которые можно узнать, изучая и анализируя эту таблицу.
Строение и принципы построения периодической таблицы
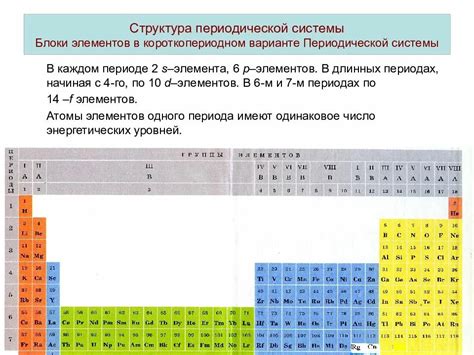
Периодическая таблица является основополагающим инструментом в химии и представляет собой упорядоченную систему элементов, в которой они разделены по столбцам и строкам. Строение периодической таблицы основано на двух принципах: атомной массе и электронной конфигурации элементов.
Периодическая таблица состоит из 7 периодов (строк) и 18 групп (столбцов). Каждая строка представляет собой новый энергетический уровень, а каждый столбец соответствует группе элементов с общими химическими свойствами. Важно отметить, что последовательность элементов в таблице основана на атомной массе, при этом все элементы размещаются в порядке возрастания атомных масс.
Каждый элемент периодической таблицы представлен своим символом, обозначенным одной или двумя буквами латинского алфавита. Также для некоторых элементов используются символы латиницы и греческого алфавита. Например, кислород обозначается символом "O", а серебро символом "Ag".
Кроме символов элементов, периодическая таблица содержит информацию о атомной массе каждого элемента. Атомная масса представляет собой среднюю массу атомов данного элемента, выраженную в атомных единицах (у). В таблице атомные массы указаны с точностью до нескольких десятых значений.
Принципы построения периодической таблицы основаны на электронной конфигурации элементов. Каждый элемент имеет свою электронную конфигурацию, которая состоит из расположения электронов в энергетических уровнях и подуровнях. Порядок заполнения электронных уровней и подуровней основан на принципе заполнения от низших энергетических уровней к высшим.
Место металлов в периодической таблице и их группировка
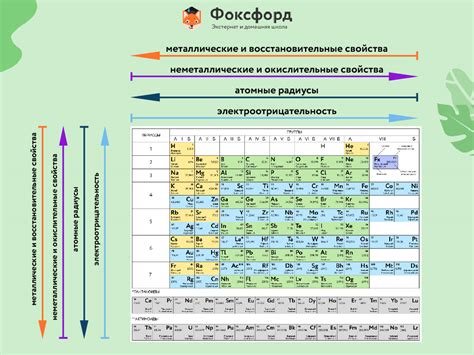
Металлы занимают большую часть периодической таблицы химических элементов. Они расположены в левой части таблицы, начиная с первого столбца. Металлы включают в себя такие элементы, как железо, медь, алюминий, свинец, никель и др. Всего металлов в таблице около 80, и они представлены в различных группах и периодах.
Металлы обладают рядом общих свойств: высокой электропроводностью, теплопроводностью и блеском. Они также обладают способностью образовывать ионы положительного заряда, поэтому обычно в веществе металлов преобладают катионы. Металлы имеют хорошую пластичность и обратимую деформацию, что позволяет им быть легко обрабатываемыми и использоваться в различных отраслях промышленности.
Металлы в периодической таблице группируются по сходству свойств и химической реактивности. Они расположены в нескольких вертикальных группах, таких как щелочные металлы (литий, натрий, калий), щелочноземельные металлы (магний, кальций, стронций), переходные металлы (железо, медь, никель) и др.
Отдельно стоит выделить благородные металлы, которые расположены в одной из вертикальных групп таблицы. Они обладают высокой устойчивостью к химическим реакциям и имеют малую активность. К этой группе относятся золото, платина, серебро и др. Благородные металлы ценятся за свои уникальные свойства и широкое применение в ювелирной промышленности, электронике и других отраслях.
Роль металлов в химических реакциях

Металлы играют важную роль в химических реакциях благодаря своим уникальным свойствам. Они обладают высокой электропроводностью, что позволяет им принимать и отдавать электроны в реакциях окисления и восстановления. Благодаря этому они становятся активными участниками многих процессов и влияют на характер и скорость этих реакций.
Металлы образуют ионы положительного заряда, которые могут образовывать комплексы с анионами и другими молекулами. Это позволяет им участвовать в реакциях образования растворов, преобразовании веществ в соли и осадки. Также металлы способны каталитически активировать молекулы реагентов, ускоряя химические реакции и снижая их активационные барьеры.
Металлы также оказывают влияние на реакции ацидо-основного характера. Они способны образовывать ионы металлов с разной степенью окисления, что позволяет им служить как кислотными, так и основными компонентами. В реакциях с кислотами они приносят электроны и окисляются, а в реакциях с основаниями они принимают электроны и восстанавливаются. Таким образом, металлы способствуют образованию новых веществ и их стабилизации в реакциях кислотно-основного взаимодействия.
- Металлы также проявляют активность в реакциях с водой. Некоторые металлы, такие как натрий и калий, реагируют с водой, выделяя водород и образуя щелочные растворы.
- Другие металлы, такие как магний и алюминий, могут реагировать с водой, но только в присутствии кислорода, образуя соответствующие оксиды или гидроксиды.
- Некоторые металлы, такие как железо и цинк, реагируют с водой только при нагревании, выделяя водород.
Металлы также активно взаимодействуют с другими веществами, такими как кислород, сера, галогены и многие другие. Их реакционная способность придаёт им специфические свойства и позволяет использовать металлы в различных отраслях промышленности, строительстве, медицине и научных исследованиях.
Вопрос-ответ

Каково значение металлов в периодической таблице?
Металлы занимают большую часть периодической таблицы и играют важную роль в химии. Они обладают хорошей проводимостью электричества и тепла, прочностью, имеют блестящую поверхность и могут образовывать ионы положительной зарядности.
Каково положение металлов в периодической таблице?
Металлы расположены слева от ступеньчатой линии в периодической таблице. Они включают в себя щелочные металлы, щелочноземельные металлы, переходные металлы, лантаниды и актиниды.
Какие свойства характерны для металлов?
Металлы имеют несколько характерных свойств: хорошую теплопроводность и электропроводность, блестящую поверхность, прочность и пластичность, низкую электроотрицательность, способность образовывать ионы положительной зарядности.
Какова роль металлов в химии?
Металлы играют важную роль в химии. Они являются основными строительными блоками для создания различных материалов и сплавов. Металлы также используются в электронике и различных технологиях. Они обладают способностью образовывать ионы, с помощью которых можно проводить реакции со многими другими веществами.
