Металлы - это один из самых распространенных типов материалов в нашей жизни. Они находят применение во многих отраслях промышленности и имеют ряд важных свойств, таких как прочность и электропроводность. Но чем обусловлены эти особенности металлов? Оказывается, причина кроется в их особой структуре.
Металлы имеют кристаллическую структуру, то есть их атомы располагаются в виде упорядоченных решеток. Основой такой решетки являются металлические связи между атомами, которые обладают специфическими свойствами. В отличие от молекулярных связей в неметаллических веществах, которые образуются благодаря обмену электронами, металлические связи формируются за счет деликвесценции электронов в проводимости и образования электронного облака.
Металлическая связь характеризуется тем, что свободные электроны перемещаются по кристаллической решетке металла в виде электронного газа. Это обеспечивает протекание электрического тока по металлу и его хорошую теплопроводность.
Кристаллическая структура металлов также обуславливает их механические свойства, такие как прочность и упругость. Атомы металла в кристалле упорядочено располагаются, формируя плотные узлы решетки, что придает металлам твердость и устойчивость к деформации. Кроме того, наличие свободных электронов в металлической структуре позволяет атомам смещаться друг относительно друга при применении механического напряжения, что обусловливает упругость металла.
Истоки кристаллической структуры металлов

Кристаллическая структура металлов имеет свои истоки в особенностях их атомной структуры. Металлы отличаются от других материалов своей способностью образовывать кристаллические решетки, где атомы металла располагаются в определенном порядке.
Атомы металлов обладают свободными электронами в валентной оболочке, которые могут свободно передвигаться по кристаллической структуре. Это позволяет металлам обладать высокой электропроводностью и теплопроводностью. Кроме того, свободные электроны ответственны за образование связей между атомами, что определяет устойчивость кристаллической структуры металла.
Атомы металлов образуют регулярную кристаллическую решетку, которая простирается на макроскопическое расстояние. Это позволяет металлам обладать такими характеристиками, как прочность, твердость и устойчивость к механическим деформациям. Кристаллическая структура металлов также определяет их способность к формированию межкристаллических дефектов, таких как вакансии, примеси и микротрещины, которые могут влиять на механические и физические свойства металла.
Разнообразие металлических элементов

Металлы - это группа химических элементов, которые имеют специфические физические и химические свойства. Они обладают высокой теплопроводностью, электропроводностью и механической прочностью, и широко применяются как конструкционные материалы.
Существует огромное разнообразие металлических элементов, которые могут образовывать кристаллические структуры. Каждый металл имеет свою уникальную кристаллическую решетку, которая определяет его характеристики и свойства.
Некоторые из наиболее распространенных металлических элементов включают железо, алюминий, медь, свинец, никель и цинк. Каждый из этих элементов имеет свои особенности, и это делает их полезными в различных отраслях, таких как строительство, автомобильная промышленность, электроника и другие.
Кристаллическая структура металла зависит не только от его состава, но и от условий, при которых происходит остывание и затвердевание. Уникальные кристаллические структуры металлов определяют их механические, электрические и термические свойства.
Разнообразие металлических элементов продолжает расширяться благодаря современным технологиям и открытиям. Ученые постоянно исследуют новые материалы с уникальными свойствами, которые могут улучшить нашу жизнь и расширить возможности промышленности.
Строение атомов и связи между ними

Атом является основным строительным блоком всех веществ во Вселенной. В металлах, атомы образуют особую структуру, называемую кристаллической. Это происходит благодаря особым свойствам и взаимодействиям атомов.
Кристаллическая структура металлов характеризуется тем, что атомы располагаются в трехмерной решетке, образующей регулярные повторяющиеся узоры. Расстояние между атомами, их порядок и ориентация определяются химическими и физическими свойствами металла.
Строение атомов в металлах обусловлено их электронной структурой. Атомы металлов имеют один или несколько свободных электронов в своей валентной оболочке, которые могут двигаться свободно по кристаллической решетке. Это делает металлы отличными проводниками электричества и тепла.
Связи между атомами в металлах называются металлическими связями. Они образуются благодаря взаимодействию свободных электронов с ядрами атомов. Эти связи характеризуются тем, что электроны делятся между атомами, образуя общую область электронной плотности, которая обеспечивает металлам их уникальные свойства, такие как пластичность и способность к проводимости.
Строение атомов и связи между ними в металлах определяют множество их физических и химических свойств. Изучение этого строения позволяет понять поведение металлов в различных условиях и использовать их во многих отраслях промышленности и науки.
Как атомы формируют кристаллические решетки
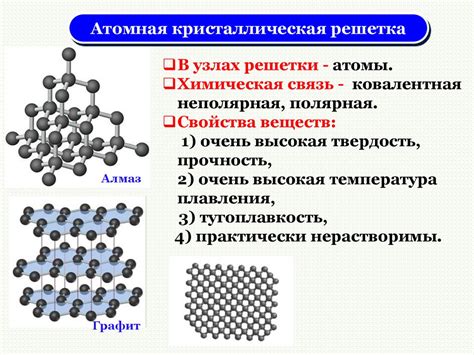
Кристаллическая структура металлов образуется благодаря особому пространственному расположению атомов в решетке. Каждый атом занимает определенное положение и связан с соседними атомами силами притяжения и отталкивания. Это позволяет атомам образовывать устойчивые кристаллические структуры, которые имеют определенную геометрическую форму и регулярность в расположении атомов.
Основной принцип формирования кристаллической структуры заключается в том, что атомы металла стремятся занять места в решетке таким образом, чтобы минимизировать свободную энергию системы. Для этого атомы образуют определенные упорядоченные группы и принимают определенную геометрическую форму.
Атомы в кристаллической структуре металлов расположены в регулярной трехмерной решетке, состоящей из повторяющихся блоков, называемых элементарными ячейками. Эти ячейки имеют определенные грани, углы и стороны, которые определяются свойствами и размерами атомов металла.
В зависимости от порядка расположения атомов, кристаллические решетки металлов могут быть различных типов, таких как кубическая гранецентрированная (ГЦК), кубическая гексагональная (ГХК), кубическая примитивная (П), тетрагональная, гексагональная и др. Каждый тип решетки имеет свои особенности и свойства, которые определяют механические и физические характеристики металла.
Таким образом, природа кристаллических решеток металлов связана с особенностями взаимодействия атомов и их стремлением к минимизации энергии. Именно благодаря этому атомы формируют устойчивые и регулярные структуры, которые дают металлам их характерные свойства.
Влияние кристаллической структуры на свойства металлов
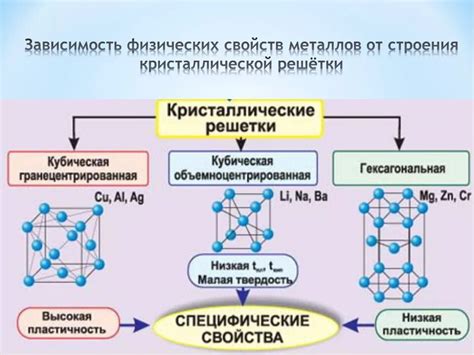
Кристаллическая структура металлов играет важную роль в их свойствах. У металлов обычно высокая плотность, и это объясняется укладкой их атомов в регулярную кристаллическую решетку. Это позволяет металлам быть прочными и устойчивыми к внешним воздействиям.
Кристаллическая структура также определяет механические свойства металлов, такие как пластичность и твердость. Например, если атомы металла укладываются в плотную кубическую решетку, то металл будет обладать высокой твердостью, а если решетка более открытая, то он будет более пластичным.
Влияние кристаллической структуры на электрические свойства металлов также очень важно. Например, в некоторых кристаллических решетках электроны могут свободно двигаться, что делает эти металлы хорошими проводниками электричества. В других решетках, где электроны имеют ограниченную свободу движения, металлы могут быть полупроводниками или даже изоляторами.
Кристаллическая структура также влияет на оптические свойства металлов. Некоторые кристаллы металлов обладают способностью отражать свет, что делает их блестящими или имеют специфический цвет. Возможность контролировать кристаллическую структуру металлов может быть использована в разных областях, например, для создания новых материалов с определенными оптическими свойствами.
Вопрос-ответ

Почему металлы образуют кристаллические структуры?
Металлы образуют кристаллические структуры из-за особенностей атомной структуры. Атомы металлов располагаются в упорядоченном трехмерном решетчатом массиве, что обеспечивает кристаллическую форму.
Какие особенности атомной структуры металлов приводят к образованию кристаллических структур?
Основные особенности атомной структуры металлов, которые приводят к образованию кристаллических структур, это наличие свободных электронов и способность атомов металлов образовывать идентичные по форме и размерам ячейки.
Какую роль играют свободные электроны в образовании кристаллических структур металлов?
Свободные электроны, которые находятся в облаке электронов внешней оболочки атомов металлов, подвижны и могут свободно перемещаться по кристаллической решетке. Их наличие обуславливает металлическую связь и способствует формированию кристаллической структуры.
Почему атомы металлов могут образовывать идентичные ячейки?
Атомы металлов имеют одинаковый размер и форму, а также простую структуру электронного облака. Из-за этих особенностей атомы металлов могут образовывать идентичные по форме и размерам кристаллические ячейки, что приводит к образованию кристаллических структур металлов.
