Электролиз - это процесс, в ходе которого металлы и другие вещества могут быть получены путем применения электрического тока. Однако, не все металлы можно получить электролизом из соответствующих растворов или расплавов. Существуют определенные причины, по которым некоторые металлы не могут быть получены этим способом.
Первая причина заключается в том, что некоторые металлы обладают высокими температурами плавления и испарения. Например, металлы, такие как вольфрам, молибден и тантал, имеют очень высокие температуры плавления и испарения. Это делает электролиз этих металлов чрезвычайно сложным, так как требует высоких температур и специальных условий.
Вторая причина связана с химической активностью металлов. Некоторые металлы, такие как золото и платина, являются химически стойкими и практически не реагируют с другими веществами при обычных условиях. Из-за своей стабильности и низкой реактивности, электролиз этих металлов оказывается очень сложным и времязатратным процессом.
Третья причина связана с наличием металлов в недоступных месторождениях. Некоторые металлы, такие как редкоземельные элементы, могут быть найдены только в небольших количествах в определенных регионах Земли. Извлечение их из этих месторождений очень сложно и дорого, что делает их получение электролизом нецелесообразным.
Итак, высокая температура плавления, низкая химическая активность и недоступность месторождений - все это причины, по которым электролиз некоторых металлов оказывается неэффективным методом получения.
Отсутствие растворимости в воде
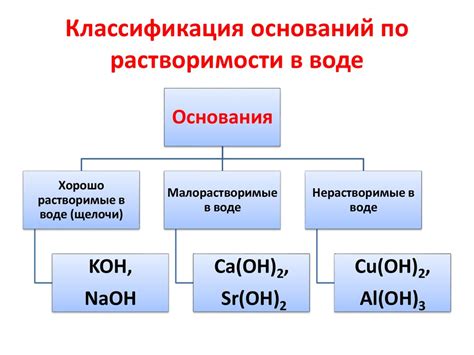
Одной из причин, по которой некоторые металлы невозможно получить электролизом, является их отсутствие растворимости в воде. В электролизе необходимо использовать раствор металлической соли, в котором растворяются металлические ионы. Однако, некоторые металлы плохо или совсем не растворяются в воде, что делает невозможным их электролиз.
Например, алюминий и магний имеют низкую растворимость в воде и образуют практически нерастворимые гидроксиды. Поэтому эти металлы нельзя получить электролизом водного раствора. Из-за низкой растворимости этих металлов для их получения чаще всего используют специальные методы, например, процессы восстановления.
Также, многие тяжелые металлы, такие как свинец, железо, медь, имеют низкую растворимость в воде. Это связано с тем, что с ростом атомного номера элемента увеличивается его плотность, что приводит к снижению растворимости металлов в воде. Поэтому для получения этих металлов чаще всего применяют другие методы, такие как пирометаллургические процессы.
Высокая энергия ионизации
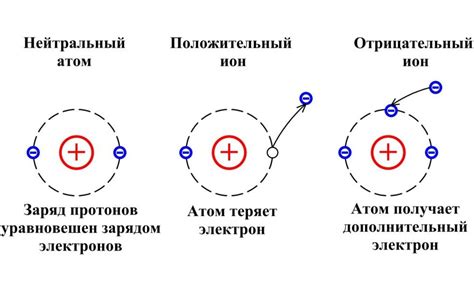
Высокая энергия ионизации является одной из причин, по которым некоторые металлы невозможно получить электролизом. Энергия ионизации - это энергия, необходимая для удаления электрона из атома. Металлы с высокой энергией ионизации обладают очень крепкими связями между атомами, что делает процесс отделения электронов сложным и требующим большого количества энергии.
При проведении электролиза, вещество разлагается на ионы, которые движутся к электродам. Однако, если металл имеет высокую энергию ионизации, то энергия, необходимая для отделения электронов, может быть слишком велика, чтобы быть достигнутой с помощью электролиза.
Примером металла с высокой энергией ионизации является алюминий. Он обладает очень высокой энергией ионизации, что делает его неподходящим для получения методом электролиза. Вместо этого, алюминий производят с помощью других методов, таких как процесс Холл-Эрра.
Также, металлы с высокой энергией ионизации могут обладать другими химическими свойствами, которые делают их неподходящими для электролиза. Например, они могут быть химически инертными или реагировать очень медленно с электролитом, что делает процесс электролиза неэффективным.
Термическая нестабильность

Одной из причин, по которым невозможно получить некоторые металлы электролизом, является их термическая нестабильность. Некоторые металлы при высокой температуре подвергаются разложению и образованию более стабильных соединений. Например, медь при нагревании сильно окисляется и образует оксид меди (CuO), которое не может быть восстановлено обратно в металлическую медь с помощью электролиза. Таким образом, электролизировать медь напрямую невозможно из-за ее термической нестабильности.
Также термическая нестабильность может проявляться и при слишком низкой температуре. Некоторые металлы при низкой температуре образуют нестабильные либо неразложимые соединения, которые не могут быть разложены восстановлением с помощью электролиза. Например, ртуть при низких температурах образует нерастворимые соединения, которые не подвергаются электролизу. Из-за этой термической нестабильности, электролизировать ртуть напрямую также невозможно.
Термическая нестабильность является важным фактором при выборе метода получения металлов. В некоторых случаях, когда металлы слишком нестабильны, другие методы, такие как химическая реакция или использование специальных реактивов, могут быть более эффективными для получения металла.
Образование прочных оксидных пленок
Один из главных факторов, по которым определенные металлы невозможно получить электролизом, заключается в образовании прочных оксидных пленок на их поверхности. Оксидные пленки образуются в результате реакции металла с кислородом из воздуха или воды и являются естественной защитой от дальнейшей коррозии и окисления.
Например, алюминий образует оксидную пленку, называемую алюминиевым оксидом (Al2O3), которая защищает его от дальнейшей окислительной реакции. Такая пленка обладает высокой прочностью и устойчивостью к разрушению, что делает трудным его электролиз с целью получения чистого металла.
Также, титан образует прочную оксидную пленку, называемую диоксидом титана (TiO2), которая обладает высокой химической стабильностью и препятствует дальнейшему процессу электролиза. Аналогично, ниобий и тантал образуют оксидные пленки на своей поверхности, которые предотвращают электролитическое разложение металла.
Образование прочных оксидных пленок на металлической поверхности является основным препятствием для проведения электролиза и осуществления процесса выделения этих металлов.
Химическая реактивность
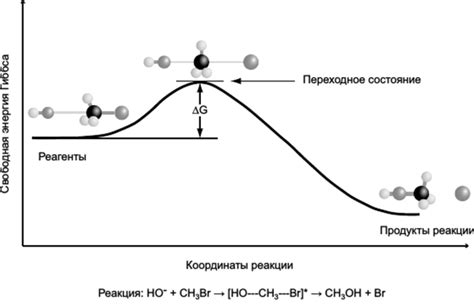
Химическая реактивность – это способность вещества вступать в химические реакции. Некоторые металлы обладают высокой химической реактивностью, что делает их неподходящими для получения электролизом.
Например, металл натрий является очень реактивным и активно реагирует с водой, выделяясь в виде водорода. Поэтому попытка получить натрий электролизом будет неэффективной.
Также, металлы, такие как калий и литий, обладают высокой химической реактивностью и сильно реагируют с веществами, присутствующими в электролите (например, с водой). Поэтому эти металлы также не могут быть получены электролизом.
Другой пример – металл алюминий, который обладает высокой химической активностью и реагирует с кислородом воздуха, образуя оксид алюминия. Поэтому сухой алюминий не может быть получен электролизом, требуется использование специальных растворов и электролитов.
Таким образом, химическая реактивность металлов является причиной, по которой эти металлы невозможно получить электролизом. Это обусловлено их способностью активно реагировать с окружающими веществами, что затрудняет или делает невозможным электролитическую реакцию.
Низкая концентрация в рудах и растворах
Одной из причин, по которым невозможно получить некоторые металлы электролизом, является их низкая концентрация в рудах и растворах. В процессе электролиза, для разделения веществ на ионы и их последующего осаждения на электроды, необходимо наличие достаточного количества металла в растворе. Однако, в случае низкой концентрации металла, процесс становится неэффективным и не может обеспечить получение требуемого количества металла.
Из-за низкой концентрации металла в рудах также затруднено его извлечение и очистка. Процесс добычи металла из руды дополнительно усложняет небольшое количество металла, что требует проведения длительных и энергоемких операций по предварительной обработке сырья и концентрированию металла.
Кроме того, низкая концентрация металла в растворах не позволяет обеспечить необходимую электропроводность, которая является неотъемлемым условием для проведения электролиза. Низкая электропроводность сильно затрудняет перемещение ионов металла к электродам, что делает процесс электролиза неэффективным и невозможным для получения металла.
Вопрос-ответ

Почему электролиз не позволяет получить некоторые металлы?
Электролиз не позволяет получить некоторые металлы из-за их высокой степени химической активности и низкой стабильности в водных растворах.
Какие причины мешают получению некоторых металлов электролизом?
Причины мешающие получению некоторых металлов электролизом могут быть разными. Некоторые металлы очень активны и уже при небольшом напряжении начинают взаимодействовать с раствором, образуя оксиды или другие соединения. Другие металлы слишком трудно восстановить и электролизом их получение будет слишком сложным и затратным.
В чем заключаются основные причины невозможности получения некоторых металлов электролизом?
Основные причины невозможности получения некоторых металлов электролизом связаны с их свойствами. Некоторые металлы очень активны и реагируют с раствором, в результате образуются оксиды или другие соединения. Другие металлы слишком трудно восстановить и требуют очень высокого напряжения, что делает электролиз их получения нерентабельным.
Можно ли получить все металлы электролизом? Какие есть препятствия?
Нет, невозможно получить все металлы электролизом. Некоторые металлы очень реактивны и образуют оксиды или другие соединения уже при небольшом напряжении. Другие металлы требуют очень высокого напряжения, что делает их получение через электролиз нерентабельным.
