Одной из характеристик металлов является их способность становиться жидкими при достижении определенной температуры. Это явление, называемое плавлением, имеет свои особенности и объясняется определенными физическими принципами.
Металлы состоят из кристаллической решетки, в которой атомы или ионы соединяются, образуя устойчивую структуру. В нормальных условиях при комнатной температуре металлическая решетка стабильна и металл находится в твердом состоянии. Однако при нагревании энергия передается атомам, что приводит к увеличению их колебаний и разрушению кристаллической структуры.
При достижении определенной температуры, называемой точкой плавления, атомы или ионы начинают двигаться достаточно активно, чтобы преодолеть силы, удерживающие их на месте. Это приводит к разрушению решетки и превращению металла в жидкость. Точка плавления зависит от химического состава металла и может быть различной для разных металлов.
Жидкость обладает особенностью принимать форму сосуда, в котором она находится, и протекать по наклонной поверхности. Кроме того, жидкость обладает значительно большей подвижностью, чем твердое вещество, что делает ее идеальным материалом для различных промышленных процессов и технологий.
Температура и положение в Менделеевской таблице

Температура является одним из важных факторов, влияющих на состояние вещества. В Менделеевской таблице химических элементов можно найти некоторые закономерности, связанные с температурными особенностями металлов.
В большинстве случаев металлы находятся в твердом состоянии при комнатной температуре. Однако, с повышением температуры они могут переходить в жидкое состояние. Такой переход связан с изменением структуры кристаллической решетки, что приводит к разрушению межатомных связей и возможности перемещения атомов и ионов вещества. Соответственно, высокая температура обеспечивает энергию, необходимую для этого перехода.
Одним из факторов, влияющих на температуру плавления металлов, является их положение в Менделеевской таблице. Например, ящерицы слева от таблицы, такие как литий и натрий, имеют низкую температуру плавления, что связано с их более слабой межатомной связью. Следующая группа металлов, группы алкалиноземельных, также имеют низкую температуру плавления.
С другой стороны, металлы справа от Менделеевской таблицы, например, платина и родий, имеют очень высокую температуру плавления, так как их межатомные связи более крепкие и требует больше энергии для разрушения решетки.
Таким образом, температура плавления металлов зависит от ряда факторов, включая структуру кристаллической решетки и межатомные связи, которые в свою очередь определяются положением металла в Менделеевской таблице.
Устройство кристаллической решетки
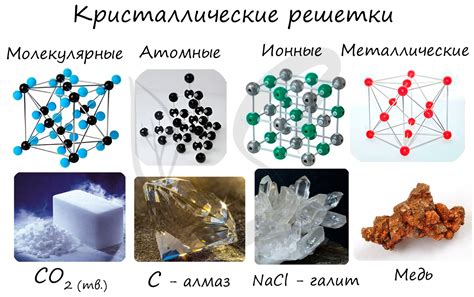
Кристаллическая решетка представляет собой систему упорядоченных атомов, расположенных в трехмерном пространстве. В каждом кристалле атомы занимают определенные позиции и соединяются друг с другом связями.
Организация атомов в кристаллической решетке определяется их взаимным расположением и типом связей, образующихся между ними. Связи между атомами обеспечивают прочность и стабильность структуры кристалла.
Кристаллическая решетка может быть описана с помощью элементарной ячейки, которая является наименьшей повторяющейся единицей решетки. Элементарная ячейка состоит из одного или нескольких атомов, которые повторяются вдоль всех направлений кристаллической решетки.
Определенные типы кристаллических решеток ведут себя особенно при повышении температуры. В некоторых металлах, например, при нагревании атомы начинают двигаться относительно своих исходных позиций в решетке, что приводит к разрушению упорядоченной структуры и образованию текучей фазы.
Термодинамические свойства металлов
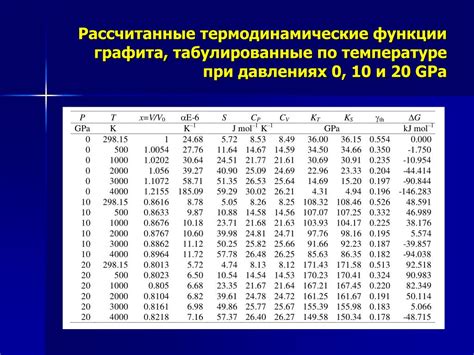
Термодинамические свойства металлов являются основными факторами, определяющими их поведение при различных температурах. Одним из наиболее важных свойств металлов является их способность переходить из твердого состояния в жидкое при достижении определенной температуры.
Один из основных факторов, влияющих на термодинамические свойства металлов, является их температура плавления. Различные металлы имеют различные значения температуры плавления: например, алюминий плавится при температуре около 660 градусов Цельсия, в то время как железо плавится при температуре около 1538 градусов Цельсия.
При достижении температуры плавления, металлы начинают претерпевать структурные изменения. В твердом состоянии атомы металла упорядочены и организованы в кристаллическую решетку. Однако при нагревании до определенной температуры эта решетка начинает разрушаться, атомы получают больше свободы движения и металл становится жидким.
Другим важным термодинамическим свойством металлов является их теплоемкость. Теплоемкость определяет количество теплоты, которое необходимо передать металлу, чтобы повысить его температуру на один градус Цельсия. Различные металлы имеют разные значения теплоемкости, что означает, что разные металлы требуют различных количеств энергии для нагрева.
Также важным фактором, влияющим на термодинамические свойства металлов, является их коэффициент теплового расширения. Коэффициент теплового расширения показывает, насколько металл расширяется при повышении температуры. Разные металлы имеют различные значения коэффициента теплового расширения, что может приводить к изменению размеров и формы металлических конструкций при нагреве.
Взаимодействие атомов и электронов
Одной из основных причин, почему металлы становятся жидкими при высокой температуре, является взаимодействие атомов и электронов. В металлах атомы расположены в кристаллической решетке, где они образуют регулярную структуру. Этот кристаллический строй обусловливает особенности свойств металлов, включая их плавление при повышении температуры.
Взаимодействие атомов в металлах происходит за счет свободных электронов, которые образуют электронное облако вокруг атомов. Эти электроны не связаны с конкретными атомами и могут свободно перемещаться по металлу. Именно благодаря этим электронам металлы обладают высокой электропроводностью и теплопроводностью.
При повышении температуры энергия атомов и электронов в металле увеличивается. Это приводит к более интенсивным движениям атомов и электронов, а также к нарушению кристаллической структуры. При определенной температуре, называемой температурой плавления, энергия становится достаточно высокой, чтобы атомы металла разрушали свои связи и освобождались от кристаллической решетки.
Таким образом, при достижении высокой температуры атомы металла получают достаточно энергии для преодоления притяжения между ними и переходят в состояние жидкости. В этом состоянии они могут свободно перемещаться друг относительно друга, что обуславливает жидкостные свойства металлов, такие как текучесть и способность принимать форму сосуда.
Примеси и легирование

Влияние примесей на свойства металлов может быть значительным. Примеси могут оказывать как положительное, так и отрицательное воздействие.
Одной из основных причин легирования металлов является улучшение их механических свойств. Добавление определенных примесей может повысить прочность, твердость и усталостную стойкость металлов. Так, например, легирование железа углеродом превращает его в сталь, которая обладает высокой прочностью и твердостью.
Помимо механических свойств, примеси также могут влиять на электрические, тепловые и магнитные свойства металлов. Например, добавление небольшого количества хрома в железо превращает его в нержавеющую сталь, которая обладает высокой коррозионной стойкостью и широко используется в производстве изделий, подверженных воздействию влаги и агрессивных сред.
Легирование может также улучшить способность металлов к формированию специфичных структур, что может быть полезно в процессе обработки и формования материала. Например, добавление алюминия в медь позволяет получить легкую и прочную сплаву, которая используется в авиационной и аэрокосмической отрасли.
Однако, неправильное или избыточное легирование также может привести к негативным последствиям. Избыток примесей может снизить механическую прочность материала, вызывать склонность к коррозии или ухудшать технологические свойства.
В целом, легирование является важной технологической процедурой, которая позволяет улучшить свойства металлов и адаптировать их для различных приложений. Внимательный выбор примесей и их концентрация могут существенно повлиять на свойства металла и определить его применение в конкретных условиях.
Вопрос-ответ

Почему металлы становятся жидкими при высокой температуре?
Металлы становятся жидкими при высокой температуре из-за изменения внутренней структуры и связей между атомами. При нагреве атомы начинают двигаться более энергично, что приводит к разрушению упорядоченной кристаллической структуры и образованию более хаотичного положения. В результате металлы переходят из твердого состояния в жидкое, где атомы свободно перемещаются, но сохраняют свои связи.
