Окисление металлов является обычным явлением в нашей повседневной жизни. Коррозия, или окисление металлов, происходит при контакте металлов с кислородом воздуха, что приводит к поверхностному разрушению и потере свойств. Но почему некоторые металлы не окисляются?
Первым фактором, который предотвращает окисление металлов, является образование защитной пленки на поверхности. Некоторые металлы, такие как алюминий, цинк или хром, обладают способностью образовывать тонкий слой оксида на своей поверхности, который защищает их от дальнейшего окисления. Эта пленка является неразрушаемой и не проницаемой для кислорода и влаги, что позволяет сохранить металл в исходном состоянии.
Вторым фактором, обеспечивающим устойчивость металлов к окислению, является их электрохимическая активность. Металлы с низкой электрохимической активностью, такие как золото, серебро или платина, обладают малой способностью к окислению, поскольку они имеют высокое значение электрохимического потенциала. Это значит, что эти металлы не будут легко отдавать электроны в окружающую среду, что и предотвращает их окисление.
Почему металл не окисляется

Окисление – процесс, при котором металлический материал взаимодействует с кислородом из воздуха, в результате чего на его поверхности образуется оксидный слой. Однако некоторые металлы не подвержены окислению, сохраняя свою металлическую структуру и свойства на протяжении длительного времени.
Главным образом, это объясняется наличием пассивности – способностью металла образовывать защитную пленку, которая предотвращает доступ кислорода и влаги к материалу. Если пассивный слой оксида нарушается, то окисление металла возобновляется.
Пассивность обусловлена различными факторами, включая:
- Содержание в сплаве специальных элементов, таких как хром или алюминий, которые образуют прочный и устойчивый оксидный слой на поверхности металла.
- Специфические условия окружающей среды, в которой находится металл. Например, медь пассивируется при высокой влажности и наличии сернистых соединений.
- Взаимодействие с другими химическими элементами, которые могут предотвратить окисление металла. Например, алюминий пассивируется благодаря образованию пленки оксида алюминия ихолида.
Пассивность некоторых металлических материалов является не только способом защиты, но и обуславливает способность этих материалов к длительному функционированию в различных условиях. Например, нержавеющая сталь обладает высокой коррозионной стойкостью благодаря образованию пассивного слоя оксида хрома.
Причины сохранения металлического блеска

Металлический блеск у металлов является результатом их особой структуры и свойственных им характеристик. Одной из причин сохранения металлического блеска является плотная упаковка металлических атомов в кристаллической решетке. Благодаря этому металлы обладают высокой плотностью и отражательной способностью, что придает им яркий блеск.
Второй важной причиной сохранения металлического блеска является природа химической связи в металлах. Металлы образуют электронный газ, состоящий из свободных электронов, которые свободно движутся между положительно заряженными ионами металла. Этот свободный электронный газ позволяет металлам хорошо отражать свет и сохранять свой блеск.
Кроме того, одной из причин сохранения металлического блеска является устойчивость к окислению. Металлы обладают высокой активностью и способностью к окислению, однако некоторые металлы образуют защитные оксидные пленки на своей поверхности, которые предотвращают дальнейшее окисление. Эти пленки являются непроницаемыми для воздуха и воды, сохраняя металлический блеск.
Таким образом, металлический блеск металлов обусловлен плотностью упаковки атомов, наличием электронного газа и способностью металлов формировать защитные оксидные пленки. Эти факторы позволяют металлам сохранять свою характеристическую внешность и металлический блеск долгое время.
Оксидационные процессы в металлах

Оксидация - это процесс химической реакции, при которой металл взаимодействует с кислородом воздуха или воды и образует оксид. Этот процесс может происходить как при комнатной температуре, так и при повышенной температуре.
Оксидация металлов осуществляется за счет электрохимических реакций, в которых происходит передача электронов между атомами металла и оксидного иона. В результате оксидации образуется слой оксидного покрытия на поверхности металла.
Оксидные покрытия играют важную роль в защите металла от дальнейшей коррозии. Они предотвращают проникновение кислорода и влаги, которые являются основными причинами окисления металлов. Кроме того, оксидные покрытия могут улучшать эстетический вид металла, делая его более долговечным и устойчивым к повреждениям.
Важно отметить, что некоторые металлы могут образовывать стабильные оксидные покрытия, такие как оксид алюминия на поверхности алюминия. Эти покрытия обладают высокой степенью стойкости к окислению и могут существовать в течение длительного времени без дополнительной защиты.
Однако, не все металлы образуют стабильные оксидные покрытия. Некоторые металлы, такие как железо, медь и цинк, склонны к быстрой окислительной реакции при взаимодействии с кислородом. В таких случаях необходимы дополнительные меры для защиты металла от окисления, такие как нанесение защитного покрытия или использование специальных антикоррозионных веществ.
Роль окислительно-восстановительных реакций

Окислительно-восстановительные реакции играют важную роль в механизмах протекания химических процессов. В частности, они влияют на окисление и восстановление металлов. Механизм таких реакций заключается в передаче электронов между различными веществами, что меняет их степень окисления.
Окисление – это процесс, при котором вещество теряет электроны, приобретая положительный заряд, в то время как восстановление – это процесс, при котором вещество получает электроны, становясь отрицательно заряженным. В случае металлов, окисление означает образование оксидов, которые являются продуктом реакции металла с кислородом из воздуха.
Многие металлы, такие как железо, алюминий и цинк, подвергаются окислению при взаимодействии с кислородом. Однако существуют металлы, которые не окисляются на воздухе, например, золото и платина. Это объясняется тем, что такие металлы обладают высокой стабильностью своего структурного состояния, что препятствует окислению.
Более того, некоторые металлы, такие как алюминий и цинк, образуют прочную оксидную пленку на своей поверхности, которая защищает их от дальнейшего окисления. Эта пленка является результатом окислительно-восстановительных реакций между металлом и кислородом из воздуха. В результате таких реакций образуется оксид металла, который затем служит защитной пленкой.
Окислительно-восстановительные реакции имеют важное значение не только в химических процессах, но и в повседневной жизни. Например, они применяются в батарейках и аккумуляторах, где металлы являются активными компонентами, участвующими в окислительно-восстановительных реакциях, которые обеспечивают получение электрической энергии. Таким образом, понимание и управление такими реакциями имеет большое практическое значение.
Электрохимический механизм предотвращения окисления
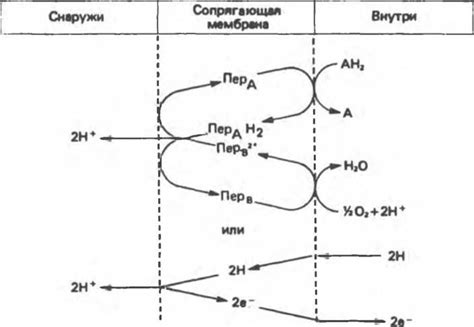
Металлы могут быть устойчивы к окислению благодаря электрохимическому механизму. Этот механизм основан на действии электронно-донорных свойств металла.
Одним из факторов, предотвращающих окисление, является наличие защитной пленки на поверхности металла. Эта пленка может быть образована путем реакции металла с окружающей средой или быть искусственно нанесенной, например, покрытием металла специальным слоем.
Защитная пленка, создаваемая электрохимическим механизмом, защищает металл от дальнейшего окисления путем формирования барьера между металлом и окружающей средой. Эта пленка может быть молекулярной или осажденной из ионов окружающей среды.
Одним из примеров электрохимического механизма предотвращения окисления является образование пленки оксида алюминия на поверхности алюминия. Пленка оксида алюминия защищает металл от контакта с воздухом и водой, предотвращая его окисление.
Таким образом, электрохимический механизм предотвращения окисления основан на создании защитной пленки на поверхности металла, которая предотвращает контакт металла с окружающей средой и защищает его от окисления.
Влияние поверхностной пленки на металл
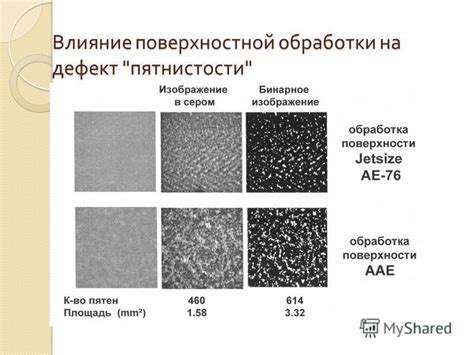
На поверхности металла образуется тонкий слой пленки, который играет важную роль в предотвращении окисления металла. Эта пленка образуется благодаря взаимодействию металла с воздушным кислородом и другими веществами.
Поверхностная пленка может быть образована как естественным образом в результате реакции металла с окружающей средой, так и с помощью специальной обработки металла. Она обладает особыми свойствами, которые способствуют защите металла от окисления и коррозии.
Во-первых, поверхностная пленка образует барьер между металлом и окружающей средой. Она предотвращает проникновение кислорода и влаги, которые являются основными причинами окисления металла. Таким образом, пленка действует как защитный слой, который предотвращает реакцию металла с окружающей средой.
Во-вторых, поверхностная пленка может иметь положительный электрический заряд, который препятствует окислительно-восстановительным процессам. Это происходит благодаря пассивированию металла, то есть уменьшению его активности в химических реакциях. Пассивирование создает условия для стабильного состояния металла и предотвращает его окисление.
Кроме того, поверхностная пленка может быть химически инертной и не реагировать с окружающей средой. Это также способствует защите металла и предотвращает его окисление. Такие инертные пленки образуются на поверхности некоторых металлов, таких как алюминий и титан, и служат долговременной защитой от окисления и коррозии.
В целом, поверхностная пленка играет важную роль в предотвращении окисления металла. Она образуется на поверхности металла и действует как барьер, препятствующий проникновению окислительных веществ и влаги. Благодаря своим особым свойствам, таким как пассивирование и инертность, пленка защищает металл и предотвращает его окисление на длительное время.
Защитные покрытия и пленки на металле

Металлы подвержены окислению, что ведет к их повреждению и коррозии. Однако существуют способы защиты металлических поверхностей от окисления.
Одним из наиболее распространенных методов является нанесение защитных покрытий. Покрытия могут быть нанесены на металл различными способами, включая покраску, гальваническое осаждение и напыление. Эти покрытия создают на поверхности металла защитную барьерную пленку, которая препятствует проникновению влаги и кислорода, тем самым предотвращая окисление металла.
Одним из примеров защитно-декоративных покрытий являются эмали. Эмали обладают не только прекрасными декоративными свойствами, но и препятствуют окислению поверхности металла.
Кроме того, использование пленок на металлических поверхностях также является эффективным способом защиты. Пленки образуются благодаря взаимодействию металла с химическими веществами, которые формируют плотную и несмываемую пленку на поверхности металла. Это предотвращает окисление и коррозию, увеличивая срок службы металлического изделия.
Примером пленок на металле являются пленки, образующиеся на поверхности алюминия и нержавеющей стали в результате их взаимодействия с атмосферным кислородом.
Таким образом, защитные покрытия и пленки являются эффективными способами защиты металла от окисления и повреждений. Они создают барьерную пленку на поверхности металла, которая препятствует проникновению окислительных сред и увеличивает срок его службы.
Вопрос-ответ

Почему металл не окисляется?
Металл не окисляется из-за своей химической структуры и свойств. Металлы обладают способностью образовывать оксидные слои, которые защищают их от окисления. Когда металл вступает в реакцию с кислородом воздуха, на его поверхности образуется слой оксида, который препятствует дальнейшему взаимодействию металла с кислородом.
Какие механизмы предотвращают окисление металла?
Окисление металла предотвращают несколько механизмов. Во-первых, металлы образуют оксидные слои на своей поверхности, которые служат своеобразной защитной пленкой. Эта пленка препятствует проникновению кислорода и воды к металлу. Во-вторых, металлы могут образовывать соединения с кислородом, которые не окисляются дальше. Например, алюминий образует оксидный слой Al2O3, который предотвращает дальнейшее окисление.
Какие металлы не окисляются?
Некоторые металлы не окисляются или окисляются очень медленно. К ним относятся металлы, образующие плотные и стабильные оксидные слои, такие как алюминий, фосфор, медь, цинк, свинец. Эти металлы защищены от окисления благодаря оксидной пленке на их поверхности.
Какие факторы могут способствовать окислению металла?
Несмотря на то что металлы имеют защитные оксидные слои, они все-таки подвержены окислению при определенных условиях. Факторы, способствующие окислению металла, включают высокую температуру, наличие агрессивных химических веществ, влажность и наличие механических повреждений на поверхности металла.
Как происходит процесс окисления металла?
Процесс окисления металла осуществляется взаимодействием металла с кислородом. Когда металл попадает в окружающую среду с кислородом, на его поверхности происходит реакция, в результате которой образуется оксид металла. Оксид образует тонкую пленку, которая предотвращает дальнейшее окисление металла. Однако, если пленка повреждается или разрушается, то металл может продолжить окисляться.
