Первое правило ряда напряжения металлов – это основной принцип, который определяет, как металлы реагируют на окружающую среду и другие вещества. Это правило является основой для понимания реакций металлов и их использования в различных отраслях промышленности.
Согласно первому правилу, каждый металл имеет свое собственное значение напряжения в ряду напряжения металлов. Это значение определяет способность металла отдавать или принимать электроны при взаимодействии с другими веществами. Металлы с более высоким значением напряжения будут отдавать электроны, а металлы с более низким значением будут принимать их.
Ключевое значение первого правила состоит в том, что оно позволяет предсказать, как два металла будут взаимодействовать друг с другом. Например, если один металл имеет более низкое значение напряжения, а другой – более высокое, то первый металл может быть склонен к окислению (при отдаче электронов), а второй металл к восстановлению (при приеме электронов).
Знание первого правила ряда напряжения металлов является важным для многих областей применения металлов, таких как электроника, химическая промышленность и экстрактивное производство. Правильное использование этого правила позволяет улучшить эффективность и долговечность различных металлических материалов и изделий.
Понятие ряда напряжения металлов

Ряд напряжения металлов – это упорядоченная таблица, в которой металлы располагаются в порядке их химической активности. Этот ряд полезен для определения того, какой металл будет окисляться, а какой будет выделяться в виде ионов при электрохимической реакции.
В ряде напряжения металлов наиболее активные металлы находятся в верхней части, а наименее активные – в нижней. Например, металлы вроде лития, калия и натрия являются очень активными, поэтому они будут выделяться в виде ионов при взаимодействии с растворами солей даже без приложения электрического тока.
Ряд напряжения металлов является важным инструментом для определения потенциальной возможности осуществления электрохимических реакций. По этому ряду можно оценить, возникнет ли электрический ток в реакции и в какую сторону он будет идти.
Важно отметить, что в ряду напряжения металлов встречается обратная зависимость между их активностью и степенью их сохранности. То есть, самые активные металлы – те, которые хорошо окисляются, в то время как наименее активные – те, которые мало подвержены окислению. Это связано с тем, что активные металлы обладают меньшей атомной удельной массой и высокими энергиями электронов на поверхности.
В заключение, ряд напряжения металлов является важным предметом изучения в химии. Он помогает понять, какие металлы могут быть использованы в электрохимических процессах, а также предсказать направление и силу тока в реакциях.
Почему важно знать первое правило ряда напряжения металлов?

Первое правило ряда напряжения металлов является основой для понимания различных процессов, связанных с электрохимией и коррозией металлов. Это правило позволяет предсказывать, какие металлы могут быть подвержены коррозии в определенных условиях и какие металлы будут действовать как аноды, а какие как катоды.
Знание первого правила ряда напряжения металлов позволяет принимать важные решения при выборе материалов для конструкций и оборудования. Если мы знаем, что металл с более высоким значением потенциала будет действовать как анод, то мы можем избегать парных сочетаний металлов, которые могут привести к коррозии. Таким образом, мы можем продлить срок службы металлических конструкций и предотвратить повреждение их поверхности.
Важно знать первое правило ряда напряжения металлов также для обеспечения безопасности в электронике. Если мы используем разные металлы в электрической цепи, их различные потенциалы могут привести к возникновению электрохимических реакций, коррозии или образованию гальванических элементов. Это может привести к нестабильности работы электронных устройств и даже к их выходу из строя. Знание первого правила ряда напряжения металлов позволяет проектировать электрические схемы с учетом этих факторов и обеспечивать надежность и долговечность устройств.
Таким образом, знание первого правила ряда напряжения металлов является необходимым для понимания и предотвращения коррозии, обеспечения безопасности и надежности в различных отраслях промышленности и науке. Это правило позволяет детально анализировать и учитывать электрохимические процессы, происходящие с металлами, и принимать информированные решения в своих проектах и исследованиях.
Что определяет первое правило ряда напряжения металлов?

Первое правило ряда напряжения металлов в химии определяет относительную способность металлов к окислительно-восстановительным реакциям. Оно устанавливает порядок, в котором различные металлы предпочитают окисляться или восстанавливаться в реакциях с растворами солей. Это правило позволяет предсказывать, какие металлы будут реагировать с растворами солей других металлов, а также определять направление и интенсивность этих реакций.
Первое правило ряда напряжения металлов основано на том, что металлы имеют различные степени удаления электрона, связанного с атомом. Чем более высокой электроотрицательностью обладает металл, тем более сильно он удерживает свои электроны и менее способен отдавать их во внешнюю среду. Следовательно, металлы с более низкими положениями в ряду напряжения имеют большую склонность к окислительным реакциям и могут восстанавливаться металлами с более высокими положениями в ряду.
Первое правило ряда напряжения металлов представляет собой упорядоченный список металлов, составленный в порядке убывания их способности к окислительно-восстановительным реакциям. Каждый металл в ряду связан с определенным потенциалом окисления, выраженным велечиной электрического потенциала. Чем ближе электрический потенциал металла к нулю, тем более вероятна его окислительная реакция. Это правило является важным инструментом для изучения химических реакций и определения стоимости и эффективности различных процессов с участием металлов.
Как использовать первое правило ряда напряжения металлов в практике?
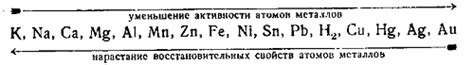
Первое правило ряда напряжения металлов – это основной принцип, который помогает определить, какой металл будет выступать в качестве анода или катода в электрохимической реакции. Для использования этого правила в практике необходимо знать значения стандартного электродного потенциала различных металлов.
Применение первого правила ряда напряжения металлов очень полезно при определении направления электрохимических процессов. Если известно значение стандартного электродного потенциала каждого металла, то можно определить, какой металл окисляется и какой восстанавливается в реакции.
Например, если имеется раствор с двумя металлами, то металл с более высоким стандартным электродным потенциалом будет выступать в качестве катода, а металл с более низким потенциалом – в качестве анода. Это позволяет предсказать направление течения электролиза и определить, какие вещества будут выделяться на электродах.
Еще одним полезным применением первого правила ряда напряжения металлов является определение возможности проведения электрохимической реакции. Если значение стандартного электродного потенциала полной реакции положительно, то процесс может протекать самопроизвольно, а если отрицательно – не может.
Какие металлы находятся в начале ряда напряжения?

Первое правило ряда напряжения металлов гласит, что металлы упорядочены в порядке возрастания их способности окисляться. То есть, в начале ряда напряжения находятся металлы, которые имеют меньшую способность к окислению, а в конце - те, которые имеют большую способность образовывать положительные ионы.
Самыми активными металлами, находящимися в конце ряда напряжения, являются щелочные металлы, такие как литий, натрий, калий и др. Они легко окисляются и образуют положительные ионы.
В начале ряда напряжения находятся металлы, которые имеют меньшую активность и возможность образовывать положительные ионы. К ним относятся, например, медь, серебро и золото. Эти металлы хорошо известны своей низкой активностью и устойчивостью к окислению.
Еще одним металлом, расположенным в начале ряда напряжения, является железо. Оно несколько активнее меди, серебра и золота, но все же имеет меньшую активность по сравнению с щелочными металлами.
В общем, металлы, которые находятся в начале ряда напряжения, обладают невысокой активностью и способностью к окислению, что делает их более устойчивыми и менее склонными к реакциям с окружающей средой.
Какие металлы находятся в конце ряда напряжения?

Ряд напряжения металлов — это упорядоченный список веществ по их реактивности в растворах. В конце этого ряда находятся металлы, проявляющие самую низкую реактивность.
Основные металлы, которые находятся в конце ряда напряжения, включают:
- Золото (Au): Золото — это блестящий желтый металл, который не коррозирует воздухом или водой. Благодаря своей стабильности, золото широко используется в ювелирном и электронном промышленности.
- Платина (Pt): Платина — это серебристо-белый блестящий металл, который обладает высокой химической инертностью. Он используется в производстве ювелирных изделий, электроники и в автомобильной промышленности.
- Ртуть (Hg): Ртуть — это единственный металл, который является жидким при комнатной температуре. Она имеет серебристо-белый цвет и используется в научных и медицинских целях.
- Серебро (Ag): Серебро — это блестящий металл, который обладает высокой электропроводностью и термической проводимостью. Серебро часто используется в ювелирном деле и в производстве различных электронных устройств.
Металлы в конце ряда напряжения обычно обладают низкой активностью и малой склонностью к окислению. Они часто используются в различных отраслях промышленности и имеют высокую ценность из-за своей устойчивости и уникальных свойств.
Примеры использования первого правила ряда напряжения металлов

Первое правило ряда напряжения металлов используется для определения возможности коррозии металлов при контакте с другими металлами или электролитами. Это правило гласит, что металл будет коррозировать металлы, которые находятся ниже него в ряду напряжения металлов. Ряд напряжения металлов составляется на основе стандартного электродного потенциала.
Один из примеров использования первого правила ряда напряжения металлов - выбор материалов для соединения в системах с различными металлами. Если два металла находятся в контакте, и один из них находится выше другого в ряду напряжения металлов, то металл, который находится ниже, будет коррозировать. Например, если алюминий и железо находятся в контакте в среде, которая содержит электролит, то алюминий, который находится выше железа в ряду напряжения металлов, будет коррозировать.
Ещё одной сферой применения первого правила ряда напряжения металлов является химическая промышленность. Зная ряд напряжения металлов, можно предсказать, какие металлы будут использоваться в электролитических процессах для осаждения или растворения металлических ионов. Например, в электролизе раствора меди можно использовать алюминий в качестве инертного электрода, так как алюминий находится выше меди в ряду напряжения металлов и не будет коррозировать.
Вопрос-ответ

Какие металлы реагируют с кислотами?
Многие металлы реагируют с кислотами и разлагают их на газы воспламенение, например, водород.
Что происходит с металлом, когда он реагирует с кислотой?
Когда металл реагирует с кислотой, происходит окислительно-восстановительная реакция, в результате которой образуется соль и выделяется водород.
