Периодическая таблица химических элементов — это удивительный инструмент, который помогает нам понять и организовать множество информации о различных химических элементах. Состоящая из строк и столбцов, она представляет собой систематическую организацию всех известных элементов и их свойств. В этой таблице каждый элемент имеет свое место и порядковый номер, а также указаны его атомная масса и химический символ.
Одной из главных особенностей периодической таблицы является ее способность предсказывать свойства и характеристики элементов. Взглянув на расположение элементов в таблице, можно определить их отношения и закономерности. Например, элементы в одной и той же вертикали, называемой группой, имеют схожие химические свойства и образуют химически сходные соединения.
Периодическая таблица содержит различные группы элементов, от щелочных металлов, таких как литий и натрий, до инертных газов, таких как гелий и неон. Каждая группа имеет свои уникальные свойства и характеристики. Некоторые элементы являются основными строительными блоками материи, так как они обладают высокой реактивностью и образуют многочисленные химические соединения. Другие элементы, такие как инертные газы, стойки и не реагируют с другими элементами, что делает их полезными в различных промышленных процессах и научных исследованиях.
Изучение периодической таблицы помогает нам лучше понять строение и свойства веществ, а также расширяет наши знания о многообразии химических элементов, которые окружают нас в повседневной жизни. В этой статье мы рассмотрим основные черты периодической таблицы и ее важность в изучении химии.
От щелочных металлов до инертных газов
Периодическая таблица химических элементов – это систематическое представление химических элементов, упорядоченных по возрастанию их атомных номеров и сгруппированных похожие свойствами. Она является важным инструментом для понимания химических свойств и взаимодействий элементов.
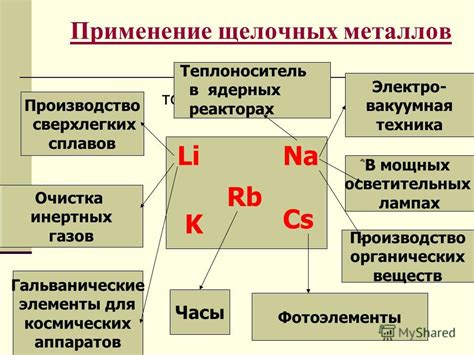
Щелочные металлы – первая группа элементов в периодической таблице. К ним относятся литий, натрий, калий, рубидий, цезий и франций. Они характеризуются низкой плотностью, высокой реакционной способностью и образованием щелочных оксидов и гидроксидов. Щелочные металлы широко используются в различных сферах, включая батарейки, стекло и промышленную химию.
После щелочных металлов следует вторая группа – щелочноземельные металлы. Они включают бериллий, магний, кальций, стронций, барий и радий. Щелочноземельные металлы обладают высокой плотностью и реакционной способностью, образуют соединения с щелочными свойствами, но не такими выраженными, как у щелочных металлов.
Инертные газы – последняя группа элементов в периодической таблице. Они включают гелий, неон, аргон, криптон, ксенон и радон. Инертные газы характеризуются низкой реакционной способностью и прекрасно подходят для использования как заполнители в лампах, для защиты от окисления и увеличения срока службы различных материалов.
Первая группа: щелочные металлы
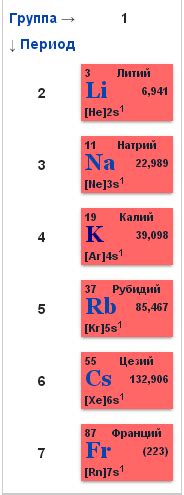
Первая группа периодической таблицы элементов включает в себя щелочные металлы. Щелочные металлы - это металлы, которые легко окисляются и создают щелочные растворы, когда взаимодействуют с водой. В эту группу входят литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Щелочные металлы обладают низкой плотностью, низкой температурой плавления и кипения, а также мягкой консистенцией. Они хорошо проводят электричество и тепло, и часто используются в различных электронных устройствах.
Эти металлы имеют одну внешнюю электронную оболочку, что делает их очень реактивными и склонными к образованию ионов, в результате чего они образуют положительно заряженные ионы, известные как катионы. Катионы щелочных металлов играют важную роль в многих биологических процессах и имеют широкое применение в промышленности, например, для производства мыла и стекла.
Стоит отметить, что вода является токсичной для чистых щелочных металлов, поэтому они хранятся под слоем минерального масла или в инертной среде. Некоторые щелочные металлы, такие как литий и калий, имеют также медицинское применение, например, в лечении болезней нервной системы и высокого кровяного давления.
Вторая группа: щелочноземельные металлы

Вторая группа периодической таблицы включает щелочноземельные металлы — редкие и ценные элементы, отличающиеся своими химическими свойствами. К этой группе относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Щелочноземельные металлы обладают характеристиками, промежуточными между щелочными металлами и переходными металлами. Они имеют два валентных электрона во внешней оболочке и легко образуют ионные соединения. Бериллий является химически активным и токсичным элементом, используется в производстве сплавов и керамики. Магний и его соединения широко применяются в промышленности, включая производство легких сплавов и фармацевтических препаратов.
Кальций является необходимым элементом для здоровья человека и животных, участвует во многих биологических процессах и строительстве костей. Стронций применяется в ядерной энергетике и в производстве огнетушителей. Барий используется для получения осадков и красителей, а также в медицине для рентгенологических исследований. Радий является радиоактивным элементом и имеет очень ограниченные применения из-за его высокой токсичности и излучений.
Последний столбец: инертные газы

Последний столбец периодической таблицы элементов - это столбец инертных газов. Инертные газы известны своей низкой реактивностью и малой склонностью к образованию химических соединений. В этом столбце находятся следующие элементы: гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радон (Rn).
Инертные газы получили свое название потому, что они обладают стабильными электронными конфигурациями и заполненными электронными оболочками, что делает их малоактивными в химических реакциях. Все инертные газы являются мономатомными, то есть состоят из одиночных атомов.
Инертные газы обладают рядом уникальных свойств, которые делают их важными для различных применений. Например, гелий используется в заполнении воздушных шаров и в аэростатике, потому что он легче воздуха и обладает низкой плотностью. Неон широко используется в рекламной и осветительной промышленности, благодаря своему яркому красному свету. Аргон используется в сварке и в процессах с повышенным тепловыделением, так как он незаметен для многих химических реакций.
Кроме того, инертные газы играют важную роль в нашей окружающей среде. Они входят в состав атмосферы и предоставляют защиту от вредных воздействий. Например, аргон оказывает защитное действие на Землю, поглощая солнечное излучение и предотвращая его попадание на поверхность планеты во время дневного света. Таким образом, инертные газы играют важную роль в различных сферах нашей жизни и имеют большое значение для научных и промышленных исследований.
Организация таблицы
Периодическая таблица химических элементов - это удобное средство для организации информации об элементах, их свойствах и взаимодействиях. Эта таблица состоит из строк, называемых периодами, и столбцов, называемых группами. Каждый элемент в таблице представлен своим символом и атомным номером.
Периоды в таблице обозначают энергетические уровни, на которых располагаются электроны в атомах элементов. Группы представляют собой вертикальные столбцы элементов с похожими химическими свойствами.
Внутри каждой ячейки периодической таблицы содержится информация о соответствующем элементе: его название, атомная масса и показатель электроотрицательности. Кроме того, в таблице можно найти дополнительные сведения о симболе элемента и его блоке в таблице.
Периодическая таблица также может быть организована по блокам элементов, включая s-, p-, d- и f-блоки. Блоки отображают электронную конфигурацию элементов и их связь с различными химическими свойствами.
Использование периодической таблицы позволяет химикам и другим ученым быстро находить необходимую информацию о химических элементах и строить связи между ними, что существенно упрощает изучение и понимание химической науки.
Вопрос-ответ

Что такое периодическая таблица?
Периодическая таблица - это систематическое представление всех химических элементов, расположенных в порядке возрастания атомных номеров. Она включает различные данные о каждом элементе, такие как его символ, атомный номер, атомная масса и химические свойства.
Какие элементы считаются щелочными металлами?
Щелочными металлами считаются элементы первой группы периодической таблицы: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они характеризуются низкой плотностью, мягкостью и активностью в реакциях с водой.
Какие элементы считаются инертными газами?
Инертными газами считаются элементы из группы 18 периодической таблицы, которая также называется группой благородных газов. К этим элементам относятся: гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радон (Rn). Их основное свойство - низкая химическая реактивность.
