P2O3 (триоксид фосфора) - это неорганическое соединение, состоящее из двух атомов фосфора и трех атомов кислорода. Вопрос о том, является ли P2O3 металлом или нет, вызывает интерес среди ученых и любителей химии.
Во-первых, для определения характера P2O3 следует рассмотреть его химическую структуру и свойства. По своей природе P2O3 является оксидом фосфора, что означает наличие связи между атомами фосфора и кислорода.
Второе важное свойство, которое следует учитывать, - это электроотрицательность атомов. Фосфор имеет электроотрицательность 2,1, а кислород - 3,5. Таким образом, кислород в P2O3 является более электроотрицательным элементом, что указывает на ионный характер соединения.
В заключение, P2O3 не является металлом. Оно имеет ионную структуру и формирует ионы фосфора и кислорода, а не металлическую решетку. Эта информация важна для понимания свойств и использования P2O3 в различных областях, таких как химическая промышленность и материаловедение.
Металлические свойства P2O3 химического соединения
Химическое соединение P2O3, также известное как фосфора оксид, обладает некоторыми металлическими свойствами. В основном это связано с его структурой и способностью проводить электрический ток.
Фосфора оксид образует кристаллическую решетку, атомы которой могут двигаться относительно своего положения. Это позволяет соединению иметь подвижность электронов и проводить ток.
Кроме того, фосфора оксид обладает высокой теплопроводностью. Это означает, что он способен эффективно передавать тепло по своей структуре, что является характерным для металлов.
Однако, P2O3 всё же не является полностью металлическим соединением. Его химические свойства более характерны для неметаллов. Оно обладает высокой электроотрицательностью и имеет тенденцию образовывать ковалентные связи с другими элементами.
Таким образом, можно сказать, что P2O3 обладает некоторыми металлическими свойствами, но его химическое поведение в целом более близко к неметаллам.
P2O3: общие сведения и свойства

P2O3 (тетраоксофосфат (III)) является химическим соединением, состоящим из двух атомов фосфора и трех атомов кислорода. Оно представляет собой оксид фосфора с формулой P2O3 и молярной массой 109,945 г/моль.
Тетраоксофосфат (III) обладает особыми свойствами, которые делают его полезным в различных областях. Оно является кристаллическим соединением, образующим бесцветные или светло-желтые кристаллы. Соединение растворимо в некоторых органических растворителях, таких как бензол и уксусная кислота.
Одним из основных свойств P2O3 является его реакция с водой. Когда соединение взаимодействует с водой, происходит гидролиз, в результате которого образуется фосфиновая кислота (PH3) и фосфорная кислота (H3PO4). Гидролиз P2O3 имеет большое практическое значение, так как является одним из методов получения фосфиновой кислоты.
Кроме того, P2O3 применяется в качестве катализатора в различных химических реакциях. Он активно используется в производстве эфиров и органических соединений, а также в синтезе фармацевтических препаратов и пестицидов.
Вывод: P2O3 является химическим соединением, обладающим уникальными свойствами. Оно может быть использовано как промежуточное вещество в различных процессах синтеза и имеет широкий спектр применения в различных отраслях промышленности.
Состав P2O3 и его применение

P2O3 - это химическое соединение, формула которого указывает на присутствие 2 атомов фосфора и 3 атомов кислорода. Вещество является безцветным и имеет кристаллическую структуру.
P2O3 применяется в различных областях, благодаря своим свойствам и составу. Оно является источником фосфора, который широко используется в химической промышленности для производства удобрений, пестицидов и многих других продуктов.
Кроме того, P2O3 используется в процессе синтеза органических соединений, таких как фосфорные эфиры и фосфонаты. Эти соединения могут применяться в качестве реактивов, катализаторов и компонентов лекарственных препаратов.
Некоторые производители также используют P2O3 в качестве компонента стекловолокна, которое применяется для производства изоляции и упаковки в электронике и других отраслях промышленности.
В целом, P2O3 является важным соединением, которое находит широкое применение в различных сферах деятельности человека и является источником фосфора для многих производственных процессов.
Физические свойства соединения P2O3

Соединение P2O3, известное также как дифосфортриоксид, обладает рядом уникальных физических свойств. Это бесцветное кристаллическое вещество с плотностью 2.39 г/см³. Температура плавления P2O3 составляет примерно 105°C, что делает его относительно низкотемпературным соединением.
Дифосфортриоксид является нелинейным молекулярным соединением, состоящим из двух атомов фосфора и трех атомов кислорода. В структуре P2O3 взаимодействие атомов фосфора и кислорода происходит посредством ковалентной связи, что придает соединению его химические свойства.
Помимо этого, дифосфортриоксид хорошо растворим в воде, образуя кислотные растворы. Данное соединение также обладает способностью окислять другие вещества, что делает его эффективным окислителем. P2O3 обладает также некоторыми важными применениями в промышленности, например, в производстве фосфорной кислоты и галофосфатов, а также в качестве катализатора.
Итак, физические свойства соединения P2O3 включают его бесцветный кристаллический вид, низкую температуру плавления, нелинейную молекулярную структуру, растворимость в воде и способность к окислительным реакциям. Все эти свойства делают P2O3 высокоинтересным веществом для исследования и применения в различных сферах науки и промышленности.
Химические свойства P2O3 и его реакции

P2O3 - одно из окислов фосфора, которое имеет особые химические свойства и обладает рядом интересных реакций.
Взаимодействие P2O3 с водой является экзотермическим процессом, сопровождающимся образованием кислорода и кислоты ортофосфорной, H3PO4:
- P2O3 + 3H2O → 2H3PO4
В реакции с кислородом P2O3 окисляется до P2O5. Эта реакция является важным промежуточным этапом в производстве гидроксифосфоновых кислот.
Реакция P2O3 с хлором приводит к образованию оксихлорида фосфора - P2O3Cl4:
- P2O3 + 2Cl2 → P2O3Cl4
Взаимодействие P2O3 с аммиаком дает гидроксиамин фосфоновую кислоту - NH4PO3:
- 4P2O3 + 10NH3 + 6H2O → 8NH4PO3
Также P2O3 может реагировать с оксидами металлов, образуя соль и фосфаты:
- P2O3 + 3Ag2O → 2Ag3PO3
- P2O3 + 3CuO → 2Cu3PO3
- P2O3 + 3ZnO → 2Zn3(PO3)2
Таким образом, P2O3 проявляет разнообразные реакции с другими веществами, что позволяет использовать его в различных химических процессах и синтезе соединений.
Влияние P2O3 на окружающую среду и здоровье человека

P2O3 (триоксид фосфора) – химическое соединение, которое может оказывать негативное влияние на окружающую среду и здоровье человека. Взаимодействие P2O3 с атмосферным воздухом может приводить к образованию опасного газа – фосфористого ангидрида (P2O5). Этот газ является раздражающим для слизистых оболочек дыхательных путей и может вызывать осложнения у лиц с заболеваниями дыхательной системы.
При попадании водных растворов P2O3 в природные водоемы происходит изменение их химического состава и нарушение биологического равновесия. Высокая концентрация фосфора в воде приводит к понижению концентрации кислорода и росту водорослей, что создает неблагоприятные условия для развития живых организмов.
Свинец – токсичный элемент, который часто находится в составе P2O3. Постоянное попадание этого соединения в почву приводит к загрязнению почвенного покрова и осуществляется дальнейший перенос токсичных веществ в растения, животных и, в конечном итоге, человека. Токсичность свинца может вызывать серьезные заболевания организма, такие как нарушение функций нервной системы, патология сердечно-сосудистой системы, а также влиять на фертильность.
Таким образом, P2O3 имеет негативное воздействие на окружающую среду и здоровье человека. Его использование и обращение должны осуществляться с особой осторожностью и строго соблюдать все правила и требования в области охраны окружающей среды и санитарно-гигиенические нормы.
Процесс получения P2O3 и особенности его производства
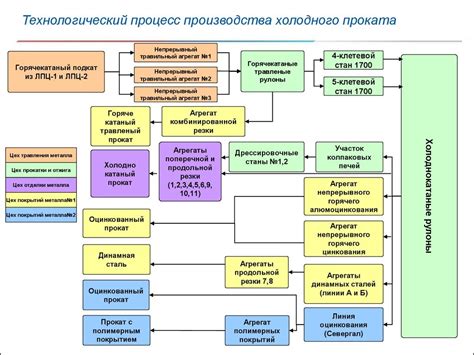
P2O3 - один из неорганических оксидов фосфора, который имеет важное применение в различных областях науки и промышленности. Этот соединение является весьма нетривиальным в получении, так как он обладает высокой реакционной способностью и подвержен разложению при невысоких температурах.
Основной метод получения P2O3 заключается в действии фосфора на кислород при температуре около 600-700 ℃. В этом случае происходит окисление фосфора, изначально находящегося в форме белого фосфора (P4), до оксида P2O3, который затем реагирует с водой, образуя фосфорную кислоту.
Процесс получения P2O3 требует осторожного контроля реакционных условий и тщательного удаления кислорода из области реакции. Для этого обычно используют инертные газы или методы вакуумной дистилляции, чтобы избежать окисления фосфора до других оксидов.
Полученный P2O3 может быть использован в различных областях, таких как производство фосфатных удобрений, электронная индустрия и катализаторы. Это соединение также является важным промежуточным продуктом в синтезе фосфорных кислот и других соединений фосфора. Благодаря своим уникальным свойствам, P2O3 играет важную роль в развитии различных научных и технических отраслей.
Использование P2O3 в промышленности и быту

P2O3 (триоксид фосфора) играет важную роль в различных отраслях промышленности и быту.
В химической промышленности P2O3 используется для производства фосфорных соединений, таких как фосфаты, фосфиты и фосфорные кислоты. Фосфаты широко используются в производстве удобрений, поскольку они являются основным источником фосфора для растений. Фосфиты применяются как антиоксиданты и стабилизаторы в пластике, резине и других материалах.
В быту P2O3 находит применение в производстве чистящих средств, таких как моющие порошки и жидкости для посуды. Он обладает отбеливающими свойствами и помогает удалять пятна и загрязнения. Также P2O3 используется в производстве стекла, поскольку он улучшает его прозрачность и прочность.
Триоксид фосфора также применяется в производстве электроники и полупроводников. Он используется для создания покрытий на электронных компонентах, таких как микрочипы и платы, чтобы обеспечить защиту от коррозии и улучшить проводимость.
В некоторых отраслях промышленности, P2O3 используется в качестве катализатора в химических реакциях. Он способствует ускорению реакции и повышает ее эффективность. Кроме того, P2O3 применяется в производстве огнеупорных материалов, где он обеспечивает высокую стойкость к нагреву и химическим воздействиям.
В целом, P2O3 является важным компонентом в промышленности и быту, благодаря своим разносторонним свойствам и способности быть использованным в различных областях деятельности.
Вопрос-ответ

Что такое P2O3 и может ли его назвать металлом?
P2O3 - это химическое соединение, которое состоит из двух атомов фосфора и трех атомов кислорода. Оно не является металлом, а является окислом фосфора.
Может ли P2O3 быть использован в качестве металла для производства изделий?
Нет, P2O3 не может быть использован в качестве металла для производства изделий, так как само по себе это окисл фосфора и не обладает металлическими свойствами.
Какие свойства у P2O3?
P2O3 обладает следующими свойствами: высокая температура плавления (в около 580°C), нерастворимость в воде, реакция с водой, активность в химических реакциях.
Какие еще соединения фосфора с кислородом существуют?
Кроме P2O3, существуют еще два главных окисла фосфора: P4O6 и P4O10. P4O6 имеет молекулярную структуру, а P4O10 - полимерную.
