Тема "Металлы" в химии изучает свойства, строение и особенности металлических элементов. Знание металлов является важным для понимания многих явлений и процессов в природе и технологиях.
Первоначально важно определить, что такое металл. Металлы - это химические элементы, обладающие специфическими свойствами: высокой теплопроводностью, электропроводностью, блеском, пластичностью и т.д. Они имеют определенный металлический блеск, проводят ток и тепло, а также хорошо восстанавливаются. Все металлы имеют определенную структуру, которая обеспечивает их уникальные свойства.
На контрольной работе по теме "Металлы" в 9 классе обычно задаются вопросы о строении и свойствах металлов, а также о способах получения металлов и их применении в различных отраслях промышленности. Важно помнить, что металлы имеют широкое применение в многих сферах жизни, будь то строительство, производство автомобилей или электроника.
Важно отметить, что металлы делятся на две основные группы: черные металлы и цветные металлы. Черные металлы, такие как железо и сталь, широко используются в строительстве и машиностроении. Цветные металлы, например медь и алюминий, обладают высокой коррозионной стойкостью и применяются в электронике, авиации и других отраслях промышленности.
Знание о металлах и их свойствах важно как для понимания окружающего мира, так и для применения их в практике. Надеемся, что данные готовые ответы помогут вам успешно справиться с контрольной работой и улучшить свои знания в области химии.
Основные понятия о металлах

Металлы - это группа химических элементов, которые обладают высокой проводимостью электричества и тепла, а также обладают способностью быть исполнителями формы. Они обладают специфической структурой, в которой атомы расположены в виде решетки.
Одним из главных свойств металлов является их способность отдавать электроны, что делает их хорошими проводниками электричества. Большинство металлов относится к активным элементам, что означает, что они легко образуют ионные соединения и реагируют с кислотами.
Металлы могут быть разделены на две крупные группы: легкие и тяжелые. Легкие металлы, такие как алюминий и магний, имеют низкую плотность и являются хорошими проводниками тепла и электричества. Они также обладают высокой реактивностью и способностью образовывать оксиды. Тяжелые металлы, такие как железо и свинец, имеют более высокую плотность и являются менее реактивными.
Металлы имеют широкий спектр использования в нашей жизни. Они часто используются в строительстве, машиностроении, электронике, производстве автомобилей и многих других областях. Металлы также играют важную роль в медицине, так как они используются для создания медицинских инструментов и имплантатов.
Физические свойства металлов
Проводимость: Металлы обладают хорошей электропроводностью и теплопроводностью. Это объясняется наличием свободных электронов, которые могут передвигаться внутри металлической структуры. Именно поэтому металлы широко применяются в электрических проводах и теплообменных устройствах.
Пластичность и упругость: Металлы обладают высокой пластичностью и упругостью, что позволяет их легко деформировать без разрушения. Благодаря этому свойству металлы применяются в процессе ковки, проката и формирования различных изделий.
Твердость и плавление: Металлы часто обладают высокой твердостью, однако существуют и металлы, которые можно нарезать ножом. Также металлы обладают высокой температурой плавления, что позволяет им использоваться в качестве строительных материалов в условиях высоких температур и сопротивляться механическим воздействиям.
Отсутствие прозрачности: Металлы обычно не пропускают свет, и поэтому не прозрачны. Однако некоторые металлы могут быть полупрозрачными, например, тонкопленочные металлы, которые широко применяются в солнечных батареях и стеклопокрытиях.
Магнитные свойства: Некоторые металлы, такие как железо, никель и кобальт, обладают магнитными свойствами. Они притягиваются к магниту и могут потерять свои магнитные свойства при нагревании или воздействии других факторов.
Свойства окрашивания: Некоторые металлы, в особенности переходные металлы, способны изменять цвет при окислении или образовании различных соединений. Это свойство позволяет использовать металлы для создания красителей и пигментов в художественной и промышленной областях.
Химические свойства металлов

Металлы обладают рядом характерных химических свойств, которые определяются строением и атомными связями в их кристаллической решетке.
Одной из основных характеристик металлов является их способность образовывать ионные соединения. Металлы могут отдавать электроны и образовывать положительно заряженные ионы, которые притягиваются отрицательно заряженными ионами или молекулами веществ, с которыми они вступают в реакцию.
Металлы также способны реагировать с кислородом, образуя основные оксиды. При этом происходит окисление металла, при котором он теряет электроны. Основные оксиды металлов обладают щелочными свойствами и взаимодействуют с водой, образуя гидроксиды.
Еще одной характерной особенностью металлов является их способность реагировать с кислотами. При этом металлы отдают электроны и образуют положительно заряженные ионы. В результате таких реакций образуются соли металлов и выделяются водородные ионы.
Также металлы обладают высокой теплопроводностью и электропроводностью, что связано с их способностью перемещаться электроны внутри кристаллической решетки.
Реакции металлов с кислотами

Металлы, находящиеся в плоскости активного ряда, могут реагировать с различными кислотами. Под воздействием кислот металлы могут проявлять различные свойства, изменяться и образовывать новые вещества.
Реакция металлов с кислотой может проходить с образованием солей и выделением водорода. В зависимости от активности металла и концентрации кислоты, реакция может протекать медленно или бурно, с выделением тепла и образованием пузырьков газа.
Например, металл натрий, реагируя с соляной кислотой, образует хлорид натрия и выделяет водород. Реакция может быть представлена следующим уравнением: 2Na + 2HCl → 2NaCl + H2.
Металлы могут также реагировать с другими кислотами, такими как серная кислота, азотная кислота и уксусная кислота. При этом образуются соответствующие соли и выделяются газы.
Реакции металлов с водой

Реакция металлов с водой является одним из основных способов проявления химических свойств металлов. Многие металлы, например, щелочные металлы (натрий, калий), реагируют с водой мгновенно и ярко. При этом выделяется газ водород, и в результате образуется основание – гидроксид металла.
Однако не все металлы реагируют с водой. Некоторые, например, нобелевы металлы, практически инертны по отношению к воде и не проявляют химическую активность при контакте с ней. Для таких металлов реакция с водой происходит лишь при нагревании или в присутствии катализаторов.
Важно отметить, что реакции металлов с водой могут быть разными. Некоторые металлы, например, цинк и железо, обладают способностью сорбировать воду на своей поверхности и выделять при этом водород. Другие металлы, например, олово и свинец, реагируют с водой только при высокой температуре.
Таблица ниже представляет реакции различных металлов с водой:
| Металл | Реакция с водой |
|---|---|
| Натрий (Na) | 2Na + 2H2O = 2NaOH + H2 |
| Калий (K) | 2K + 2H2O = 2KOH + H2 |
| Цинк (Zn) | Zn + H2O = ZnO + H2 |
| Железо (Fe) | 3Fe + 4H2O = Fe3O4 + 4H2 |
Таким образом, реакции металлов с водой являются важным проявлением их химической активности и используются для получения оснований и водорода в промышленности и научных исследованиях.
Реакции металлов с кислородом

Многие металлы реагируют с кислородом, образуя оксиды. Реакции такого рода широко распространены и часто применяются в производстве и в ежедневной жизни. Некоторые из этих реакций металлов с кислородом могут проходить с выделением тепла.
Например, алюминий, реагируя с кислородом из воздуха, образует оксид алюминия(III), который имеет формулу Al2O3. В результате этой реакции выделяется большое количество тепла, отчего она протекает экзотермически. Оксид алюминия(III), или алюминиевая глина, широко используется в строительстве и производстве керамики.
Железо, реагируя с кислородом воздуха, образует оксид железа(III), который имеет формулу Fe2O3. Этот оксид, или ржавчина, является одним из наиболее распространенных веществ в природе. Он используется в производстве стали, окрашивании и защите поверхностей, а также в других промышленных процессах.
Таким образом, реакции металлов с кислородом являются важной частью изучения химии металлов и находят широкое применение в промышленности и быту.
Процессы коррозии металлов
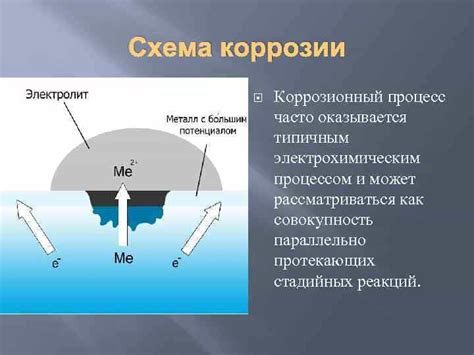
Коррозия металлов представляет собой процесс разрушения металлических материалов под воздействием окружающей среды. Она может привести к потере прочности и долговечности конструкций и изделий из металла. Причиной коррозии является электрохимическое взаимодействие между металлом, окружающей средой и влагой.
Коррозия происходит в несколько этапов. Вначале на поверхности металла образуется окисная пленка, которая обычно обеспечивает защиту металла от дальнейшей коррозии. Однако, при наличии избытка влаги или агрессивных веществ в окружающей среде, пленка может быть разрушена, и начинается активный процесс коррозии.
Существует несколько видов коррозии металлов. Одним из наиболее распространенных видов является питание-контактная коррозия, которая возникает при взаимодействии двух различных металлов в присутствии влаги и электролита. Еще один вид коррозии - поверхностная коррозия, которая происходит на поверхности металла из-за воздействия окружающей среды.
Для предотвращения коррозии металлов применяются различные методы защиты. Один из них - нанесение защитного покрытия на поверхность металла. Также используются катодная защита, анодная защита и использование специальных антикоррозионных материалов. Важно знать, что правильное хранение и обращение с металлическими изделиями также способствуют предотвращению коррозии.
Применение металлов в повседневной жизни

Металлы играют важную роль в нашей повседневной жизни. Они используются в различных отраслях и областях, поскольку обладают набором уникальных свойств, таких как прочность, пластичность и проводимость.
Одним из наиболее распространенных применений металлов является строительство. Железо, сталь и алюминий используются для создания каркасов зданий, мостов и других сооружений. Они обеспечивают надежность и долговечность конструкций. Кроме того, металлы используются для производства облицовочных и отделочных материалов, таких как кровельные листы, оконные рамы и двери.
Металлы также играют важную роль в производстве транспортных средств. Алюминий, медь и сталь используются для создания кузовов автомобилей, корпусов самолетов и кораблей. Они обладают не только прочностью, но и легкостью, что позволяет увеличить эффективность транспортных средств и снизить расход топлива.
Еще одной областью применения металлов является электроника. Медь и алюминий используются для производства проводов и плат, а также для создания различных компонентов электронных устройств. Благодаря своей проводимости, металлы обеспечивают эффективное передачу сигналов и электроэнергии.
Кроме того, металлы находят применение в медицине. Титан используется для создания имплантатов, таких как искусственные суставы и пластины для фиксации костей. Это обеспечивает пациентам возможность восстановления после травм или замены поврежденных суставов.
В заключение, металлы являются неотъемлемой частью нашей повседневной жизни. Они применяются в строительстве, транспорте, электронике и медицине, обеспечивая нам прочность, функциональность и комфорт. Благодаря своим уникальным свойствам, металлы стали незаменимыми материалами в современном мире.
Вопрос-ответ

Какие металлы относятся к активным?
Активными металлами являются калий, натрий, кальций, магний, алюминий, цинк, железо, свинец и медь.
Какие металлы относятся к недостаточно активным?
Недостаточно активными металлами являются серебро, золото и платина.
Что такое коррозия металлов?
Коррозия металлов - это процесс их разрушения под действием окружающей среды или химически активных веществ.
Что такое реакция металла с кислотой?
Реакция металла с кислотой - это химическая реакция, при которой металл взаимодействует с кислотой, образуя соль и выделяяся водород.
Какие металлы используются для получения электроэнергии?
Для получения электроэнергии используются такие металлы, как железо, алюминий и медь.
